对抗知识焦虑,从看懂这条开始
App 下载
白血病干细胞的隐身术被破,75%难治患者获缓解
联合疗法|侯宇教授|MMRN1蛋白|白血病干细胞|急性髓系白血病|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
联合疗法|侯宇教授|MMRN1蛋白|白血病干细胞|急性髓系白血病|肿瘤学|医学健康
对于复发/难治性急性髓系白血病(AML)患者来说,传统化疗和免疫治疗的有效率不足30%,大部分人最终会被体内的白血病干细胞拖入绝境——这些像“不死种子”的细胞不仅能躲避免疫系统的追杀,还能不断自我更新,让癌症卷土重来。2026年4月,重庆医科大学侯宇教授联合多团队的研究,终于撬开了这些干细胞的“隐身密码”:他们发现了一个名为MMRN1的蛋白,正操控着白血病干细胞的双重生存技能,而针对它的联合疗法,已让75%的难治患者获得缓解。
你可以把白血病干细胞想象成一个精通伪装和分身的“逃犯”,而MMRN1就是它的“全能助手”。
首先是“隐身术”:MMRN1通过自身的EGF样结构域激活EGFR/STAT1信号通路,像按下了“糖链合成加速键”——它阻止细胞表面的唾液酸(一种带负电的糖类)被降解,让大量唾液酸糖链在干细胞表面堆积。这些糖链就像给干细胞套上了一层“免疫伪装衣”,能和免疫细胞表面的Siglec受体结合,传递“别杀我”的抑制信号,直接废掉T细胞和NK细胞的攻击能力。这是一种和PD-1/CTLA-4完全不同的“糖免疫检查点”,也是之前免疫治疗对AML效果不佳的关键原因。
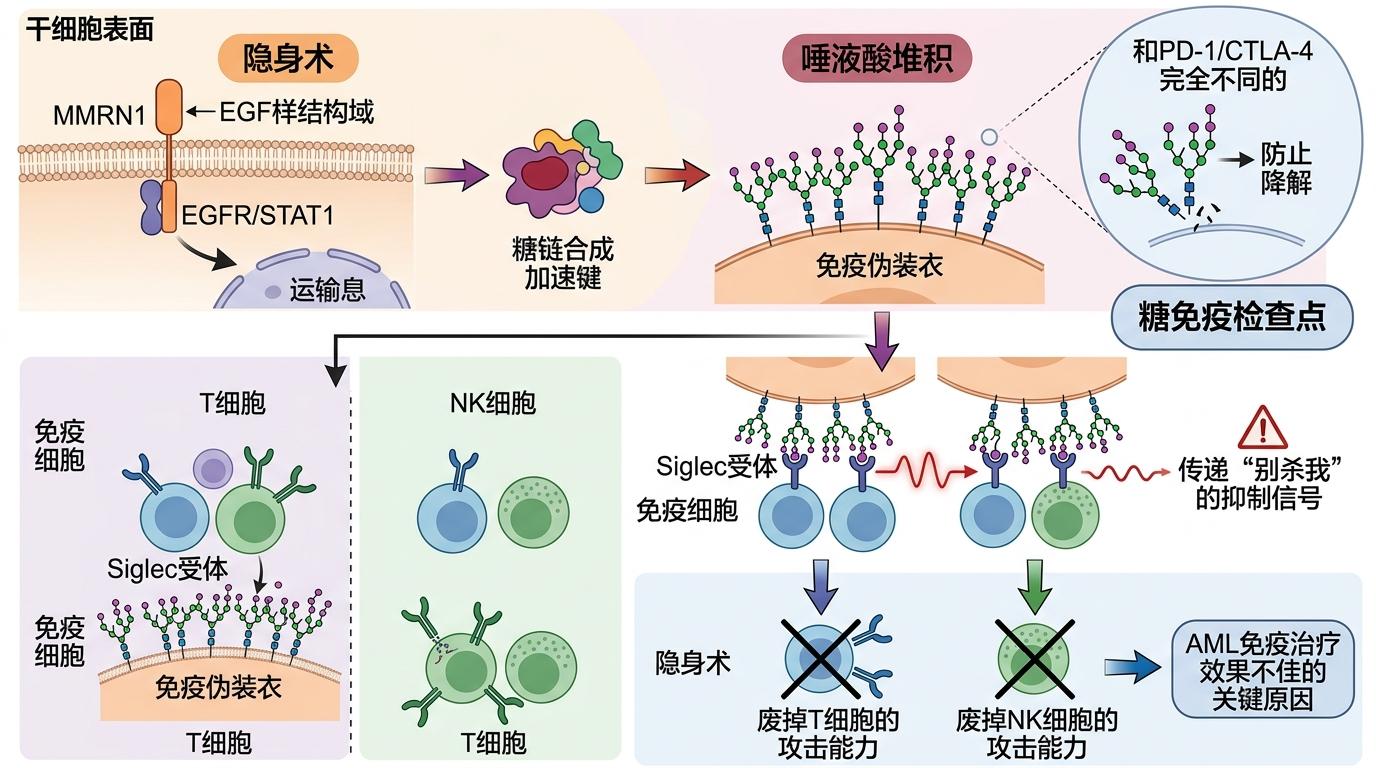
然后是“分身术”:MMRN1还能通过EGFR/STAT5/CD9通路,维持白血病干细胞的自我更新能力。简单来说,就是让这些“种子细胞”不断分裂出和自己一样的“不死分身”,哪怕化疗杀死了大部分普通白血病细胞,只要有这些干细胞在,癌症就会复发。
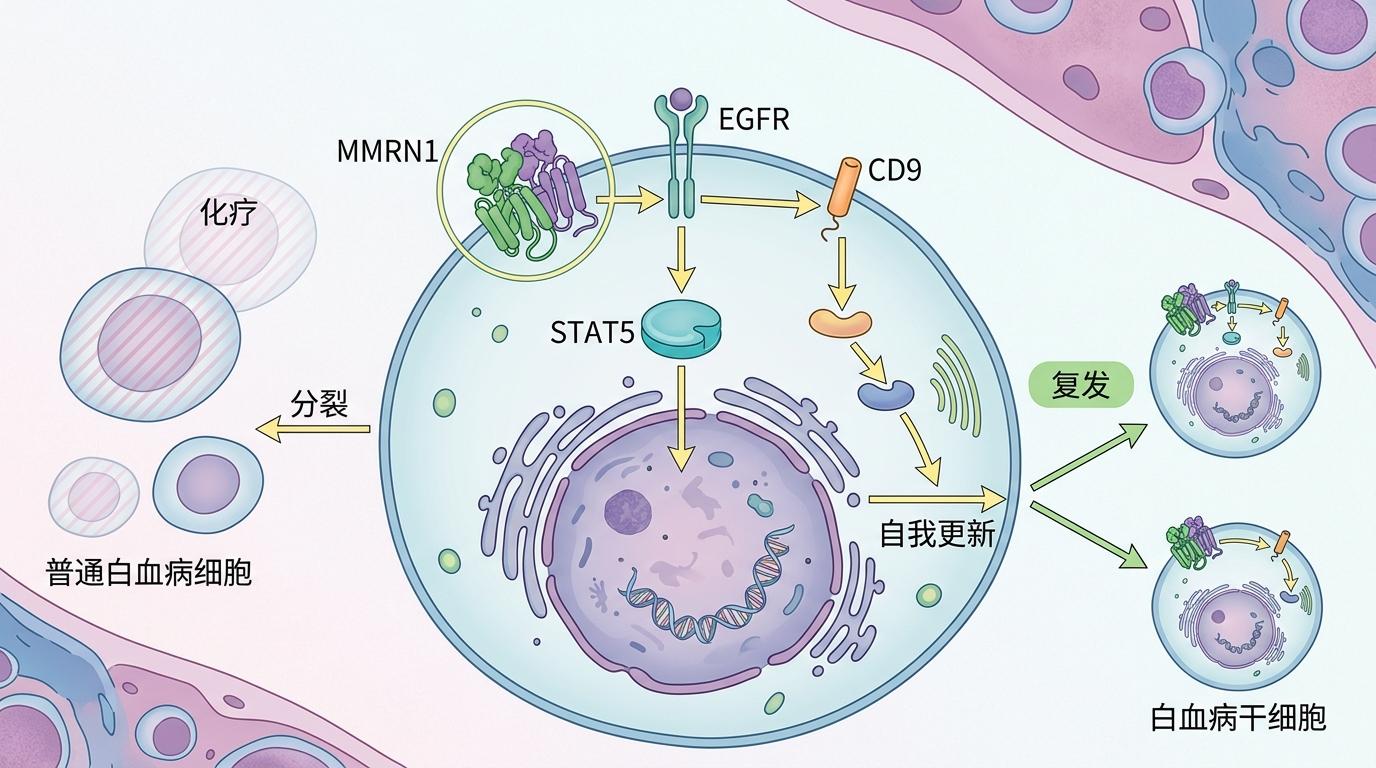
更关键的是,MMRN1只在白血病干细胞和少数正常造血干细胞中高表达,这意味着靶向它不会像化疗那样“不分敌我”地杀伤正常细胞。
研究团队先是在小鼠模型和患者来源的细胞中验证了MMRN1的作用:敲除MMRN1后,白血病干细胞的“隐身衣”消失了,免疫细胞能顺利识别并杀死它们,同时干细胞的自我更新能力也被大幅削弱,AML的进展被显著延缓。更惊喜的是,敲除MMRN1后再使用PD-1/CTLA-4抑制剂,免疫治疗的效果直接翻倍——原本对免疫治疗不敏感的AML细胞,在“伪装衣”被脱掉后,终于成了免疫细胞的靶子。
在此基础上,他们设计了针对MMRN1-EGFR信号轴的临床方案:用EGFR抑制剂厄洛替尼,联合阿扎胞苷和经典的HAG化疗方案(高三尖杉酯碱、低剂量阿糖胞苷、粒细胞集落刺激因子)治疗复发/难治性AML患者。初步临床试验结果显示,75%的患者获得了缓解,这个数字比传统治疗的30%有效率高出一倍还多。
不过研究团队也坦诚,目前的方案并非完美:EGFR抑制剂可能会带来皮疹、腹泻等副作用,而且部分患者可能会出现耐药。此外,MMRN1在不同AML亚型中的表达水平有差异,如何精准筛选适合的患者,还需要更大规模的研究。
这次研究最核心的突破,其实是找到了AML免疫逃逸的“新靶点”——糖免疫检查点。
传统的PD-1/CTLA-4免疫检查点是蛋白层面的“刹车”,而糖免疫检查点是细胞表面糖链和免疫受体的结合,属于更上游的免疫调控机制。在AML、胰腺癌等多种癌症中,癌细胞都会通过高表达唾液酸糖链来逃避免疫攻击,这也是很多患者对免疫治疗无反应的原因。
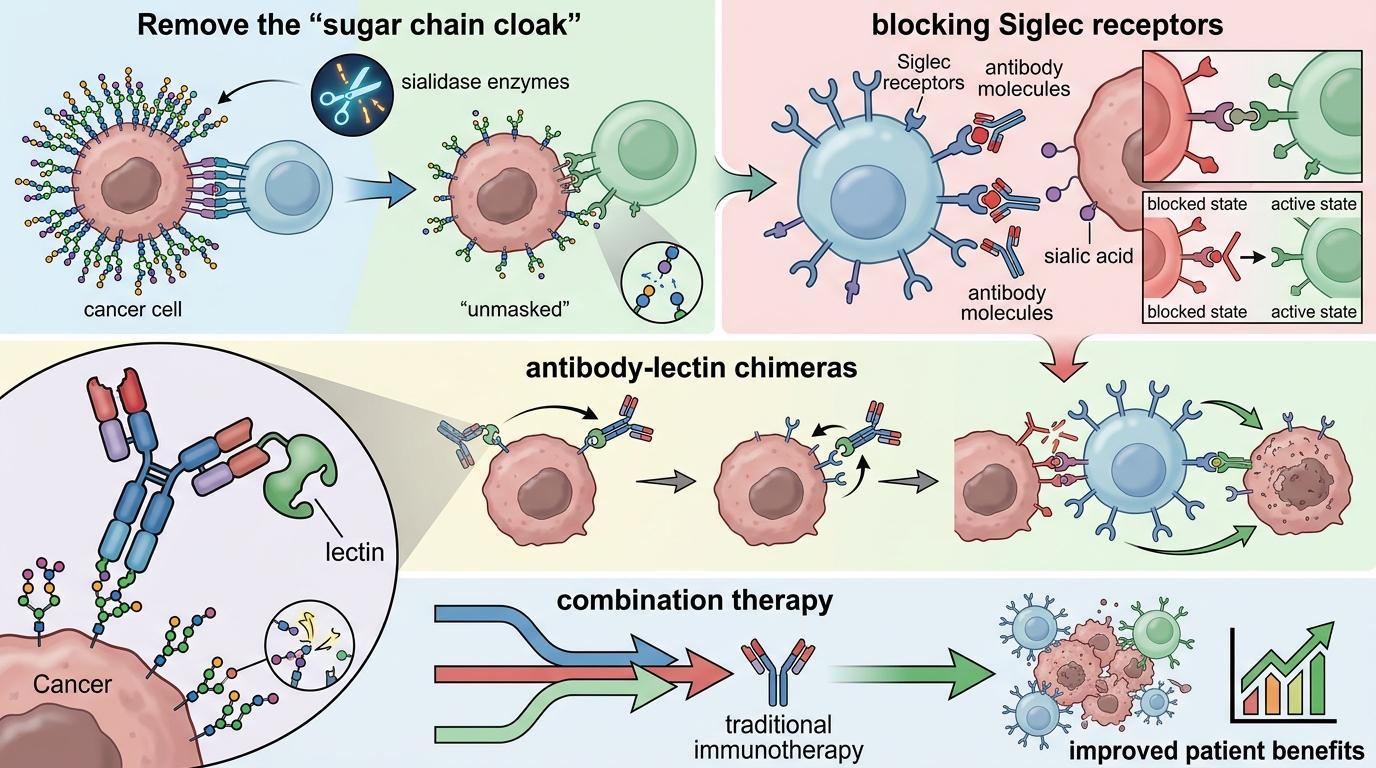
除了靶向MMRN1-EGFR通路减少糖链合成,科学家还在探索其他破局方法:比如用唾液酸酶去掉癌细胞表面的糖链“伪装衣”,或者开发能阻断Siglec受体的抗体,甚至设计“抗体-凝集素嵌合体”,一边识别癌细胞,一边阻断糖免疫检查点的抑制信号。这些方法都在实验室阶段显示出了潜力,未来可能和传统免疫治疗联合使用,让更多癌症患者获益。
从发现MMRN1的作用机制,到临床试验取得75%的缓解率,这场针对白血病干细胞的“围剿战”,只用了短短几年时间。但这只是一个开始:我们还需要更精准的靶点筛选方法,更安全的靶向药物,以及能破解耐药问题的联合方案。
癌症的狡猾之处,就在于它总能找到新的生存策略。但每一次对它生存逻辑的破解,都是在为患者多争取一分生机。靶点藏在糖链里,希望藏在细节中。未来的癌症治疗,终将是一场精准到分子层面的“狙击战”,而我们已经摸到了扳机。