
9 天前

9 天前
当AI能从一串氨基酸序列里精准算出蛋白质的三维结构时,生物学家本该欢呼——毕竟结构是功能的钥匙。但哥伦比亚大学的Hashim Al-Hashimi教授却泼了盆冷水:我们要的从来不是静态的“分子照片”,而是RNA在细胞里“干活”的效率——这才是破解遗传疾病、开发新药的核心。
现在,他的团队在《Cell》上发表的研究,终于给了RNA活性预测一个可行的答案:不是靠AI的黑箱拟合,而是回归最朴素的生物物理原理。更关键的是,他们发现了RNA活性的真正密码,藏在它不停变化的“结构集合”里。为什么有些RNA突变会彻底废掉病毒复制能力,有些却毫无影响?答案就藏在这个动态的分子世界里。
你可以把RNA想象成一个永远坐不住的小孩——它不会乖乖保持一个姿势,而是在皮秒到毫秒的时间里,不停切换着不同的折叠形状,这就是结构集合(ensemble):一系列构象的动态平衡。
有些构象稳定,能在集合里占90%以上的“出镜率”;有些却像昙花一现,只占0.4%的比例,寿命短到2.1毫秒。但恰恰是这些罕见的“激发态”构象,往往是RNA执行功能的关键——比如HIV的TAR RNA,就是靠一个短暂的构象结合病毒蛋白,启动复制。
传统的结构解析技术,比如X射线晶体学,只能拍到这些构象的“平均照片”,根本抓不住那些转瞬即逝的功能态。而Al-Hashimi团队的突破,正是先通过无标记NMR技术,精准测定了HIV TAR RNA及其27种单点突变体的完整结构集合——包括每个构象的比例、稳定性,甚至切换速度。
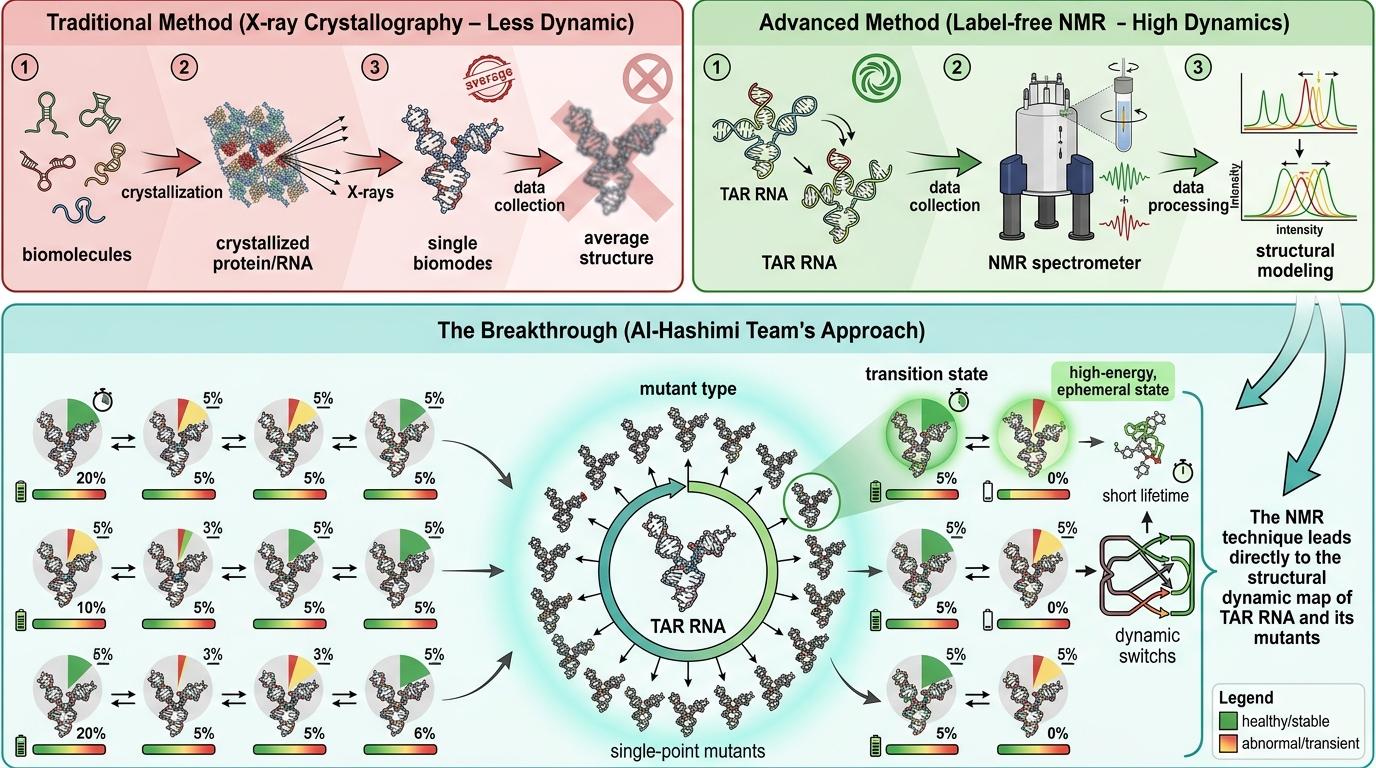
他们发现,一个单点突变就能让活性构象的比例变化500倍,直接导致病毒复制效率下降300倍。这也解释了为什么有些RNA位点在进化中高度保守:不是因为它们直接参与分子结合,而是因为它们是维持整个结构集合平衡的“支点”——这就是他们提出的新概念**结构集合保守性**。
Al-Hashimi团队没有用AI训练海量数据,而是基于已知的RNA二级结构热力学模型,搭建了一个能从序列直接预测结构集合的框架。这个模型的逻辑很直接:
他们用HIV的TAR RNA验证了模型:输入27种突变体的序列,模型预测的活性和实验测量结果完全吻合。更重要的是,这个模型还能推广到另一种HIV调控RNA RRE,理论上适用于所有小调控RNA。
和AI模型相比,这个生物物理模型的优势在于“可解释”——它能清晰告诉你,哪个碱基突变改变了哪个构象的比例,又如何影响了活性,而不是给你一个看似精准却无从追溯的黑箱结果。当然它也有局限:目前只能处理小RNA,面对更长、更复杂的mRNA,还需要结合AI来拓展构象采样的效率。
这个模型给RNA靶向药物开发打开了新的大门。传统药物设计遵循“锁钥原理”——找到一个静态的靶点,设计对应的小分子。但RNA是动态的“变形者”,传统方法往往抓不住真正的功能态。
现在,科学家可以先预测RNA的结构集合,找到那些低丰度但高活性的构象,再设计小分子去稳定它或者干扰它——比如针对HIV TAR RNA的活性构象,设计药物让它无法结合病毒蛋白,从而阻断复制。在遗传病领域,这个模型也能解释为什么有些RNA突变会致病:不是因为破坏了静态结构,而是因为打乱了结构集合的平衡。
但从实验室到临床,还有三道坎:首先是如何把模型拓展到更长的RNA分子;其次是如何在细胞内直接验证结构集合的变化——毕竟试管里的测量和细胞内的真实环境还有差距;最后是递送难题,RNA药物要进入细胞发挥作用,还需要更高效的载体。
当我们为AI的“万能”欢呼时,Al-Hashimi团队的研究像一个提醒:生命的本质是动态的平衡,不是静态的结构。AI能帮我们快速找到分子的“快照”,但要理解生命的“动态电影”,最终还是要回归到生物物理的基本原理。
结构即平衡,平衡即功能。这句话不仅适用于RNA,也适用于整个生命世界。未来的精准医疗,或许不是找到一个静态的靶点,而是学会调控一个动态的平衡——就像给那个永远坐不住的RNA小孩,找一个能让它好好干活的“姿势”。
点击充电,成为大圆镜下一个视频选题!