对抗知识焦虑,从看懂这条开始
App 下载
心梗后炎症的隐秘推手,被中国科学家找到了
RNA结合蛋白|山东大学|炎症风暴|心脏巨噬细胞|ILF3蛋白|心脑血管疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
RNA结合蛋白|山东大学|炎症风暴|心脏巨噬细胞|ILF3蛋白|心脑血管疾病|医学健康
当心肌梗死发生,最致命的往往不是最初的细胞坏死——而是随后爆发的炎症风暴。这些本应清理坏死组织的免疫细胞,会在失控后反过来啃食健康心肌,把暂时的损伤拖成终身的心力衰竭。过去几十年,科学家们一直在寻找这场风暴的“开关”,却始终卡在复杂的免疫网络里。直到2026年4月,山东大学、中科大、北京安贞医院的联合团队,在心脏巨噬细胞里抓住了那个真正的“点火者”。
研究团队先对比了急性心梗患者和健康人的心脏样本,又在小鼠模型里反复验证,最终锁定了一个名为白细胞介素增强子结合因子3(ILF3)的RNA结合蛋白——它在急性心梗后的巨噬细胞里含量飙升,而且炎症越重、心脏功能越差,它的水平就越高。
为了确认ILF3的“恶行”,他们做了一个关键实验:在小鼠的巨噬细胞里特异性敲除ILF3基因。结果很直接:心梗后的炎症反应被砍掉了一大半,小鼠的心脏射血分数提升了近20%,原本会变形的心室也保持了更规整的形态。
这相当于在一场失控的火灾里,发现了不断往火堆里添柴的人——只要把他拉走,火势就能迅速得到控制。
ILF3到底是怎么“添柴”的?研究团队顺着这条线索往下挖,揪出了一条环环相扣的分子链条:
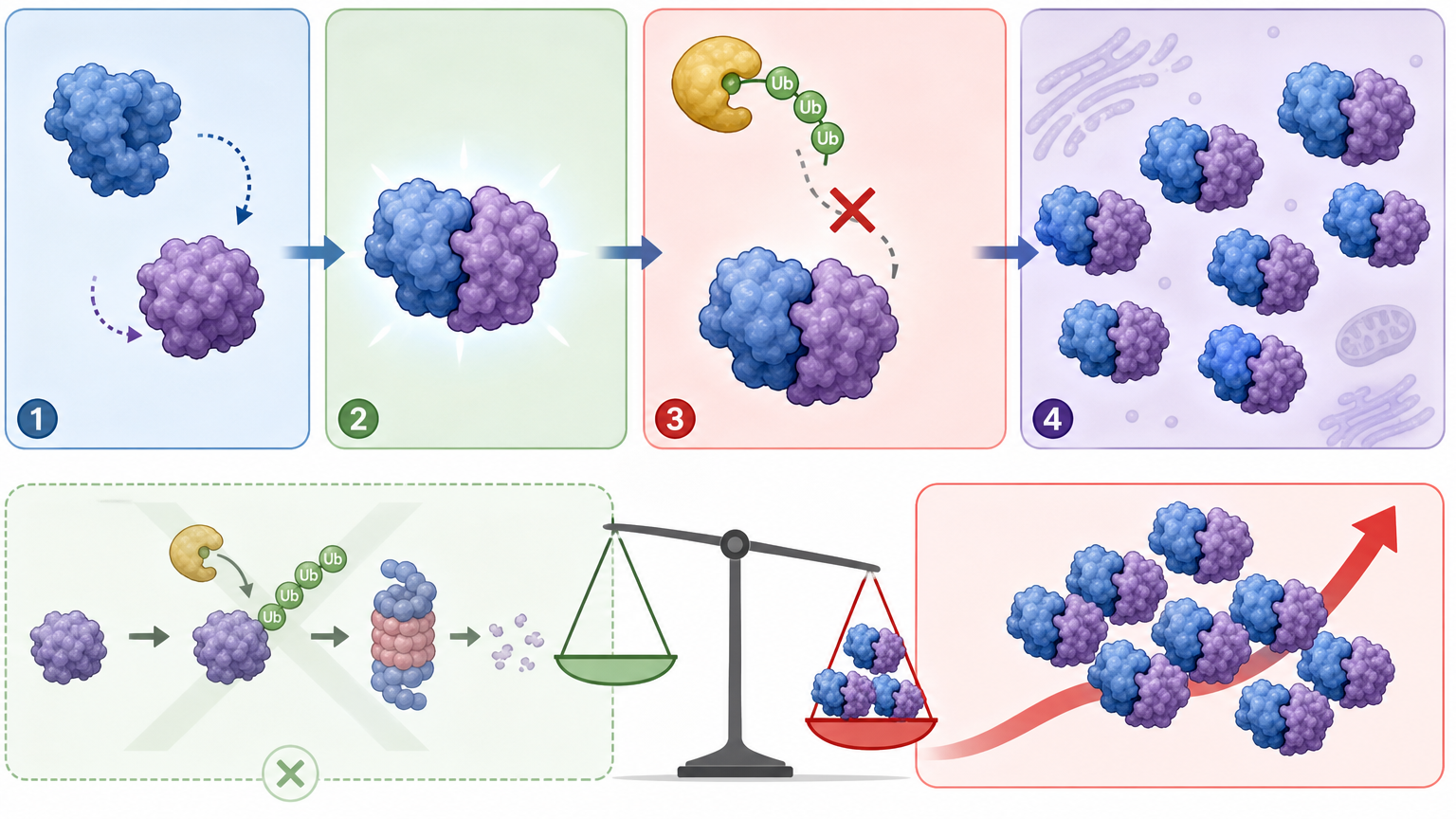
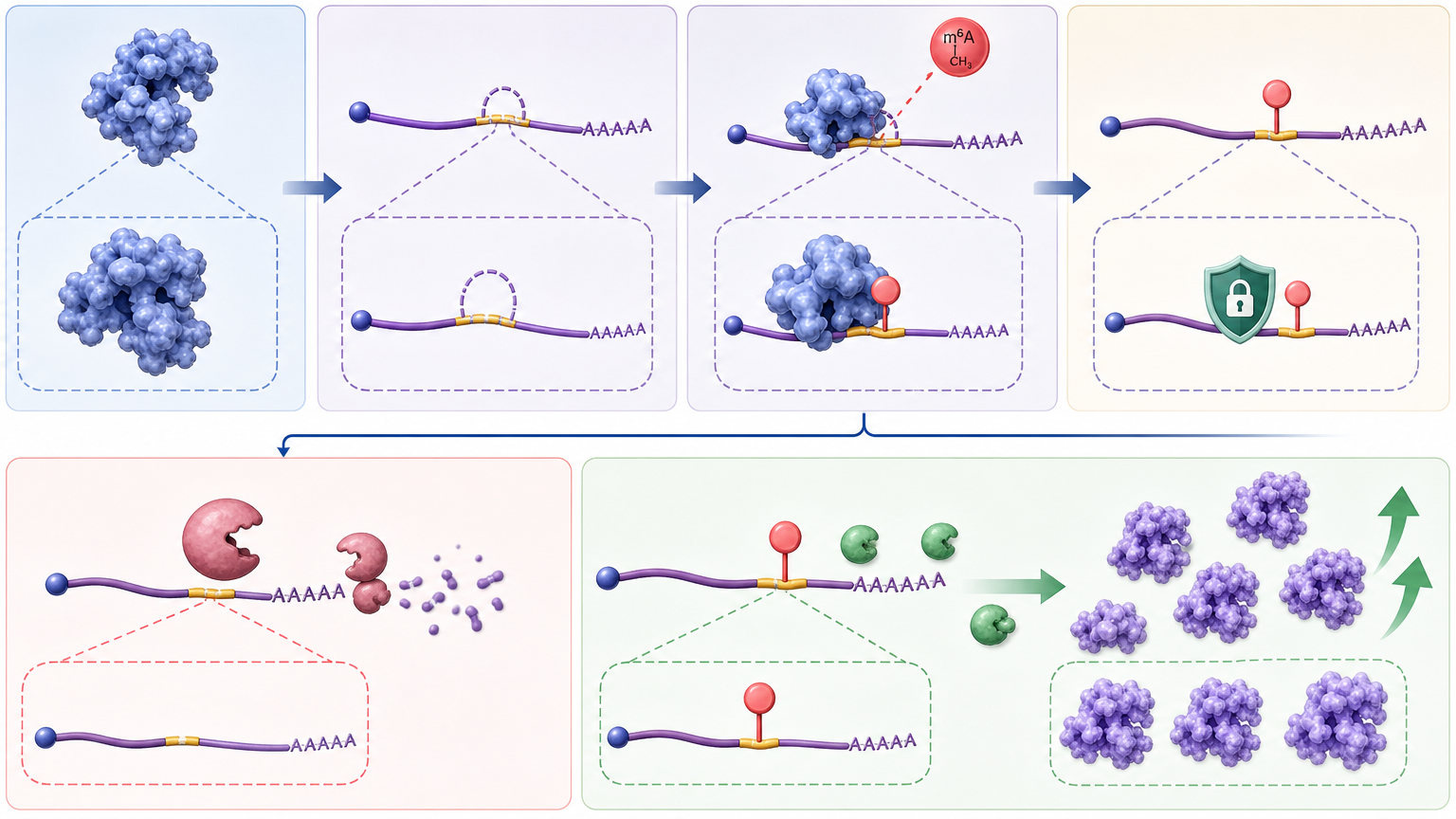
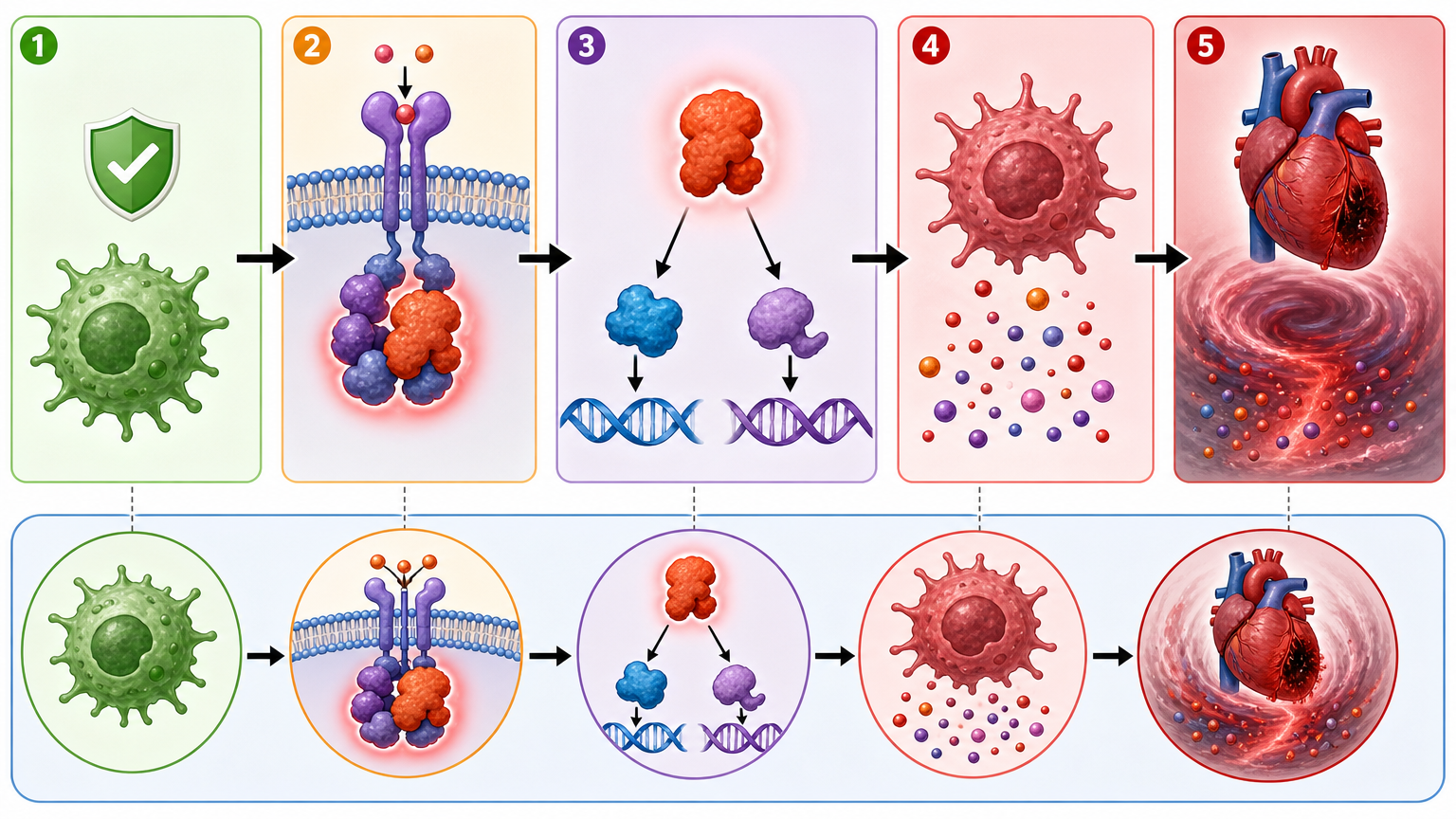
简单说,ILF3就是这场风暴的“启动器”,HNRNPA2B1是“传令兵”,IRAK4是“机枪手”,三者连在一起,就成了心梗后心脏的“自杀链条”。
既然理清了链条,干预的方向就明确了。研究团队验证了三个靶点:敲除ILF3有效,抑制HNRNPA2B1有效,直接阻断IRAK4的活性也有效——三个环节里任何一个被打断,炎症风暴都会被显著抑制,心脏修复的进程都会加快。
更重要的是,这条ILF3/HNRNPA2B1/IRAK4轴在人和小鼠身上高度保守,意味着针对它开发的药物,很可能在人体里也能发挥同样的效果。目前已经有针对IRAK4的小分子抑制剂进入临床试验,主要用于自身免疫病,这次的研究相当于给这些药物找到了一个新的适应症方向。
当然,风险也存在:m6A修饰是细胞里的通用调控机制,非特异性的干预可能影响正常细胞的功能;而且心梗后的炎症并非全是坏事,早期的炎症是清理坏死组织的必要环节,如何精准把握干预的时间窗,避免“杀敌一千自损八百”,还需要更多临床研究。
过去我们总把心梗后的炎症当成“必要的恶”,以为只能被动承受它的副作用。但这次的研究让我们看到,炎症不是一场无差别爆炸,而是有精确开关和传导链条的可控反应。
精准掐断炎症的“点火链”,才是心脏修复的关键。
未来的心梗治疗,或许不再是单纯的溶栓、搭桥,而是在打通血管的同时,精准地给炎症风暴踩下刹车——让免疫细胞回到“清理工”的本职,而不是变成“破坏者”。这不仅是分子生物学的突破,更是给千万心梗患者的心脏,多留了一条生路。