对抗知识焦虑,从看懂这条开始
App 下载
一滴血查乳腺癌早筛、分型、转移全搞定
影像漏诊|浙江大学医学院附属第二医院|cfDNA检测|游离DNA|乳腺癌早筛|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
影像漏诊|浙江大学医学院附属第二医院|cfDNA检测|游离DNA|乳腺癌早筛|肿瘤学|医学健康
26个女性拿着超声和钼靶的报告松了口气——结果显示她们的乳腺只是BI-RADS 3级的良性病变。可后续病理切片却给了沉重一击:其中25人其实患上了早期乳腺癌,全部被影像检查漏诊了。这不是极端案例,在亚洲女性致密性乳腺中,钼靶的漏诊率能超过50%;超声则依赖医生经验,对未形成肿块的早期病变束手无策。而曾经被寄予厚望的液体活检,要么早期检出率不足20%,要么特异性堪忧。现在,浙江大学医学院附属第二医院的团队找到了新的突破口:从血液里的游离DNA碎片里,读出极早期乳腺癌的信号。
你可以把血液里的游离DNA(cfDNA)想象成细胞死亡后散落的“基因碎片”——正常细胞死亡后,这些碎片会保持166bp左右的统一长度,像整齐切割的纸条;但肿瘤细胞的碎片却会变得更短、更杂乱,断裂的位置、末端的碱基序列都带着独特的“指纹”。
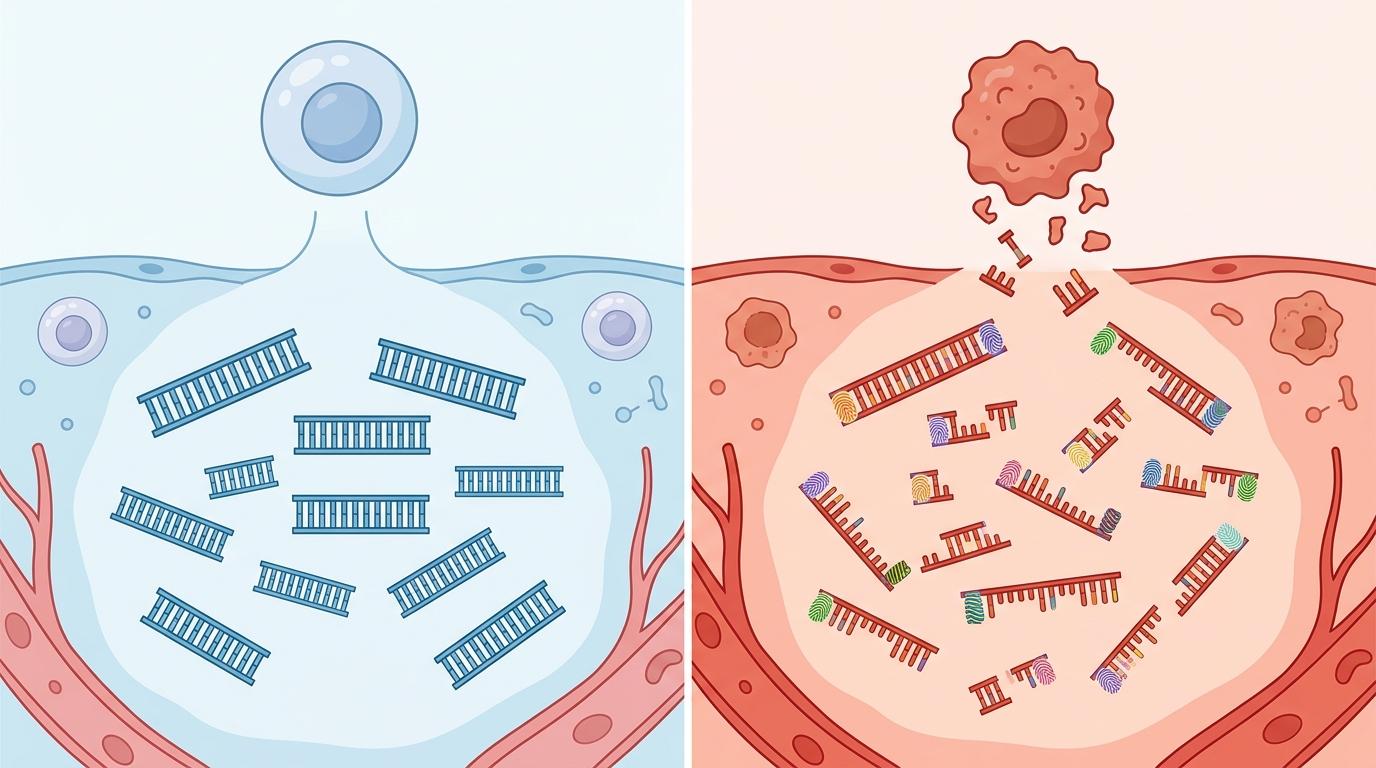
过去的液体活检要么盯着突变基因,要么看甲基化标记,可早期肿瘤释放的突变DNA太少,很难捕捉到。而这项研究的思路完全不同:它不找某个特定的“癌症标记”,而是用机器学习模型分析数千个维度的碎片特征——长度分布、末端碱基、断裂位置、重复元件频率……就像通过比对一整箱碎纸的切割痕迹,判断它是被剪刀整齐裁剪,还是被暴力撕碎。
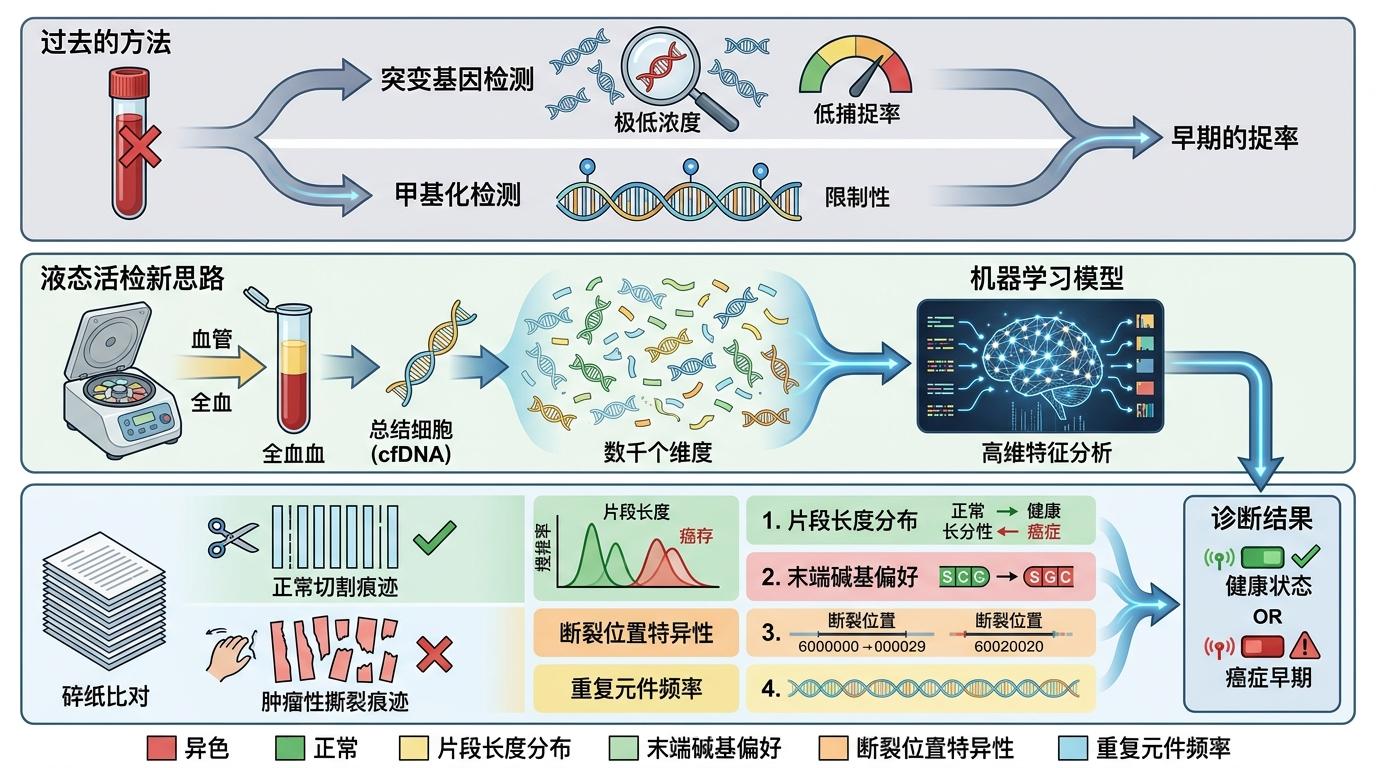
研究团队用503例乳腺癌患者和289例良性对照样本训练模型,最终实现了:训练集95%的灵敏度、78%的特异性,验证集92%的灵敏度、87%的特异性。更关键的是,那些被影像漏诊的25名早期患者,全部被这个模型准确识别。
这项技术的厉害之处,在于它不止能“查有没有癌”,还能一次性完成三件事:极早期检测、分子分型、判断淋巴结是否转移。
乳腺癌的分子分型直接决定治疗方案——管腔型用内分泌治疗,HER2阳性用靶向药,三阴性只能化疗。过去要靠穿刺活检才能分型,现在只需分析cfDNA碎片的末端基序、断点特征,就能高精度区分三种亚型,甚至对已经转移的患者,预测转移灶分型的准确率也能达到85.7%。
更让临床医生兴奋的是淋巴结转移的预测。传统影像对淋巴结转移的阴性预测值只有0.7-0.8,也就是说每10个被判断为阴性的患者里,就有2-3人其实已经转移。而这个模型的阴性预测值能达到97.6%——如果能在后续前瞻性研究中验证这一点,意味着大量患者可以避免不必要的腋窝淋巴结清扫,减少术后上肢水肿、活动受限等并发症。
当然,这项技术也有自己的局限。比如血栓、自身免疫病患者的cfDNA碎片也可能出现异常,目前的模型会把这类人群排除在外。研究团队的策略是“先解决90%核心人群的问题”——毕竟这些特殊病例在普通筛查人群中占比极低,不影响主流应用价值。
更重要的是,它的底层逻辑是“用广度覆盖弥补深度不足”:只需要低深度全基因组测序,就能捕捉到足够的碎片特征,成本远低于深度测序的突变检测。这意味着它有大规模推广的可能——未来或许能像血常规一样,成为常规乳腺癌筛查的补充手段。
不过现在它还需要通过前瞻性研究验证:它能不能真正改变临床决策?比如那些被预测为淋巴结阴性的患者,真的可以安全地跳过清扫手术吗?这才是衡量一项技术临床价值的核心标准。
当我们还在为影像漏诊、穿刺痛苦发愁时,科学家已经从血液里的基因碎片里,找到了更早期、更全面的癌症信号。这不是对传统筛查的替代,而是一种补充——就像给医生多开了一双能看见分子层面变化的“眼睛”。
碎片里藏着癌症的秘密,也藏着更早的希望。未来的癌症筛查,或许不再是“等肿块长出来再发现”,而是在细胞刚刚出现异常时,就从血液里读出预警。