对抗知识焦虑,从看懂这条开始
App 下载
精子里的环形DNA少了,可能是不育的信号
中山大学附属第七医院|精子活力|特发性弱精子症|染色体外环状DNA|生殖围产医学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
中山大学附属第七医院|精子活力|特发性弱精子症|染色体外环状DNA|生殖围产医学|医学健康
一对结婚三年的夫妻,在排除了女方生育问题、做完了所有男科常规检查后,依然找不到怀不上孩子的原因——丈夫的精子看起来浓度正常、形态也没大问题,就是前向运动的精子不足32%,属于医生口中的「特发性弱精子症」。这类不明原因的男性不育,占了临床病例的近三成,像个找不到入口的迷宫。
直到中山大学附属第七医院的研究团队,在这些「不听话」的精子里,发现了一个隐秘的变化:那些能在染色体外自由环转的DNA分子——也就是染色体外环状DNA(eccDNA),含量比健康精子少了一大截。这不仅是一个新发现的分子特征,更牵出了藏在精子活力低下背后的核心问题。
你可以把细胞核里的线性染色体想象成一卷卷装订好的书,而eccDNA就是从书里掉出来、被折成圆环的纸页——它游离在染色体之外,却带着完整的遗传片段,小到几十对碱基,大到数百万对碱基都有。
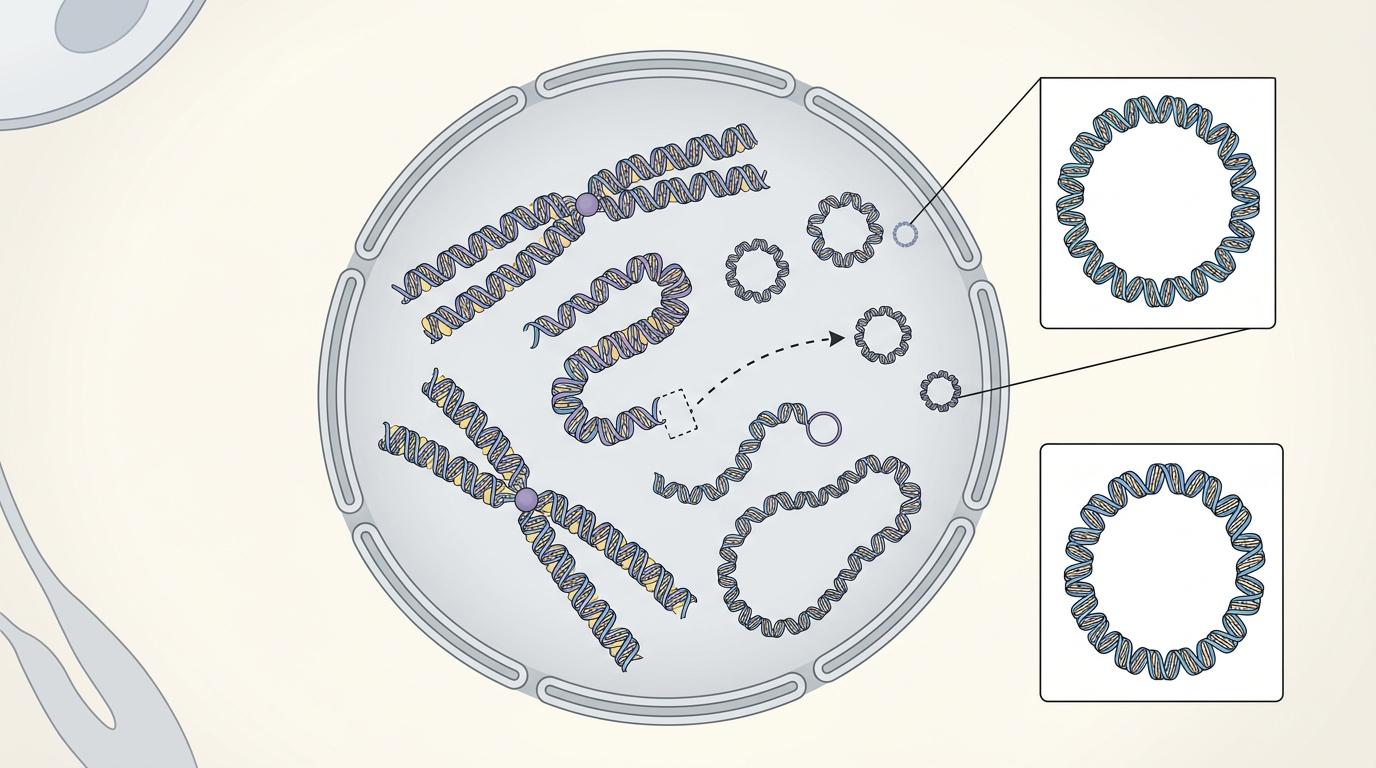
这种环形DNA不是什么罕见物,1965年就在公猪精子里被首次发现,后来证实它普遍存在于动植物甚至人类的各种细胞中。但它的功能一直像个谜:有时会帮着扩增基因、调控表达,有时又会参与维持基因组稳定,甚至能在细胞间传递信号。
在人类精子里,eccDNA的来源很有特点:多数是被核小体保护的DNA片段,大小刚好是180碱基对的倍数——就像每一页纸都刚好卡在书的装订线位置,脱落之后自然卷成了环。研究人员用高通量测序技术统计发现,健康男性的成熟精子里,这类环形DNA的数量远高于发育中的精母细胞。
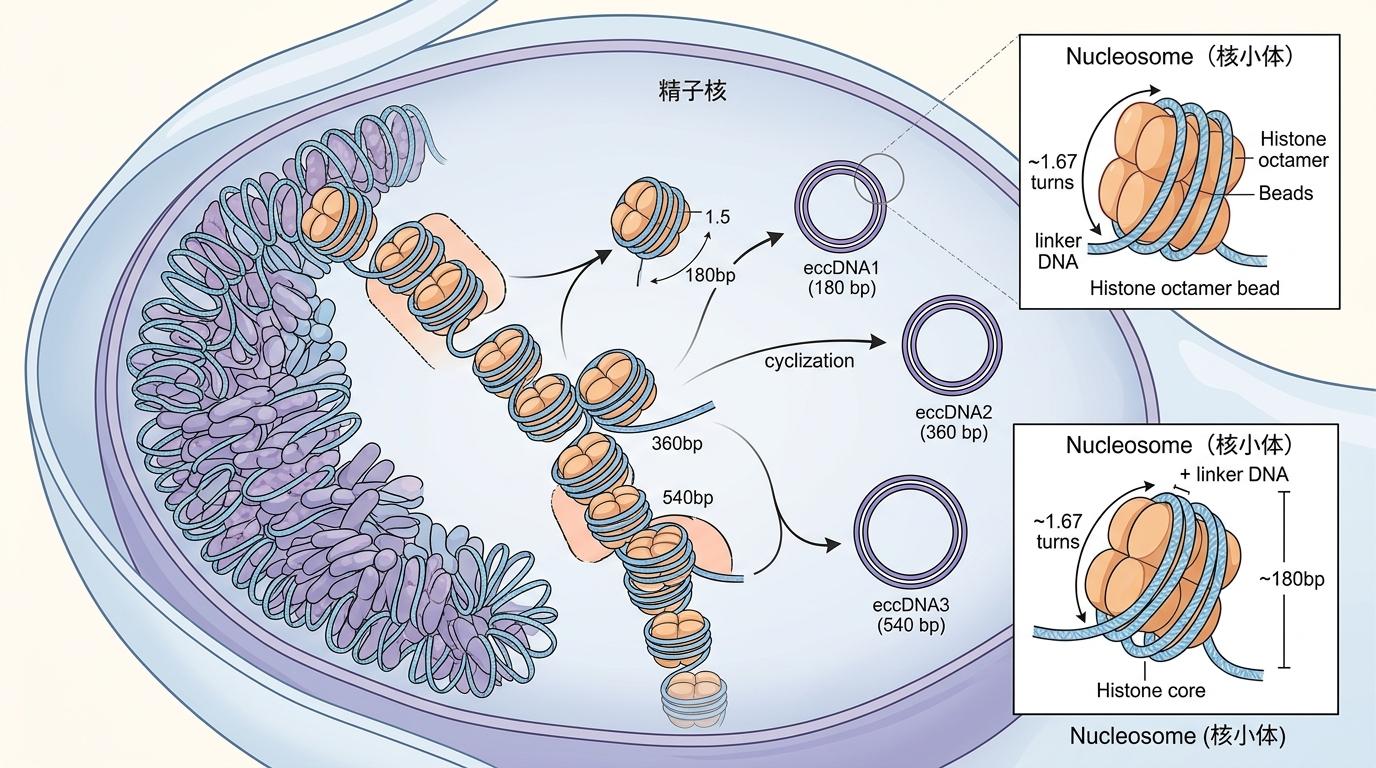
研究团队找来了31名特发性弱精子症患者和31名健康志愿者,对比他们精子里的eccDNA含量,结果一目了然:患者的eccDNA总量显著降低,而且精子前向运动能力越差,eccDNA就越少。
更关键的关联藏在DNA修复里。
你可以把精子的DNA修复系统想象成一个车间,专门修补精子生成过程中出现的DNA断裂。而APLF蛋白就是这个车间里的核心调度员——它既能帮着把断裂的DNA末端接起来,又能负责修复后的染色质重组,让DNA恢复稳定的结构。
研究人员在患者的精子里发现,APLF蛋白的表达量明显降低;当他们在细胞模型里敲除APLF基因后,全基因组的eccDNA生成量直接大幅减少。这就像车间的调度员缺位,不仅修补DNA的效率变慢,连那些本该形成环形的DNA碎片也没法正常环化了。
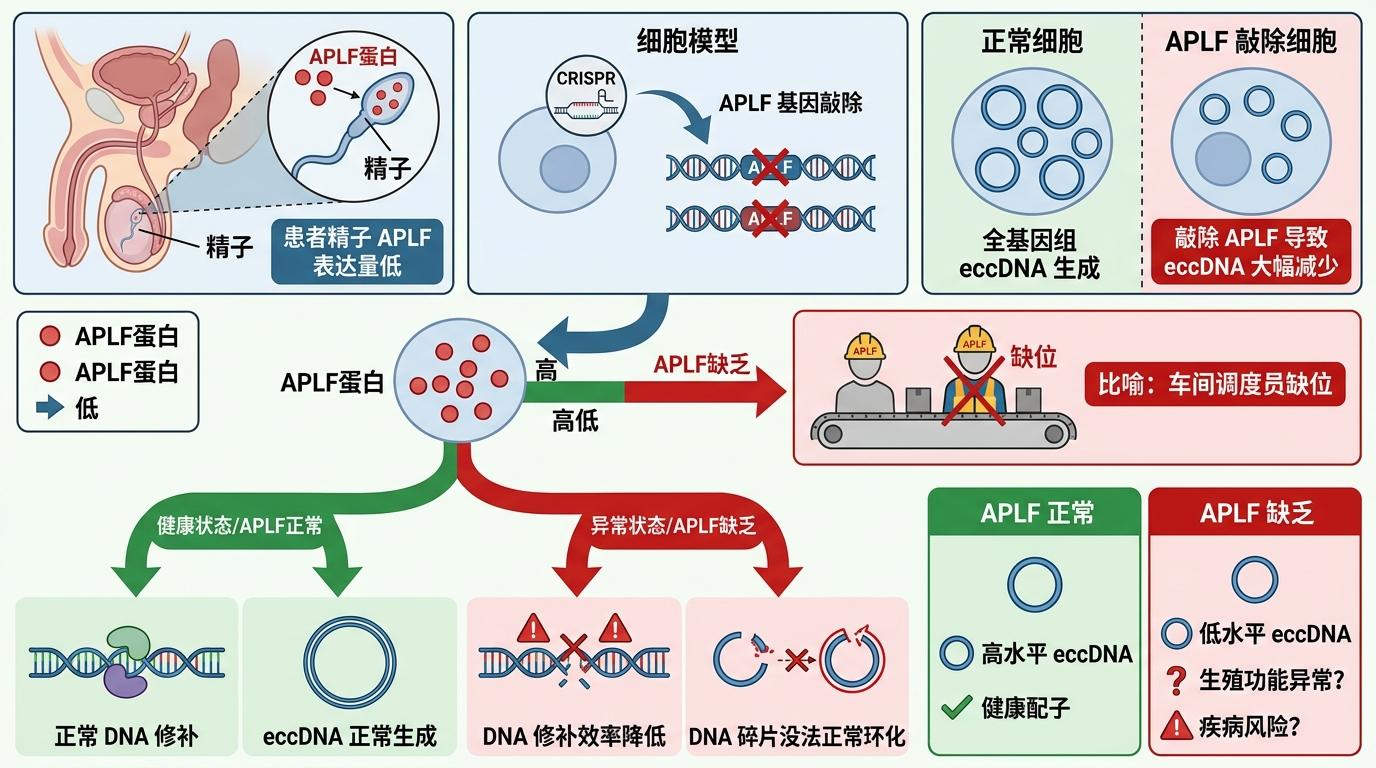
直接的连锁反应是:DNA损伤开始累积,精子的基因组稳定性被破坏,最终导致精子的运动能力下降。这也解释了为什么特发性弱精子症患者的精子DNA损伤水平普遍更高——修复系统的漏洞,才是问题的根源。
这个发现给特发性弱精子症的诊治撕开了一个新口子:未来或许可以通过检测精子里的eccDNA含量,或者APLF蛋白的表达水平,更早地发现那些常规检查找不到原因的不育病例。甚至可以针对DNA修复通路开发药物,补上精子的修复漏洞。
但现在还远没到临床应用的阶段。
首先,eccDNA的检测还依赖复杂的高通量测序技术,成本高、流程长,没法像常规精液检查那样快速普及。其次,研究只证实了eccDNA减少和弱精子症的相关性,还没完全搞清楚它的具体功能——它到底是DNA修复的「副产品」,还是真的参与调控精子活力的「功能分子」,还需要更多实验验证。
更现实的是,特发性弱精子症的病因本来就复杂,氧化应激、线粒体功能障碍、表观遗传异常都可能参与其中,eccDNA只是其中的一个线索,没法单独解释所有病例。
当我们谈论男性不育时,习惯把目光放在精子的「数量」和「形态」上,却常常忽略了这些微小分子里藏着的秘密。eccDNA的发现,让我们意识到精子的健康远不止肉眼看到的那些指标,更关乎它内部的DNA修复能力和基因组稳定性。
「修复力,才是精子的隐形活力。」这句话或许能概括这个研究的核心——那些看起来「正常」的精子,可能早已在分子层面失去了稳定遗传的能力。而这个新发现的线索,终有一天会帮更多家庭找到通往生育的入口。