
8 天前

8 天前
当你卷起袖子打疫苗加强针时,很少会在意是打在左臂还是右臂——毕竟疫苗都是一样的。但2025年悉尼加文医学研究所的一项发现,彻底打破了这个常识:在接种过第一针的同一手臂打加强针,体内产生广谱中和抗体的速度快了一倍,针对新冠变异株的B细胞克隆扩增也更显著。
这不是随机误差,而是免疫系统藏了几十年的秘密:疫苗诱导的免疫记忆,从来不是均匀分布在体内的。那些藏在初次接种部位引流淋巴结里的免疫细胞,正以我们从未察觉的方式,决定着疫苗的真实效力。为什么同一手臂会有这么大的差别?答案藏在一种不起眼的巨噬细胞里。
要理解这个发现,得先搞懂两个关键角色:记忆B细胞和引流淋巴结。
记忆B细胞是免疫系统的「档案员」——初次接种疫苗后,它们会记住病原体的特征,等下次遇到相同威胁时,要么快速变身浆细胞分泌抗体,要么重新进入生发中心「进修」,优化出能对付变异株的高亲和力抗体。而引流淋巴结,就是疫苗接种后第一批免疫细胞聚集作战的「前线指挥部」,它会把接种部位的抗原和免疫细胞都收拢过来。
过去科学家认为,记忆B细胞是在全身循环的,不管哪只手臂打加强针,唤醒的都是同一批细胞。但加文研究所的小鼠实验推翻了这个假设:初次接种部位的引流淋巴结里,藏着一批「驻守」的记忆B细胞,它们待在淋巴结的皮下腔位点,比全身循环的记忆B细胞更活跃——不仅能产生更强的回忆反应,重新进入生发中心优化抗体的概率也高出3倍。
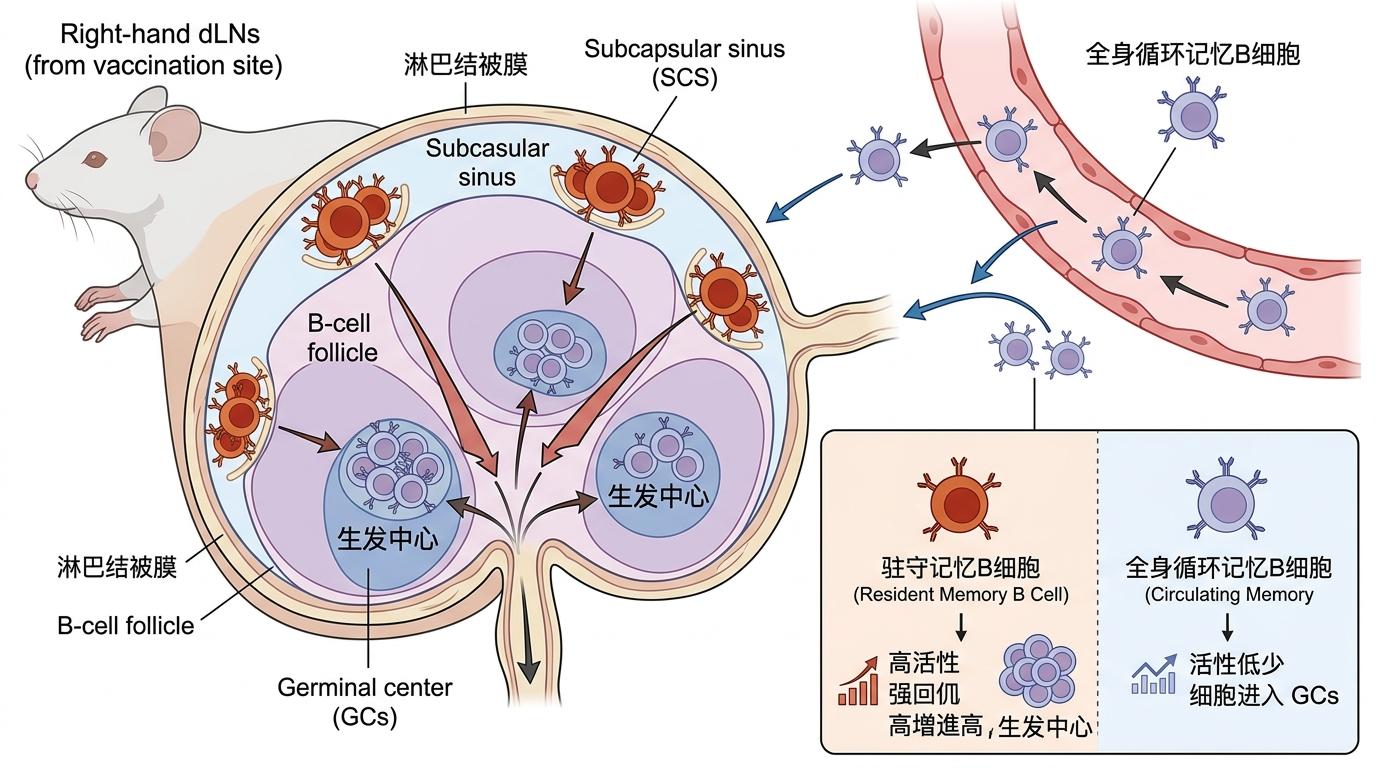
这些「驻守」的记忆B细胞,就像驻扎在前线的预备役,只要同一部位再收到抗原信号,就能立刻投入战斗。
为什么这些「驻守」的记忆B细胞反应更强烈?答案是CD169+皮下窦巨噬细胞(SSMs)——一种定居在淋巴结皮下窦的特殊巨噬细胞。
你可以把SSMs想象成淋巴结门口的「哨兵」,它们的任务不是直接消灭病原体,而是精准捕获抗原,然后把信号传递给记忆B细胞。加文研究所的实验显示,正是这些SSMs在初次接种后被激活,给引流淋巴结里的记忆B细胞「留了位置」:它们会分泌特定的细胞因子,还会通过微囊泡和滤泡树突状细胞协作,维持一个适合记忆B细胞停留和活化的微环境。
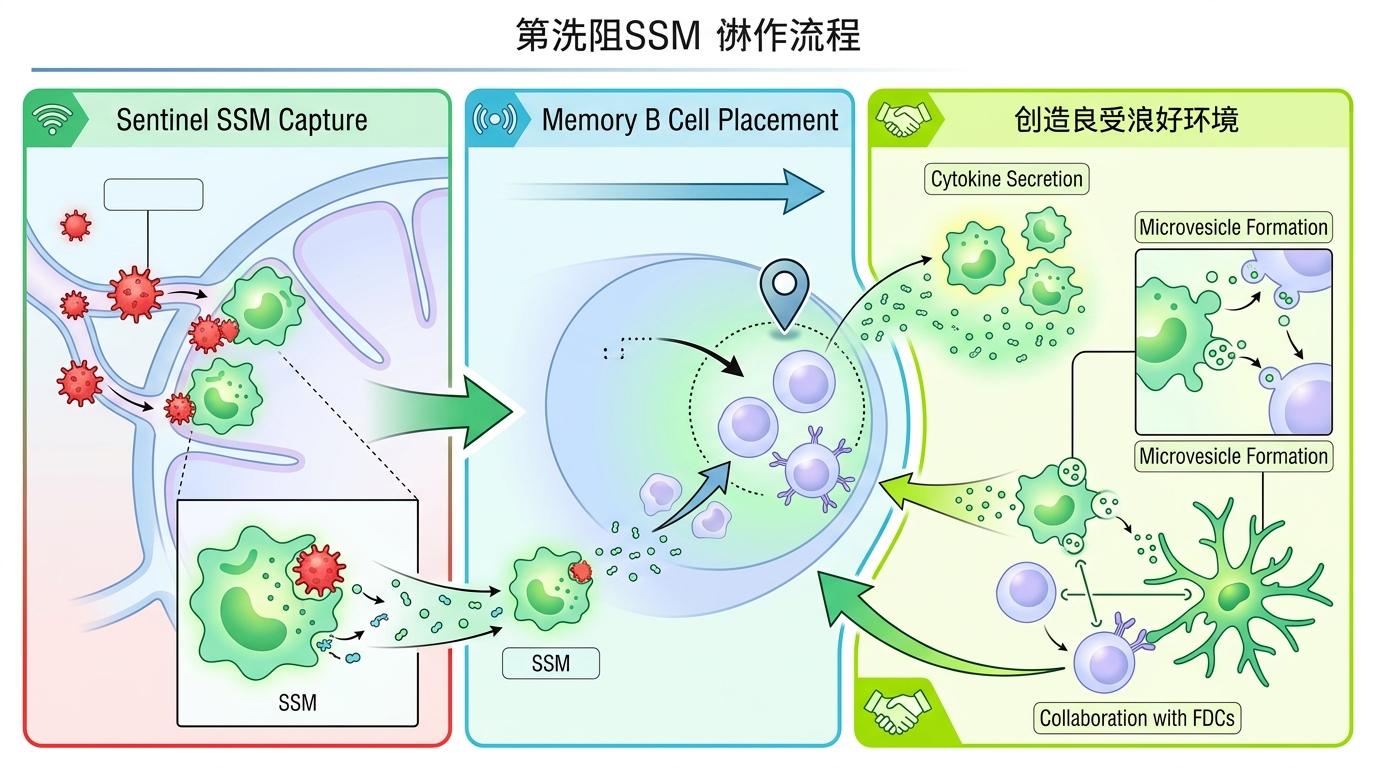
当同一手臂再次接种疫苗时,预先激活的SSMs能更快地把抗原呈递给附近的记忆B细胞,直接推动它们进入生发中心。而如果换了另一只手臂,新的引流淋巴结里的SSMs还没「热身」,记忆B细胞只能靠全身循环过来,反应自然慢半拍。
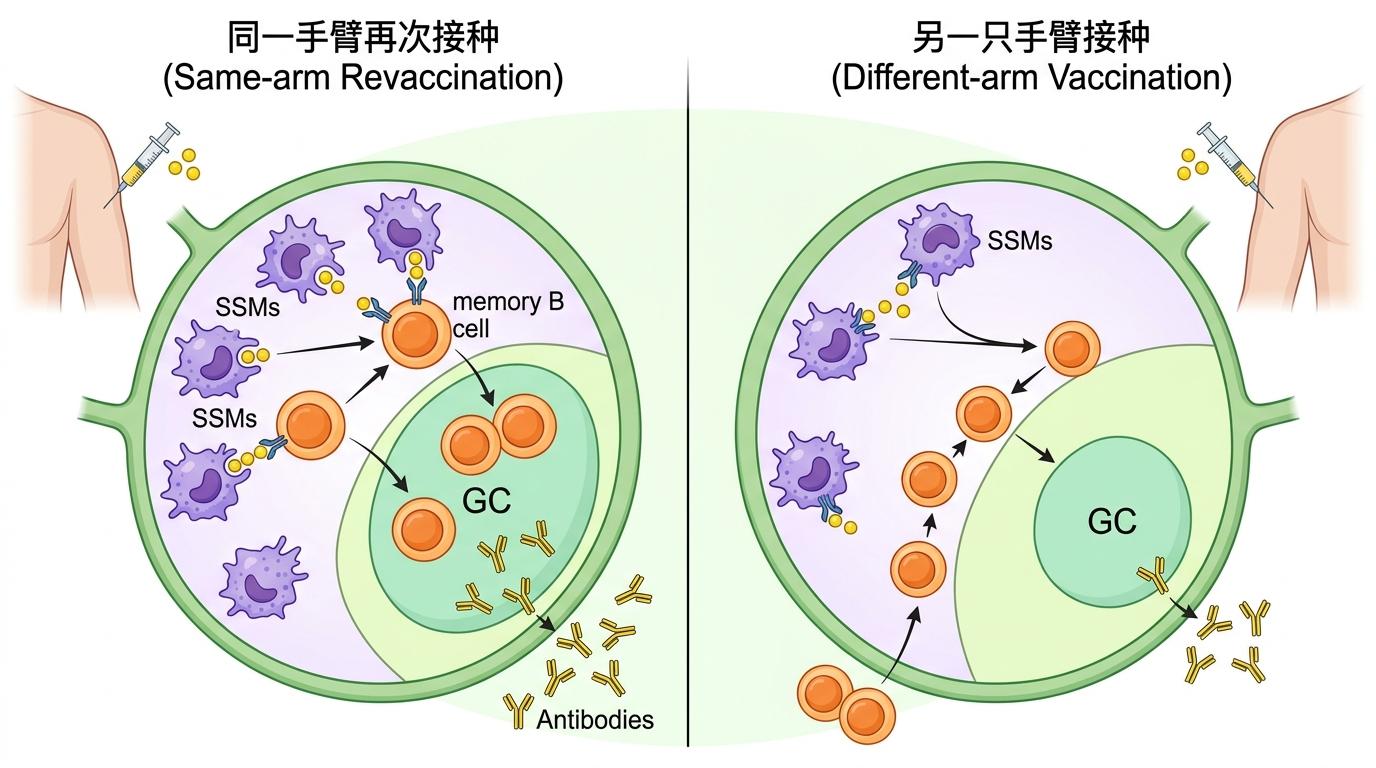
更关键的是,这种调控是「位置依赖」的——只有初次接种部位的引流淋巴结里的SSMs才有这种预激活状态,其他部位的巨噬细胞完全不具备这个能力。
不过这项研究也有局限:目前的证据都来自小鼠模型和新冠疫苗的人体试验,对于其他病原体的疫苗是否有同样效果,还需要更多验证。而且我们还不知道,这种预激活的SSMs能维持多久,是否会随着时间推移逐渐失去活性。
这个发现不止是实验室里的基础研究,它已经能直接改变我们接种疫苗的策略。
加文研究所的人体试验显示,同一手臂接种新冠疫苗加强针的受试者,在接种后第一周,广谱中和抗体的水平就比另一手臂接种的人高了40%,生发中心的参与度也提升了35%——这意味着在疫情爆发时,他们能更快获得保护。
更重要的是,这个发现给疫苗设计打开了新的思路:过去我们只关注疫苗里的抗原和佐剂,现在才意识到,「在哪里激活免疫细胞」和「激活什么细胞」同样重要。未来的疫苗或许可以专门靶向CD169+巨噬细胞,提前给引流淋巴结「预热」,让记忆B细胞能更快、更强地响应;甚至可以设计能在引流淋巴结里缓慢释放抗原的疫苗,延长SSMs的激活时间,让免疫记忆维持更久。
不过也有人担心,反复在同一手臂接种会不会导致局部免疫耐受?目前的试验还没发现这个问题,但长期的影响还需要更多数据来验证。
我们总以为免疫系统是一个「一视同仁」的整体,却忘了它其实是一个高度精准的「空间系统」——每一种细胞都有自己的岗位,每一个部位都有自己的功能。那些藏在淋巴结里的巨噬细胞和记忆B细胞,就像一群默契的战友,在我们看不见的地方,决定着疫苗的效力。
免疫记忆的关键,从来都不是数量,而是位置。
当下次再打疫苗加强针时,或许你会下意识地选择第一次接种的那只手臂——这不是迷信,而是我们终于读懂了免疫系统的「暗语」。
点击充电,成为大圆镜下一个视频选题!