对抗知识焦虑,从看懂这条开始
App 下载
T细胞耗竭元凶找到,竟是线粒体的求救信号
瑞士洛桑大学|肿瘤微环境|线粒体信号|T细胞耗竭|CAR-T细胞|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
瑞士洛桑大学|肿瘤微环境|线粒体信号|T细胞耗竭|CAR-T细胞|肿瘤学|医学健康
当医生给一位晚期白血病患者注入CAR-T细胞时,所有人都在期待那些“活的药物”能像精准导弹一样清除癌细胞——毕竟这种疗法在血液肿瘤里创造过80%以上的完全缓解率。但半年后,复查报告上的复发信号让整个团队沉默了。不是CAR-T不够强,而是这些英勇的T细胞在肿瘤微环境里“叛变”了:它们渐渐失去杀敌能力,最终彻底瘫软。全球每年有数十万患者因T细胞耗竭错失治愈机会,这道免疫治疗的天花板,最近被瑞士洛桑大学的研究团队撬开了一道缝。
你可以把T细胞想象成一台时刻待命的战斗机,线粒体就是它的发动机。当T细胞钻进肿瘤微环境这个充满毒素和缺氧的“烂泥塘”,发动机很快就会故障——专业说法叫线粒体去极化。过去我们以为,T细胞耗竭只是“油烧完了”,但这次的发现完全推翻了这个假设。
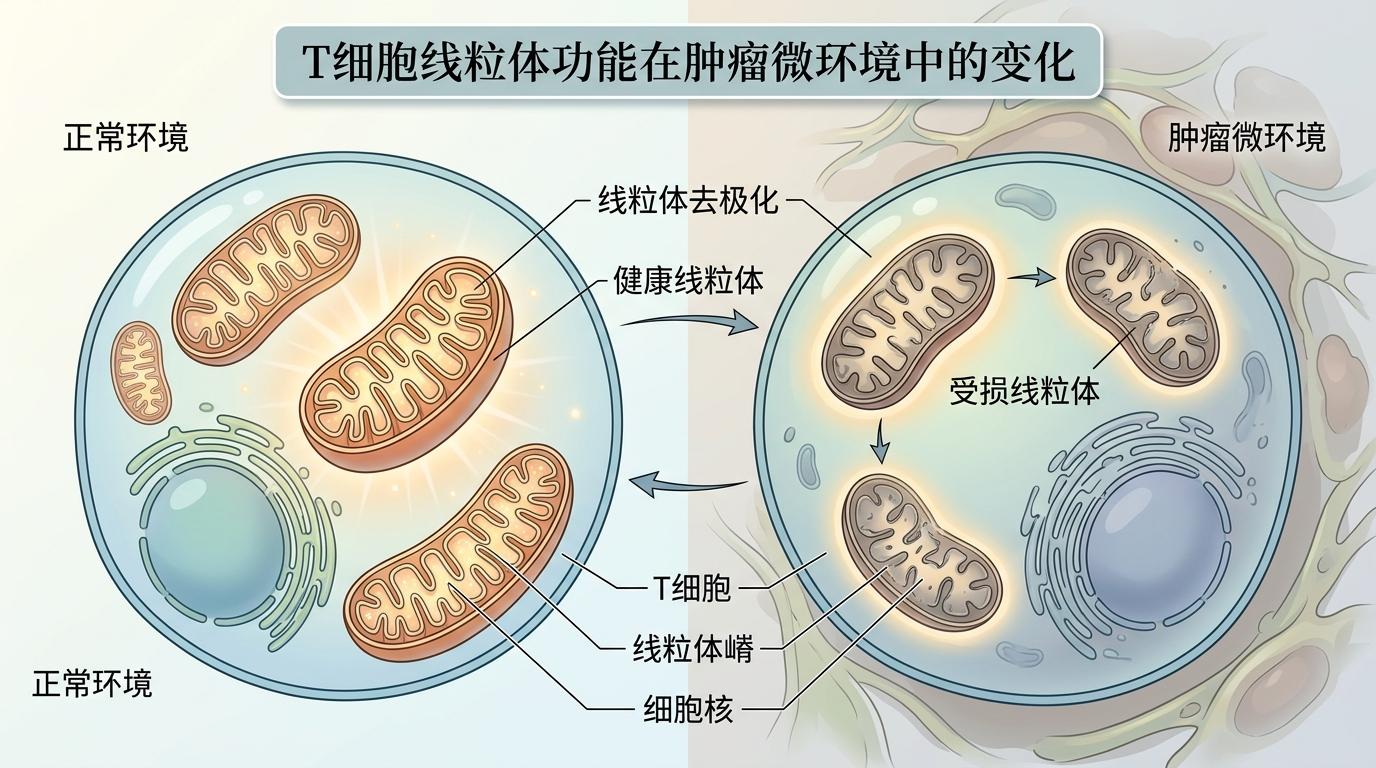
研究人员在显微镜下看到了完整的“叛变链条”:线粒体故障后,细胞会启动蛋白酶体这个“垃圾处理站”,分解受损的线粒体蛋白。这本是细胞的自救机制,没想到却捅了娄子——清理过程中,含血红素的蛋白质被拆碎,释放出大量游离的调节性血红素。
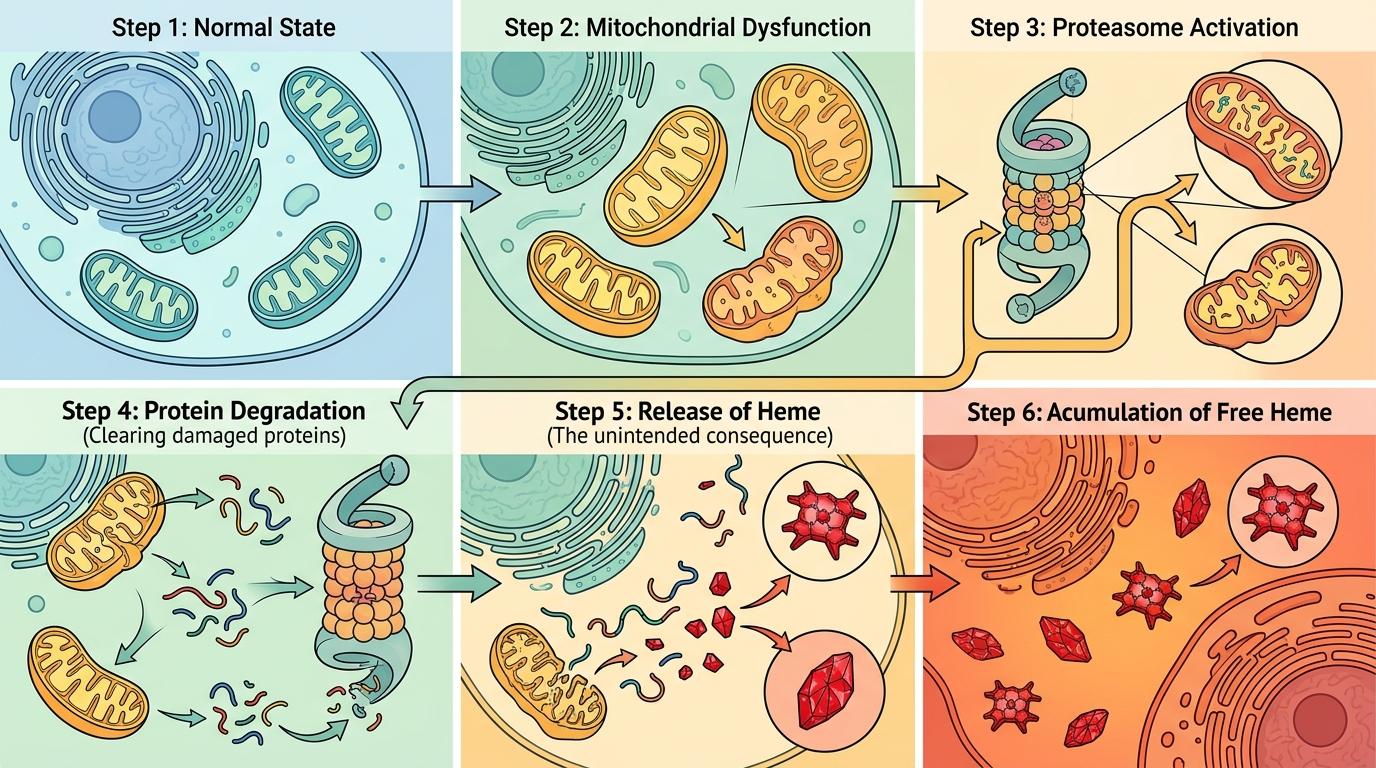
这些血红素不是废物,而是伪装成信使的内奸。它们溜进细胞核,精准找到维持T细胞“战斗力”的关键转录因子BACH2,把它彻底破坏。而BACH2原本是另一个转录因子BLIMP1的“刹车”,刹车失灵后,BLIMP1开始疯狂工作,直接把T细胞推进了“终末耗竭”的死胡同——它们不再增殖,不再产生杀敌的细胞因子,彻底变成了战场上的逃兵。
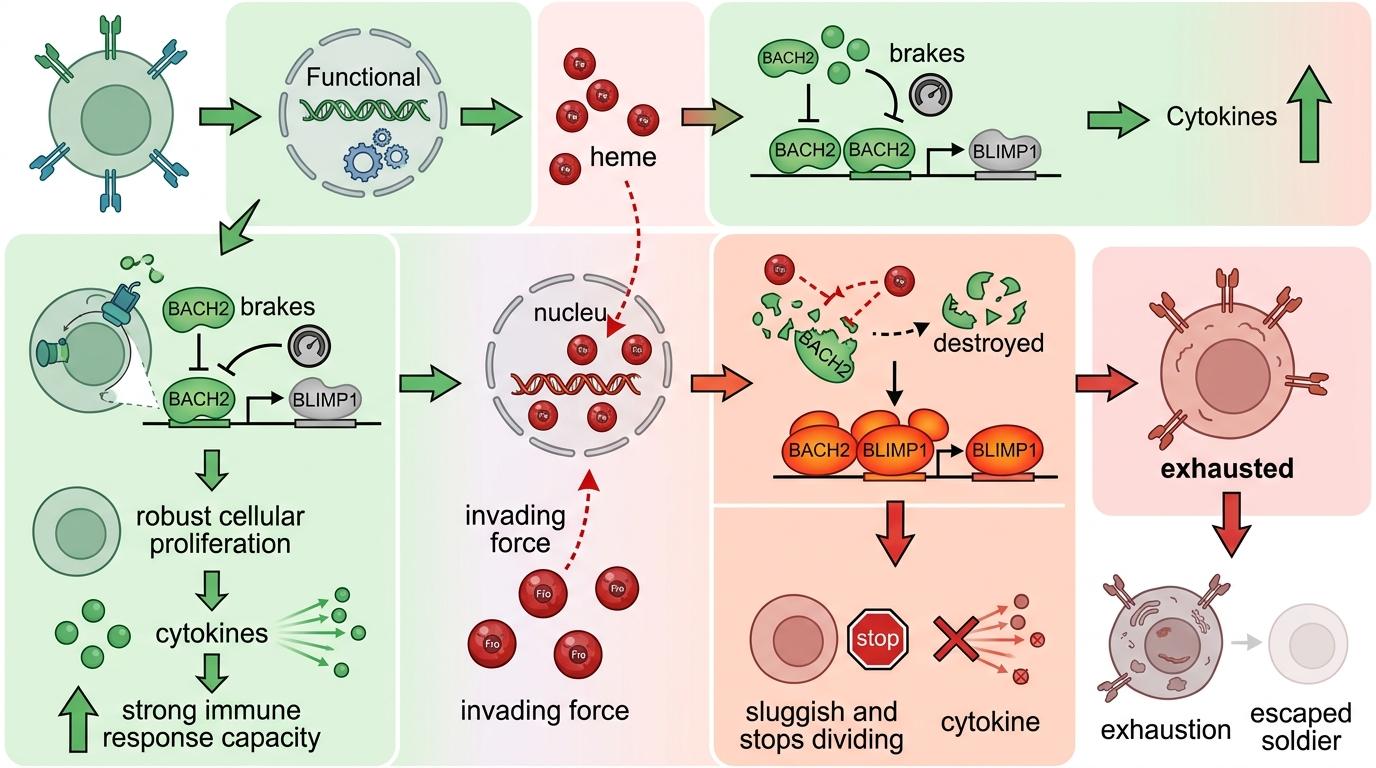
更重要的是,研究团队不仅找到了病因,还找到了精准干预的钥匙。他们在B细胞急性淋巴细胞白血病患者的样本中发现了一个明确的规律:CAR-T细胞里的蛋白酶体活性越高,患者的治疗效果就越差。这意味着,蛋白酶体活性可以直接作为预测CAR-T疗效的生物标志物——抽一管血,就能提前知道治疗胜算。
更让人振奋的是,干预方法简单到惊人。在CAR-T细胞的制备过程中,只要短暂加入低剂量的硼替佐米——一种已经获批上市的蛋白酶体抑制剂,就能切断血红素的释放通路。实验显示,经过处理的CAR-T细胞,耗竭相关基因的表达显著降低,反而朝着“记忆样状态”重编程:它们就像记住了敌人特征的老兵,能在体内长期存活,一旦发现肿瘤复发就立刻重启杀敌模式。
当然,这并不意味着我们已经彻底解决了T细胞耗竭问题。硼替佐米的最佳剂量、处理时长,对不同T细胞亚群的影响,还需要大量临床试验验证。而且实体肿瘤的微环境比血液肿瘤复杂得多,这条通路是否能成为实体瘤免疫治疗的突破口,还有待探索。
过去我们对T细胞耗竭的理解,停留在“慢性抗原刺激导致的功能衰退”,但这次的研究重新定义了它的本质:这不是简单的“累垮了”,而是细胞代谢信号通路的彻底紊乱——线粒体的自救信号,被癌细胞利用成了瓦解T细胞的武器。
这背后是免疫代谢领域的认知升级:我们不再把免疫细胞的代谢状态当成“后勤保障”,而是把它当成决定免疫细胞命运的“指挥中心”。这条蛋白酶体-血红素信号轴,连接了线粒体功能、蛋白质降解和转录调控三个核心环节,为免疫治疗打开了全新的干预维度。
更值得关注的是,这一发现的意义不止于癌症治疗。血红素作为信号分子的角色,可能在自身免疫病、慢性感染等多种免疫相关疾病中发挥作用,未来或许能为更多患者带来新的治疗希望。
当我们把T细胞当成对抗癌症的“士兵”时,往往只关注它们的武器够不够锋利,却忽略了它们的“后勤系统”可能早已被敌人渗透。这次的研究就像找到了敌军的“卧底联络站”,让我们第一次有机会从源头阻断T细胞的叛变。
代谢信号决定免疫命运,这不仅是一个科学结论,更是对未来免疫治疗的全新指引。或许在不远的将来,我们不再需要依赖“超级T细胞”,只要轻轻拨动细胞代谢的开关,就能让每一个T细胞都成为永不疲倦的抗癌战士。