对抗知识焦虑,从看懂这条开始
App 下载
肾癌耐药性被破解?PRKAB2蛋白成逆转战局新靶点
耐药机制|酪氨酸激酶抑制剂|舒尼替尼|PRKAB2蛋白|肾细胞癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
耐药机制|酪氨酸激酶抑制剂|舒尼替尼|PRKAB2蛋白|肾细胞癌|肿瘤学|医学健康
肾细胞癌(RCC),一种被称为“沉默杀手”的恶性肿瘤,正以惊人的速度侵袭全球。据统计,2020年全球新增病例超过43万,其发病率在过去二十年里几乎翻了一番。在早期,它悄无声息,超过七成的患者是在常规体检中偶然发现。然而,一旦肿瘤扩散或转移,战局便急转直下。
对于晚期肾癌患者,靶向治疗和免疫疗法是主要的武器。舒尼替尼(Sunitinib)等酪氨酸激酶抑制剂(TKIs)曾一度带来希望,它们通过切断肿瘤的血液供应来“饿死”癌细胞。然而,癌细胞的狡猾超乎想象。它们总能找到对策,产生耐药性,让这些曾经的“特效药”失效。一旦耐药发生,患者的五年生存率便骤降至不足10%。这道由耐药性筑起的高墙,是横亘在医生和患者面前最残酷的现实。
就在2026年1月底,一道惊雷划破了肾癌治疗领域的沉寂。华中科技大学的章小平、刘磊和Yuenan Liu团队在国际权威期刊《Autophagy》上发表了一项突破性研究。他们通过全基因组CRISPR筛选这一强大的基因编辑技术,从浩如烟海的基因中,精准锁定了一个关键角色——PRKAB2。
研究明确指出,PRKAB2是肾细胞癌中一个至关重要的肿瘤抑制因子。在临床数据中,PRKAB2蛋白水平较低的患者,往往预后更差,肿瘤也更具侵袭性。更令人振奋的是,当研究人员在耐药的肾癌细胞中重新提升PRKAB2的水平时,这些顽固的癌细胞竟然奇迹般地恢复了对舒尼替尼等靶向药物的敏感性。这一发现,无疑为攻克肾癌耐药性打开了一扇全新的大门。
要理解PRKAB2如何扭转乾坤,我们必须潜入细胞内部,探寻癌细胞耐药的根源。癌细胞是一个微型的能量消耗巨兽,其生存和扩张离不开细胞的“发电厂”——线粒体。肾癌细胞尤其依赖线粒体驱动的脂质代谢来获取能量。
然而,高强度的能量生产会使线粒体受损。正常细胞会通过一种名为“线粒体自噬”(Mitophagy)的机制,像清理废旧零件一样,精准地清除掉这些受损的线粒体,维持内部环境的稳定。这本是一种保护机制,但癌细胞却将其“黑化”,利用它来不断更新自己的“发电厂”,从而在靶向药物带来的巨大代谢压力下得以喘息和存活,并最终演化出耐药性。可以说,线粒体自噬成为了癌细胞抵抗治疗的“续命”法宝。
华中科技大学团队的精妙之处在于,他们不仅找到了PRKAB2这个“总开关”,还清晰地描绘出它如何通过两条截然不同的路径,为失控的线粒体自噬踩下“双重刹车”。
想象一下,启动线粒体自噬需要一个经典的“信号二人组”——PINK1和Parkin。当线粒体受损时,PINK1会发出信号,招募Parkin前来给受损线粒体贴上“待回收”的标签。
PRKAB2的第一道刹车,是**“釜底抽薪”**:
PRKAB2的第二道刹车,则是**“断其粮草”**:
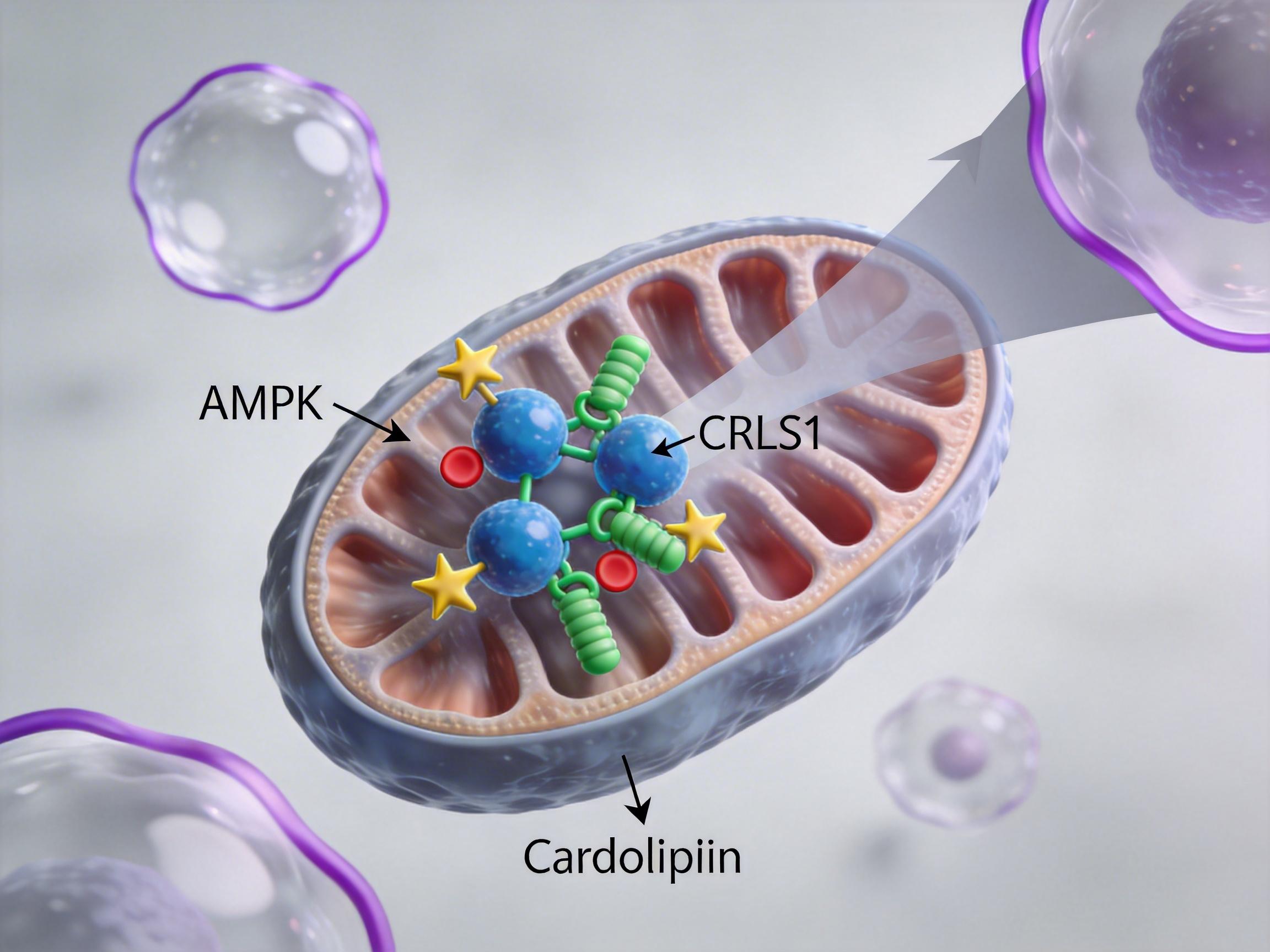
通过这两种机制的协同作用,PRKAB2有效地关闭了癌细胞赖以生存的线粒体自噬通道,使其能量代谢系统陷入混乱,最终在靶向药物的攻击下土崩瓦解。
这项研究的意义远不止于一篇高水平的学术论文。它为肾癌治疗,特别是耐药性肾癌的治疗,提供了全新的分子靶点和极具潜力的策略。
目前的肾癌治疗已经进入靶向与免疫联合的时代,如“阿昔替尼+特瑞普利单抗”等方案显著提高了患者的生存期。然而,耐药问题依然是悬顶之剑。PRKAB2的发现,意味着未来可能开发出专门激活PRKAB2或模拟其功能的药物。这类药物可以与现有的TKI靶向药联合使用,形成“增敏剂+攻击剂”的组合拳,有望:
从揭示一个沉默杀手的生存伎俩,到发现一个能够破解这一伎俩的关键蛋白,再到阐明其精密的双重调控机制,PRKAB2的故事完美诠释了基础科学研究如何为临床困境带来曙光。尽管从实验室的发现到真正应用于患者仍有很长的路要走,但这一突破无疑为无数深陷耐药泥潭的肾癌患者和家庭,点亮了一盏充满希望的灯塔。在这场与癌症的漫长博弈中,每一次对生命底层逻辑的深刻洞察,都在为我们赢得最终的胜利增添关键的砝码。