对抗知识焦虑,从看懂这条开始
App 下载
脑震荡与痴呆症的隐秘联系:哈佛研究揭示惊人突变
拳击手|基因突变|脑震荡|Christopher A. Walsh|哈佛医学院|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
拳击手|基因突变|脑震荡|Christopher A. Walsh|哈佛医学院|神经退行性疾病|医学健康
想象一位拳击手,生涯的荣光早已褪去,擂台上的呐喊也已远去。然而,另一场更漫长、更无声的战斗却在他脑海深处悄然打响。记忆开始模糊,情绪变得暴躁,曾经精准的判断力日渐迟钝。多年来,我们将这悲剧归咎于一次次猛烈的撞击——那些作用于大脑的纯粹物理力量。但如果,这只是故事的一半呢?如果真正的“幽灵”并非撞击本身,而是在撞击之后,于神经元核心深处悄然上演的一场基因叛变?
2025年10月,一扇通往理解这一谜团的新窗户被猛然推开。哈佛医学院的Christopher A. Walsh团队在顶尖期刊《Science》上发表了一项颠覆性的研究。他们利用前沿的单细胞全基因组测序技术,以前所未有的精度“阅读”了15名已故慢性创spang性脑病(CTE)患者的单个神经元基因组。
结论令人震惊:CTE患者的神经元中,积累了大量的体细胞基因突变——这些是在生命过程中新出现的基因“拼写错误”。更关键的是,这些突变的模式和特征,竟然与阿尔茨海默病(AD)患者神经元中的突变模式高度相似。这就像在两个看似无关的犯罪现场,发现了来自同一个罪犯的、独一无二的指纹。
这项研究还有一个至关重要的发现:研究团队同样分析了4名同样经历过反复头部撞击(RHI)但并未患上CTE的个体。在他们的神经元中,并未发现这种异常的突变积累。这一对比有力地证明,反复的物理撞击本身,并不足以触发这场基因灾难。 CTE的发病,背后隐藏着比物理损伤更深层的生物学机制。
深入分析这些基因突变,科学家们识别出两种截然不同的“作案手法”:
氧化应激的灼伤:第一种是大量的单核苷酸变异(SNVs),其特征与细胞“生锈”——即氧化应激——造成的损伤高度吻合。当细胞因炎症或其他压力不堪重负时,会产生大量有害的活性氧分子,它们像微小的火焰,灼烧并篡改着DNA的编码。
转录过程的“影印事故”:第二种是大量的短片段插入和缺失(Indels),其模式指向了一种名为**拓扑异构酶I(TOP1)**的酶的活性异常。这种酶在基因转录(将DNA信息“复印”为RNA)时负责解开DNA的超螺旋结构。当它工作失常,就如同复印机卡纸或漏印,导致基因序列出现删减或增加,造成严重的功能紊乱。
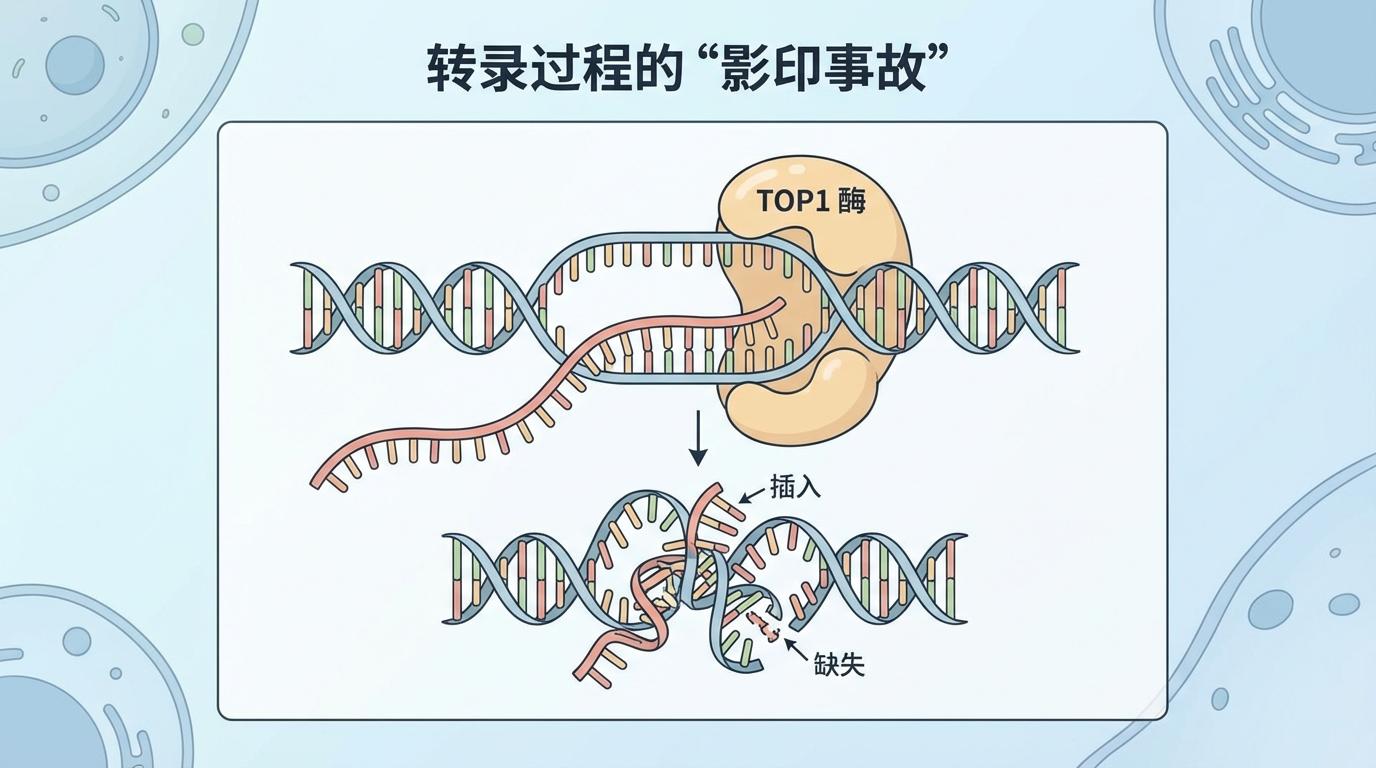
在部分CTE和AD患者的神经元中,这种短缺失突变的数量异常之高,相当于正常人大脑在一百多年自然衰老过程中才会积累的损伤量。这无疑是一场加速的、灾难性的衰老。
长期以来,神经退行性疾病的研究一直聚焦于异常蛋白的聚集。在CTE和AD的大脑中,都存在着Tau蛋白的异常磷酸化和聚集,它们像垃圾一样堆积在神经元内部,形成神经纤维缠结,阻碍细胞正常运作。尽管两者中Tau蛋白的聚集形态和分布区域略有不同,但其核心病理角色是共通的。
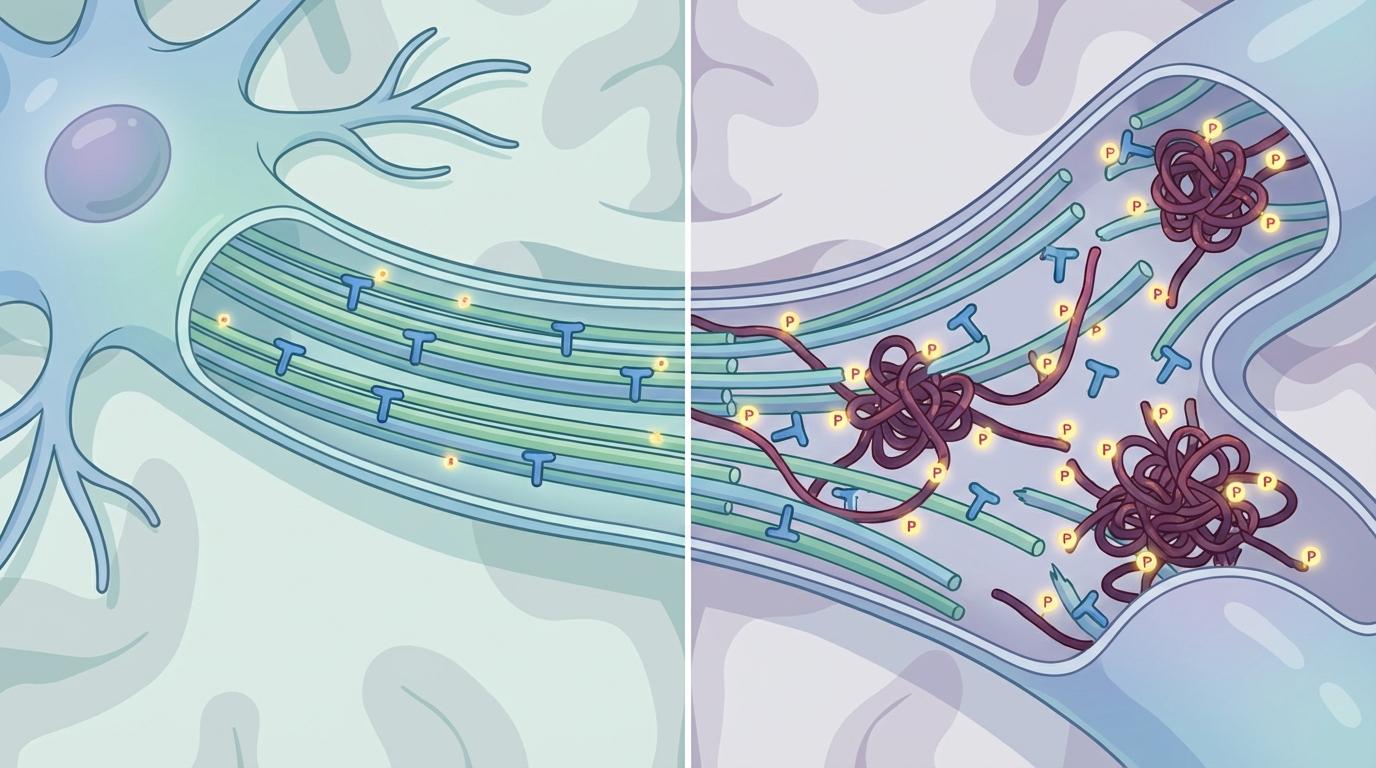
然而,故事并未就此结束。研究发现,在高达85%的CTE病例和相当一部分AD病例中,还存在另一种名为TDP-43的蛋白的异常聚集。正常情况下,TDP-43在细胞核内辛勤工作,负责RNA的加工处理。一旦它错误地跑到细胞质中并发生聚集,就会引发一系列连锁反应,导致神经元功能障碍甚至死亡。
Tau和TDP-43,这两种关键的病理蛋白,如同在即将崩塌的舞台上跳着一曲死亡之舞。它们的存在不仅加剧了细胞的压力,更可能与基因组的不稳定状态相互作用,共同将神经元推向毁灭的深渊。
现在,我们可以将所有线索串联起来。反复的头部撞击,如同向平静的湖面投入一颗石子,激起了慢性神经炎症的涟漪。大脑中的免疫细胞——小胶质细胞被持续激活,释放出大量炎症因子。这个本意是保护和修复的反应,一旦失控,就演变成一场持久的“内战”。
这场“内战”正是基因突变的催化剂。持续的炎症环境制造了大量的氧化应激,直接导致了前文所述的DNA“灼伤”。同时,受损的DNA片段本身又会像警报一样,进一步刺激免疫系统,加剧炎症反应。这就形成了一个致命的恶性循环:炎症导致基因组损伤,基因组损伤又反过来加剧炎症。
在这个循环中,物理撞击是“扳机”,而失控的炎症和随之而来的基因组不稳定性,才是那颗真正致命的“子弹”。这也解释了为何并非所有经历头部撞击的人都会患上CTE——个体的遗传背景、免疫反应强度等内在因素,决定了他们是否会陷入这个毁灭性的循环。
这项里程碑式的发现,彻底重塑了我们对CTE乃至整个神经退行性疾病谱系的认知。它告诉我们,CTE并非一个孤立的、由纯粹机械损伤导致的疾病,而是与AD等“经典”神经退行性疾病共享着深刻的分子根源——基因组完整性的丧失。
这一洞察为我们带来了前所未有的希望:
新的诊断靶点:未来,我们或许可以通过检测血液或脑脊液中与特定DNA损伤模式相关的生物标志物,来早期识别高风险人群,实现从死后确诊到生前预警的跨越。
统一的治疗策略:既然存在共同的致病路径,那么针对这条路径的药物就可能对多种疾病有效。靶向抑制拓扑异构酶I的异常活性、开发增强神经元DNA修复能力的药物、或是更精准地调控神经炎症,都可能成为减缓甚至阻断疾病进展的全新策略。
当然,前方的道路依然漫长。许多关键问题仍待解答:为何只有部分患者会出现灾难性的短缺失突变?个体的基因背景(如APOE4基因)如何影响这一过程?我们能否开发出安全有效的、能够穿透血脑屏障来修复神经元DNA的疗法?
从拳击手的悲剧,到实验室中揭示的基因密码,我们正以前所未有的深度凝视着人类大脑的脆弱与坚韧。CTE与阿尔茨海默病在神经元突变层面的意外“牵手”,不仅揭示了大脑在面对伤害时一条通往衰亡的共同路径,也为我们照亮了一条通往共同治愈的希望之路。这场对抗大脑“幽灵”的战斗,或许已经找到了真正的靶心。