对抗知识焦虑,从看懂这条开始
App 下载
造血干细胞的叛变:甲基化失衡催生血液病
表观遗传异常|曹雪涛团队|DNA甲基化|造血干细胞|骨髓增生异常综合征|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
表观遗传异常|曹雪涛团队|DNA甲基化|造血干细胞|骨髓增生异常综合征|肿瘤学|医学健康
你可能从未听说过骨髓增生异常综合征(MDS),但它是血液系统里最隐蔽的“叛变者”——患者的骨髓明明在疯狂造血,外周血里却没有足够的成熟血细胞,最终可能恶化为急性白血病。更诡异的是,这场叛变的源头,是本该维持造血稳态的造血干细胞(HSC)自己“疯”了。
过去几十年,科学家只知道这些叛变的干细胞存在表观遗传异常,却始终没看清具体的“叛变路线图”。直到2026年3月,中国医学科学院曹雪涛团队联合三家顶级医疗科研机构,终于在《Immunity & Inflammation》杂志上公布了关键证据:一张人类MDS造血干细胞的单碱基分辨率DNA甲基化全景图,以及藏在背后的“双重守门人”失守真相。
你可以把DNA甲基化想象成给基因贴“静音标签”——当某个基因的启动子区域被贴上足够多的甲基标签,这个基因就会被暂时“关闭”,不再指导合成蛋白质。正常情况下,这套标签系统精准调控着造血干细胞的命运:什么时候自我更新,什么时候分化成红细胞、白细胞,全靠标签的贴与撕维持平衡。
但真实的机制比这更精确:负责贴标签的是DNA甲基转移酶(DNMT),负责撕标签的则是TET家族蛋白——其中TET2是造血系统里最勤快的“撕标签工”,它能把甲基化的胞嘧啶逐步氧化,最终让标签彻底消失,重启基因表达。
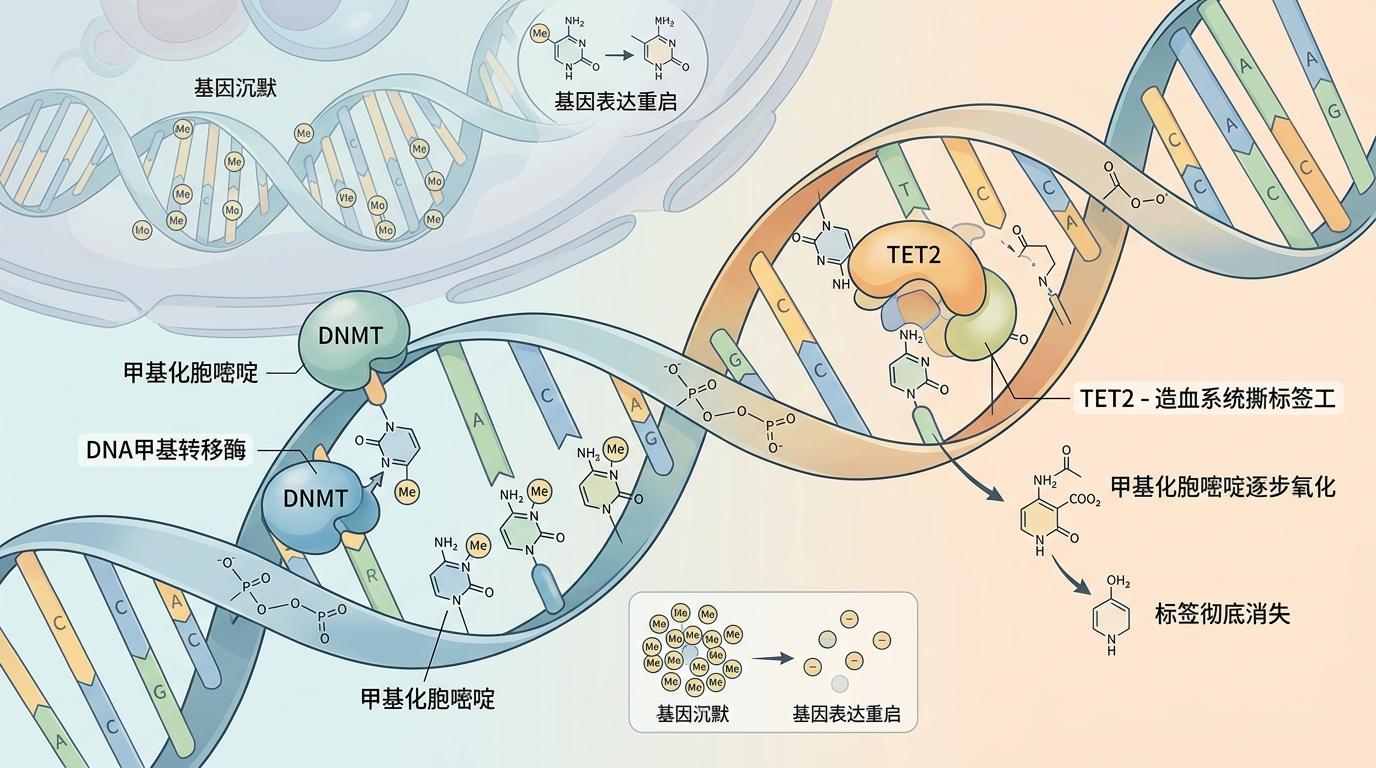
MDS患者的问题就出在这套标签系统的全面紊乱:研究人员对比了健康人和MDS患者的造血干细胞甲基化图谱,发现前者的标签分布像整齐的棋盘,后者却成了被打乱的拼图——CpG岛(基因启动子的常见区域)被过度贴标,导致大量肿瘤抑制基因被“静音”;而Alu等重复序列区域的标签却大量丢失,引发基因组不稳定。
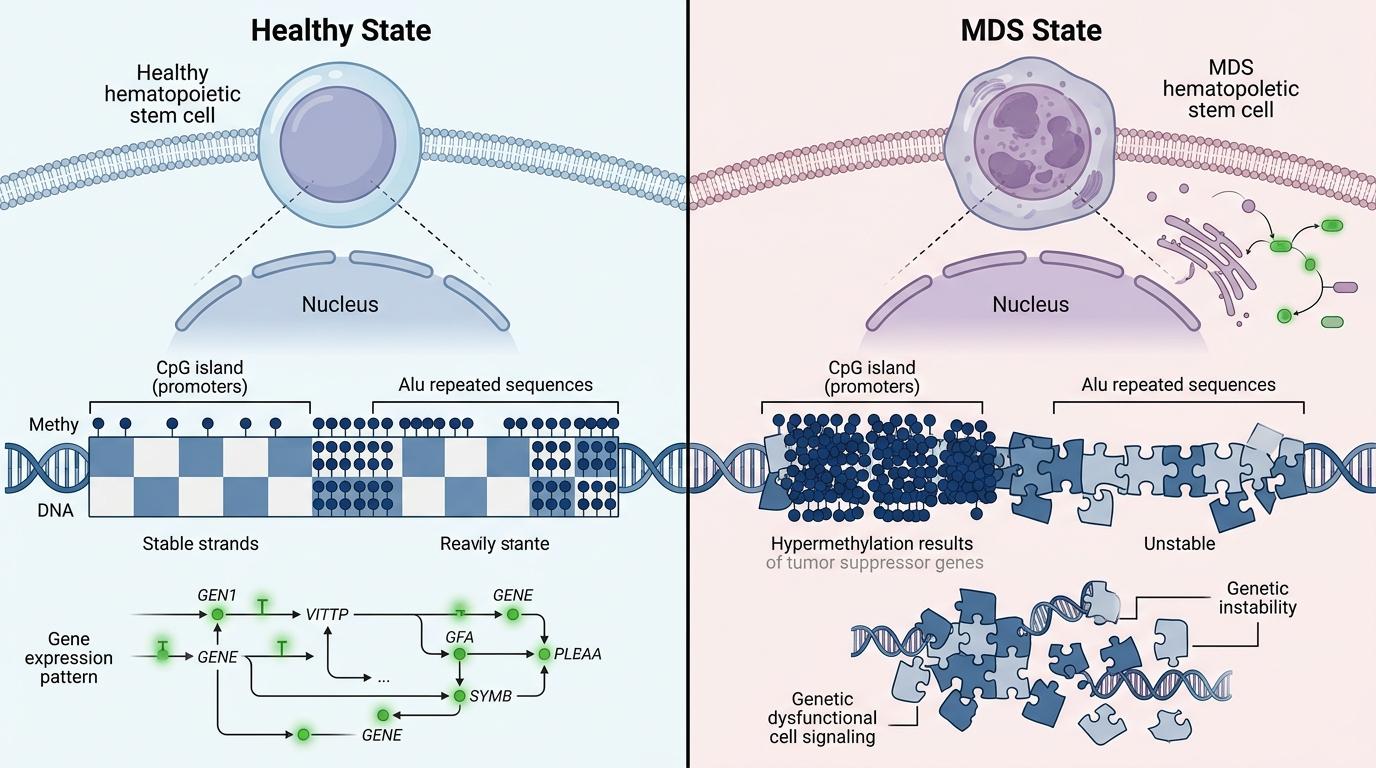
更关键的是,这些异常标签集中出现在两个关键基因上:GFI1的启动子被过度贴标,BMI1的启动子却几乎没了标签。
GFI1是造血干细胞里的“刹车踏板”。作为锌指转录抑制因子,它的本职工作是阻止干细胞过度增殖,确保分化过程有序进行。正常情况下,TET2会定期给GFI1的启动子“撕标签”,让它保持活跃,随时准备踩下刹车。
但在MDS患者中,TET2基因常常发生功能缺失突变——相当于“撕标签工”突然罢工。没有了TET2的干预,GFI1的启动子被贴上越来越多的甲基标签,最终彻底“静音”。刹车失灵的造血干细胞开始不受控制地自我更新,却无法分化成成熟的血细胞,这就是MDS最核心的“无效造血”症状。
研究团队在小鼠模型里验证了这个逻辑:
与此同时,BMI1基因因为启动子区域丢失了甲基标签,表达量异常升高——它就像干细胞的“油门踏板”,负责维持自我更新能力。刹车失灵加上油门踩满,造血干细胞彻底沦为了叛变的“癌细胞种子”。
过去治疗MDS,医生常用去甲基化药物(如阿扎胞苷),试图通过“广谱撕标签”恢复肿瘤抑制基因的活性,但这种方法就像用大扫帚打扫房间,虽然能清理部分垃圾,却也可能打乱正常的标签秩序,有效率仅约50%。
而TET2-GFI1轴的发现,给了医生一把精准的“镊子”。研究显示,携带TET2突变的MDS患者对去甲基化药物的响应率更高,这是因为他们的核心问题就是“撕标签工”罢工,药物刚好能补上这个缺口。更值得期待的是,维生素C可以作为TET酶的辅因子,增强其“撕标签”能力——动物实验显示,补充维生素C能显著抑制TET2缺失小鼠的异常造血,为辅助治疗提供了新方向。
但这套机制也并非完美:研究人员发现,MDS患者的表观遗传异常是一个复杂的网络,除了TET2和GFI1,BMI1、DNMT3B等多个因子也在相互作用,形成了精密的调控回路。目前的研究只是揭开了冰山一角,比如TET2缺失如何同时影响GFI1的甲基化和BMI1的去甲基化,其中的具体信号通路还需要进一步解析。
当我们把目光从微观的甲基标签拉远,会发现这场造血干细胞的叛变,本质上是生命调控系统的一次“程序bug”——原本精准的标签系统出现了紊乱,导致细胞偏离了预设的命运轨道。
“甲基化失衡,是血液病的隐秘导火索。”这句话或许能概括这项研究的核心价值:它不仅让我们看清了MDS的发病机制,更给所有表观遗传相关疾病的研究提供了一个范本——很多时候,疾病不是某个基因的“突然叛变”,而是一套精密调控网络的“逐渐失控”。
未来的某天,医生或许能通过检测造血干细胞的甲基化图谱,提前预判MDS的发生;也能通过精准调控TET2-GFI1轴,让叛变的干细胞重新回归正轨。而这一切,都始于科学家们用一张精细的图谱,看清了那些曾经看不见的“标签”。