
1 个月前

1 个月前
当我们提起p53,第一反应总是“抗癌卫士”——这个存在于每颗细胞里的蛋白,像个严谨的质检员,一旦发现DNA损伤就叫停细胞分裂,甚至直接“处决”癌变风险细胞。超过半数的癌症都和p53的失效有关,它的名字早已和肿瘤防治牢牢绑定。
但很少有人知道,这个“抗癌明星”还兼职着免疫系统的“维稳专员”。2026年3月,清华大学和四川大学的联合研究团队,在《Cell Reports》上揭开了p53的另一重身份:它能通过调控一种免疫细胞的代谢和基因表达,防止免疫系统“走火”攻击自身组织。而那些被自身免疫病困扰的患者,体内的这条调控通路,正悄悄失效。
为什么一个抗癌蛋白会和自身免疫病扯上关系?这得从我们体内的“免疫刹车”说起。
我们体内有一种叫调节性T细胞(Treg)的免疫细胞——你可以把它看成免疫系统的“刹车踏板”,专门负责管住那些亢奋的效应T细胞,防止它们不分敌我地攻击自身组织。一旦Treg细胞功能失常,类风湿关节炎、系统性红斑狼疮这类自身免疫病就会找上门。
过去我们以为,Treg细胞的活性只由它的“身份标记”Foxp3蛋白决定,但这次研究推翻了这个认知。团队发现,在自身免疫病患者的Treg细胞里,p53蛋白的含量比健康人低了一大截,同时另一种叫BCL-6的蛋白水平异常升高,两者呈严格的负相关。
更关键的是,当Treg细胞里的p53消失,这些“刹车踏板”直接失灵了:它们不仅没法抑制效应T细胞的增殖,连自己的核心功能基因都“沉默”了。在小鼠实验里,只要特异性敲除Treg细胞的p53,小鼠很快就出现了严重的自身免疫症状——淋巴结肿大、多器官炎症,和人类患者的表现如出一辙。
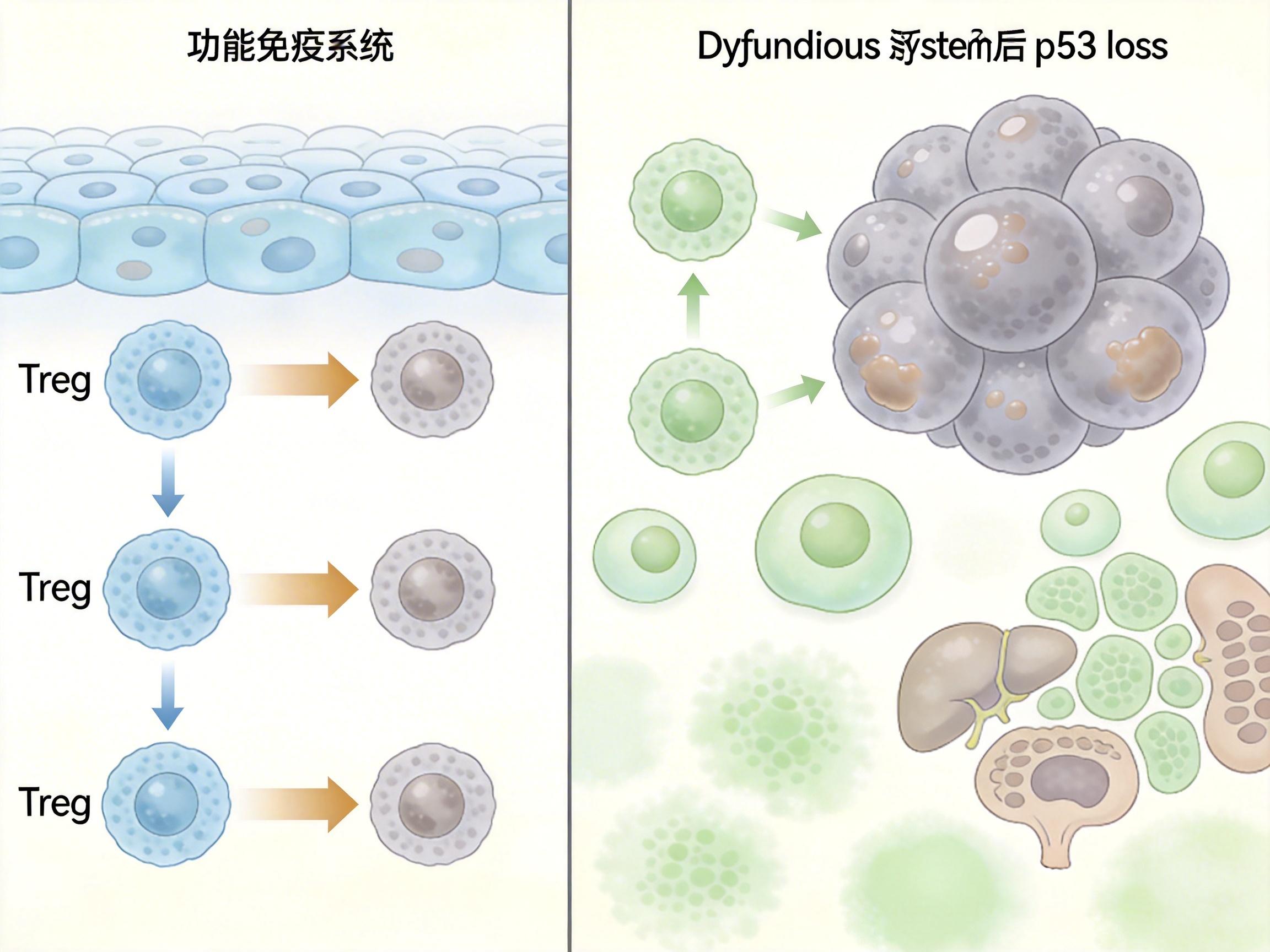
这不是p53第一次和免疫扯上关系,但却是第一次有人把它和Treg细胞的核心功能,用一条清晰的分子链条串了起来。
这条链条的核心,是一场发生在细胞内部的“代谢-表观遗传联动”。
你可以把细胞的基因表达想象成一本需要精准翻阅的书:组蛋白是书页的装订线,而组蛋白上的化学修饰,就是决定哪一页能被打开的“书签”。这次研究发现的“组蛋白丙酰化”,就是一种能激活基因的书签——它能让Treg细胞的功能基因保持“打开”状态,确保细胞能正常行使“刹车”职能。
而制造这个“书签”的原料,是一种叫丙酰辅酶A的代谢产物。研究团队发现,p53正是通过直接激活一种叫ALDH6A1的酶,来促进丙酰辅酶A的合成。当p53缺失,ALDH6A1的活性跟着下降,丙酰辅酶A不足,组蛋白丙酰化水平骤降,Treg细胞的功能基因就被“锁”了起来。
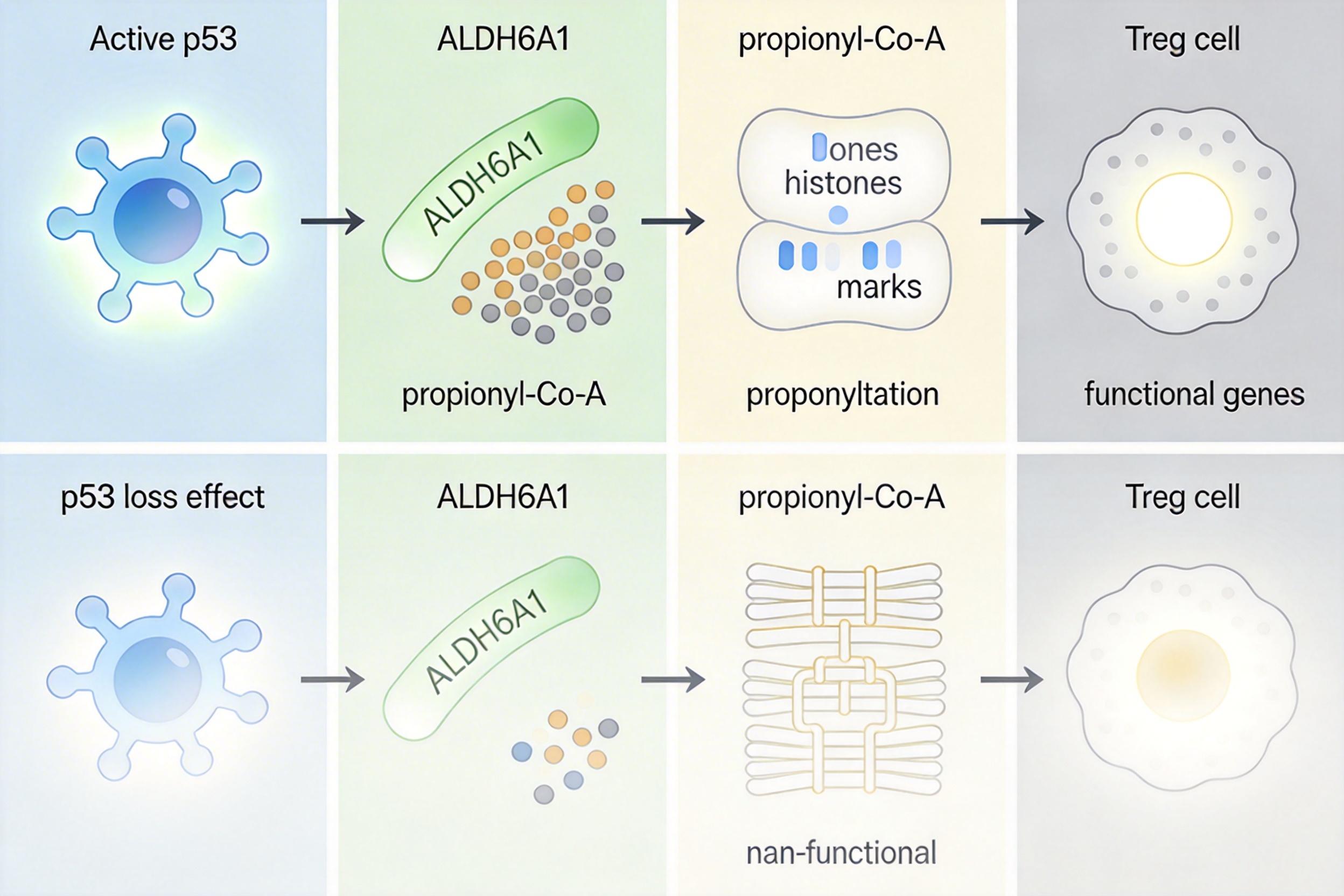
为了验证这条通路的关键作用,团队做了两组对照实验:
这就像找到了汽车刹车失灵的根源:不是刹车踏板坏了,是给踏板供能的油管堵了——而p53,就是那个控制油管开关的人。
这条p53-ALDH6A1-组蛋白丙酰化的信号轴,不只是实验室里的分子游戏,它和临床治疗直接相关。
研究团队分析了大量自身免疫病患者的临床样本,发现那些对一线治疗反应不佳的患者,体内的这条信号轴普遍受损——p53含量低,ALDH6A1活性不足,组蛋白丙酰化水平也远低于健康人。这意味着,这条通路的状态,或许可以成为预测患者治疗效果的生物标志物。
更重要的是,它为自身免疫病的治疗提供了新方向。过去我们治疗自身免疫病,要么用激素全面压制免疫系统,要么想办法增强Foxp3的表达,但前者副作用大,后者效果不稳定。而现在,我们有了更精准的靶点:比如用小分子药物激活p53,或者直接补充丙酰辅酶A,甚至可以开发ALDH6A1的激活剂,从根源上恢复Treg细胞的功能。
当然,这一切还需要更多的临床验证。比如不同自身免疫病患者的通路受损程度是否有差异?补充丙酰辅酶A的剂量和安全性如何把控?但至少,我们终于跳出了“只看Foxp3”的局限,找到了一条调控Treg细胞的全新路径。
当我们把p53从“抗癌明星”的单一标签里解放出来,才发现它像一个精密的调控枢纽,一边盯着细胞的癌变风险,一边维持着免疫系统的平衡。这次研究最动人的地方,不是发现了一个新的治疗靶点,而是让我们看到了生命系统的复杂性——一个蛋白的功能,从来不是孤立的;代谢和基因表达,也从来不是割裂的。
代谢为笔,表观遗传为纸,p53则是那个握笔的人,在每颗Treg细胞里书写着免疫耐受的故事。代谢定原料,表观塑功能,免疫守平衡。未来,当我们能精准调控这场细胞内的书写,或许就能让那些被自身免疫病困扰的人,重新找回身体的安宁。
点击充电,成为大圆镜下一个视频选题!