对抗知识焦虑,从看懂这条开始
App 下载
脓毒症炎症失控的真相:心脏竟是放大源头
重庆医科大学段晨阳团队|线粒体|多器官衰竭|心脏功能恶化|脓毒症|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
重庆医科大学段晨阳团队|线粒体|多器官衰竭|心脏功能恶化|脓毒症|感染性疾病|医学健康
想象一下:医生已经用最强效的抗生素杀死了引发感染的病菌,患者的体温也降了下来,但他的心脏功能却还在持续恶化,甚至出现多器官衰竭的“二次打击”——这是重症监护室里最让医生头疼的脓毒症困境。全球每年有近5000万人患上脓毒症,其中超过1100人因此死亡,而这种“感染控制后仍恶化”的谜团,困扰了医学界数十年。直到2026年4月,重庆医科大学段晨阳团队的一项研究,终于揭开了藏在血液循环里的秘密。
过去我们总以为,脓毒症里的心脏是被炎症攻击的“受害者”,但这项研究彻底推翻了这个认知——心脏其实是炎症风暴的“源头放大器”。心肌细胞里的线粒体含量占细胞体积的40%,是全身细胞中线粒体最密集的部位之一,同时心脏又负责血液的输入输出,天然就是向循环系统释放信号的“广播站”。
研究人员检测发现,脓毒症患者血液中,约25%的线粒体损伤信号(mtDAMP)都来自心肌细胞。这些信号不是以游离分子的形式飘在血液里,而是被打包进了一种叫线粒体微囊泡(mitoMVs)的“小包裹”里——就像细胞分泌的快递,带着破损线粒体的碎片,顺着血液流遍全身。
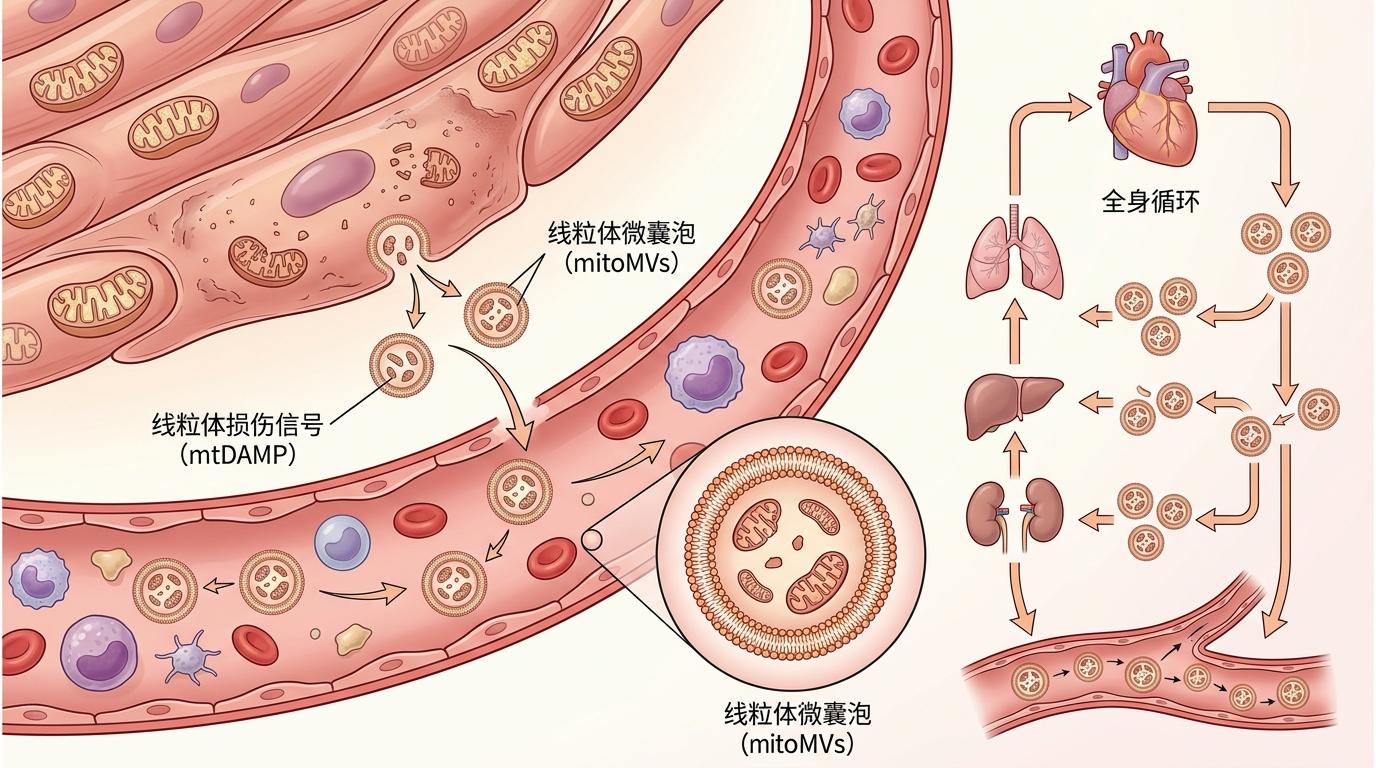
正常情况下,细胞里的受损线粒体有一套“垃圾处理系统”——线粒体自噬:细胞会把破损的线粒体包裹进自噬体,再送到溶酶体里彻底降解。但在脓毒症状态下,这套系统失灵了。
研究显示,脓毒症引发的线粒体活性氧(mtROS)大量积累,会激活RIP1/RIP3信号通路,直接阻断自噬体和溶酶体的融合。就像垃圾车开到了回收站门口,却被锁在了门外,只能拉着满车垃圾回到街上。这些无处可去的受损线粒体,只能被细胞打包成线粒体微囊泡,“扔”进血液循环里。
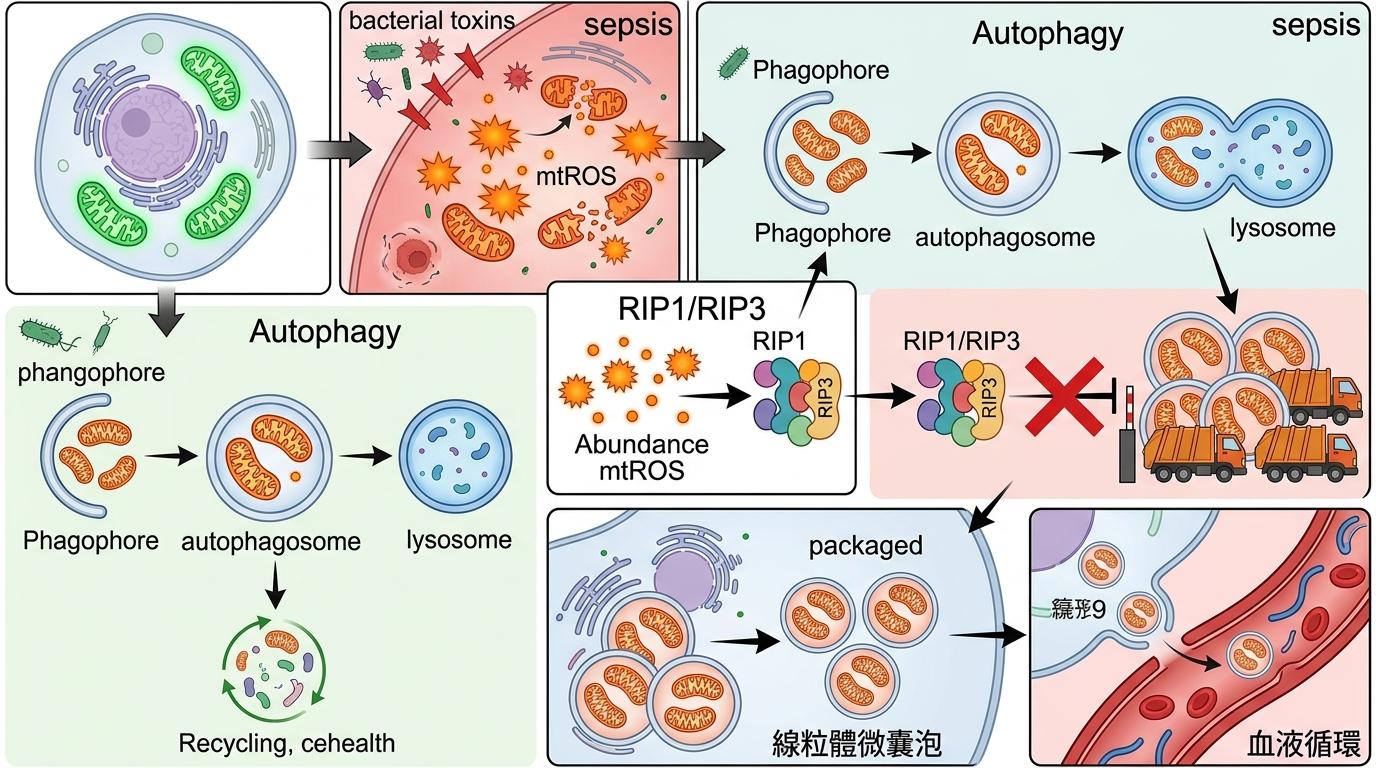
更关键的是,这些“垃圾快递”被远隔器官的细胞接收后,会激活一系列炎症通路:比如通过cGAS-STING通路诱导干扰素释放,通过TLR9激活NF-κB信号,还会让细胞的代谢模式从氧化磷酸化转向糖酵解——也就是所谓的Warburg效应,进一步增强炎症细胞的活性。而炎症反应又会反过来加重线粒体损伤,阻断自噬通路,形成一个越转越快的“炎症正反馈循环”。
这个DAMP-PAMP正反馈循环模型,不仅刷新了我们对脓毒症的认知,更给临床治疗带来了新的方向。过去我们治疗脓毒症,主要是用抗炎药物“灭火”,但现在我们知道,更关键的是要“切断火源”——要么阻止受损线粒体被打包成微囊泡,要么阻断这些微囊泡引发的炎症通路。
目前已经有一些潜在的靶点进入了研究视野:比如抑制RIP1/RIP3通路可以恢复自噬功能,减少线粒体微囊泡的释放;靶向cGAS-STING通路的抑制剂,可以阻断炎症信号的放大。不过研究人员也指出,这些策略还需要更多的临床验证,毕竟线粒体自噬的调控非常精细,过度激活或抑制都可能带来新的问题。
另外,线粒体微囊泡的含量也可能成为脓毒症的生物标志物——通过检测血液中mitoMVs的水平,可以更早地判断患者的炎症进展,甚至预测预后。
当我们把视线从“病菌”转向“细胞里的垃圾处理系统”,脓毒症的治疗似乎终于找到了新的突破口。这项研究最有价值的地方,不仅是揭示了一个分子机制,更是让我们意识到:很多全身性疾病的根源,可能藏在细胞间的“快递网络”里。
炎症的失控,从来不是单一器官的战争。 未来的脓毒症治疗,或许不再是简单的“抗炎”,而是从细胞层面重新调整“垃圾处理”和“信号传递”的平衡——这不仅是医学的进步,更是我们对生命本质认知的深化。