对抗知识焦虑,从看懂这条开始
App 下载
结直肠癌免疫荒漠突破:新疗法让“冷肿瘤”变热?
T细胞|奥沙利铂|免疫检查点抑制剂|pMMR类型|结直肠癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
T细胞|奥沙利铂|免疫检查点抑制剂|pMMR类型|结直肠癌|肿瘤学|医学健康
在对抗全球第三大常见癌症——结直肠癌的战场上,医学界曾一度陷入长达二十年的僵局。对于绝大多数(约95%)的患者而言,他们的肿瘤属于一种被称为“错配修复正常”(pMMR)的类型。这片广袤的“免疫荒漠”中,肿瘤细胞巧妙地伪装自己,使人体免疫系统的精锐部队——T细胞,无法识别和攻击。因此,当免疫检查点抑制剂(ICB)在黑色素瘤、肺癌等领域掀起革命时,pMMR结直肠癌患者只能隔岸观火。手术联合以奥沙利铂为代表的化疗方案,虽是标准疗法,但其治愈率的“天花板”早已显现,难以突破。
然而,这片沉寂的荒漠,正迎来破晓的曙光。一项颠覆性的研究,可能将彻底改写pMMR结肠癌的治疗法则。
荷兰癌症研究所的Myriam Chalabi教授及其团队,将目光投向了这片最难啃的“硬骨头”。他们主导的II期NICHE临床试验,针对31例早期pMMR结肠癌患者,在手术前仅给予两周期的双免疫联合治疗(纳武利尤单抗联合伊匹木单抗)。这是一种“新辅助”策略,意在术前就调动免疫系统,对肿瘤发起突袭。
发表于顶级期刊《Nature》的研究结果,令整个领域为之振奋:
这一数据,虽不及免疫治疗在“免疫热点”肿瘤中动辄超过50%的缓解率,但它首次有力地证明,即使是在pMMR这片贫瘠的土壤上,免疫疗法也能播下希望的种子,并收获实实在在的疗效。这不仅是一个数字的突破,更是观念上的破冰,为绝大多数结直肠癌患者打开了一扇全新的机遇之门。
为何这四分之一的患者能够幸运地走出“荒漠”?研究团队利用多组学技术,对肿瘤组织进行了地毯式搜寻,试图找出应答者的“通关密码”。出乎意料的是,答案并非指向传统的生物标志物——肿瘤突变负荷(TMB)。所有患者的TMB水平都很低,应答者与非应答者之间并无差别。
真正的线索,隐藏在更深层次的生物学特征中:
基因组的“混乱度”:研究发现,应答者的肿瘤细胞表现出更高的染色体基因组不稳定性。可以将其理解为,这些癌细胞的基因组更为混乱无序,这种内在的“缺陷”反而可能让它们在免疫系统面前更容易暴露。
关键基因的“组合拳”:一个特定的基因组合与疗效惊人地相关。当抑癌基因TP53发生突变,而驱动基因KRAS G12保持野生型(即未突变)时,患者的缓解率飙升至46%。相反,TP53野生型且KRAS G12突变的患者,无一例外地对治疗无效。这为精准筛选获益人群提供了强有力的分子依据。
相比之下,无应答者的肿瘤则呈现为“炎症-纤维化”亚型,大量的肿瘤相关成纤维细胞(CAF)构筑起一道物理和生化的“屏障”,让免疫细胞寸步难行。
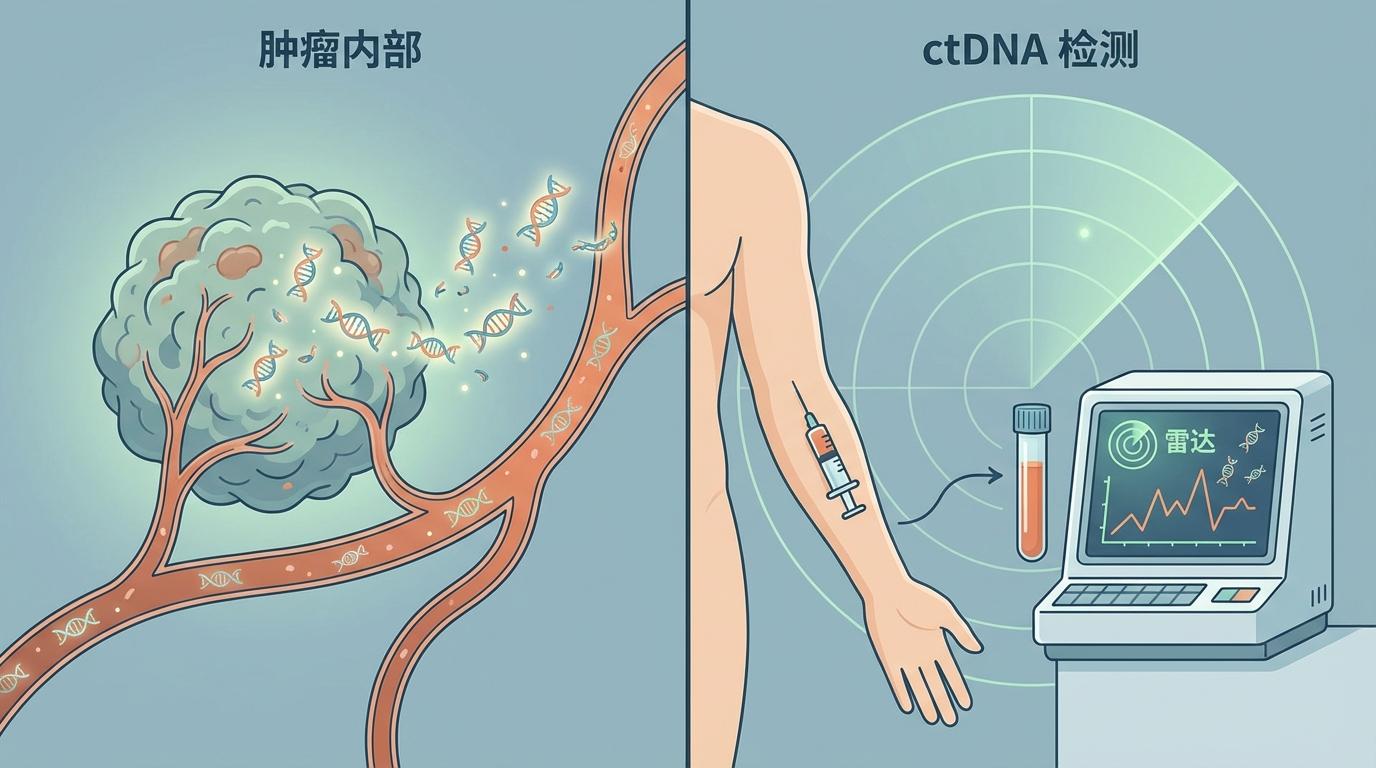
除了深入肿瘤内部寻找线索,该研究还展示了一项极具潜力的“雷达”技术——循环肿瘤DNA(ctDNA)检测。ctDNA是肿瘤细胞释放到血液中的DNA碎片,通过简单的抽血化验,就能实时追踪肿瘤的动态。
研究结果清晰地显示:
更重要的是,这一早期信号与患者的长期命运紧密相连。在中位长达56个月的随访中,所有ctDNA转阴的应答者均未复发,而无应答者中则出现了6例复发。这意味着,ctDNA有望成为一个灵敏的“哨兵”,在治疗早期就精准预测疗效和预后,帮助医生及时调整治疗方案,实现真正的个体化治疗。
NICHE试验的成功并非孤例,它代表了全球科学家试图将“冷肿瘤”转化为“热肿瘤”的共同努力。在pMMR结直肠癌领域,更多的“组合拳”策略正在涌现:
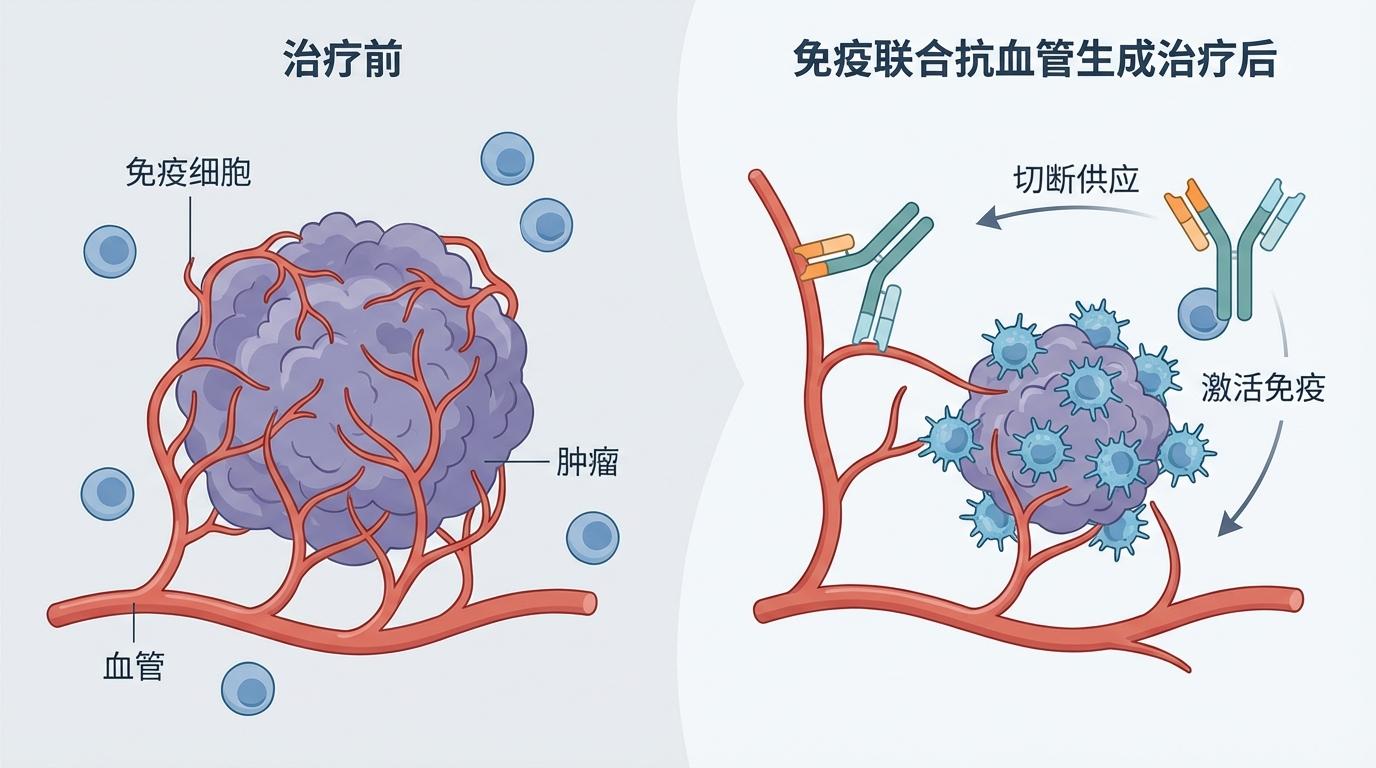
免疫联合抗血管生成:切断肿瘤的“粮草供应线”——血管,不仅能饿死癌细胞,还能改善肿瘤微环境,为免疫细胞的进入开辟道路。中国的创新药物,如康方生物研发的PD-1/VEGF双特异性抗体(依沃西),在联合化疗一线治疗pMMR/MSS型转移性结直肠癌的早期研究中,展现了高达81.8%的客观缓解率,潜力巨大。
免疫联合放化疗:传统的放疗和化疗在杀死癌细胞的同时,能释放出大量肿瘤抗原,如同在战场上点燃了“烽火”,吸引免疫系统的注意,从而为后续的免疫治疗创造条件。
这些多元化的策略,正从不同维度共同破解pMMR结直肠癌的免疫耐受难题,一个多兵种协同作战的新时代正在到来。
NICHE试验及其揭示的生物学机制,为早期pMMR结肠癌的治疗带来了范式转变的可能。我们可以预见一个全新的诊疗路径:一位新确诊的患者,不再是千篇一律地走向手术室和化疗科,而是首先通过基因组和ctDNA检测,评估其成为免疫治疗“应答者”的潜力。对于那些拥有“通关密码”的幸运儿,一次短程、精准的新辅助免疫治疗,或许就能让他们避免冗长的化疗周期,甚至获得更好的长期生存。
从“免疫荒漠”到“希望绿洲”,这不仅是一次科学的胜利,更是对生命的深刻洞察。它告诉我们,即使在最顽固的堡垒中,也可能存在着通往胜利的密道。而找到这把钥匙的,正是不断深入探索肿瘤与免疫系统之间复杂对话的科学精神。