对抗知识焦虑,从看懂这条开始
App 下载
癌细胞的增殖开关,竟藏在细胞膜的脂质里
胶质母细胞瘤|肺癌|麻省理工学院|细胞膜脂质|EGFR受体|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
胶质母细胞瘤|肺癌|麻省理工学院|细胞膜脂质|EGFR受体|肿瘤学|医学健康
每年全球有数百万人因肺癌、胶质母细胞瘤去世,这些癌症的罪魁祸首之一是EGFR——一种本该像“生长开关”的细胞表面受体:有生长因子就打开增殖信号,没有就乖乖闭合。但麻省理工学院的研究团队最近发现,有些癌细胞根本不需要“外来指令”,它们的EGFR会被自己的细胞膜“焊死”在开启状态。这不是科幻小说里的设定,而是发生在微观世界的真实机制——我们一直以为只是“细胞外衣”的细胞膜,其实是操控癌细胞疯长的幕后导演。为什么细胞膜能绕过生长因子直接控制EGFR?这得从一层看不见的脂质说起。
你可以把EGFR想象成一个插在细胞膜上的“信号插座”:正常情况下,只有生长因子(EGF)这个“插头”插进来,它才会向细胞内部传递“开始增殖”的电信号。但研究人员用无细胞表达技术,把完整的EGFR整合进成分精准可控的纳米圆盘膜模型后,发现了完全不同的图景。
当膜里的阴离子脂质含量达到癌细胞中常见的60%时——这是正常细胞的4倍——EGFR会自动“弹开”内部的锁定结构,就算没有EGF,也能牢牢抓住ATP分子,持续传递增殖信号。单分子荧光共振能量转移实验显示,此时EGFR的胞内结构域处于“开放态”,就像插座的插簧被掰开,随时能接通电流。
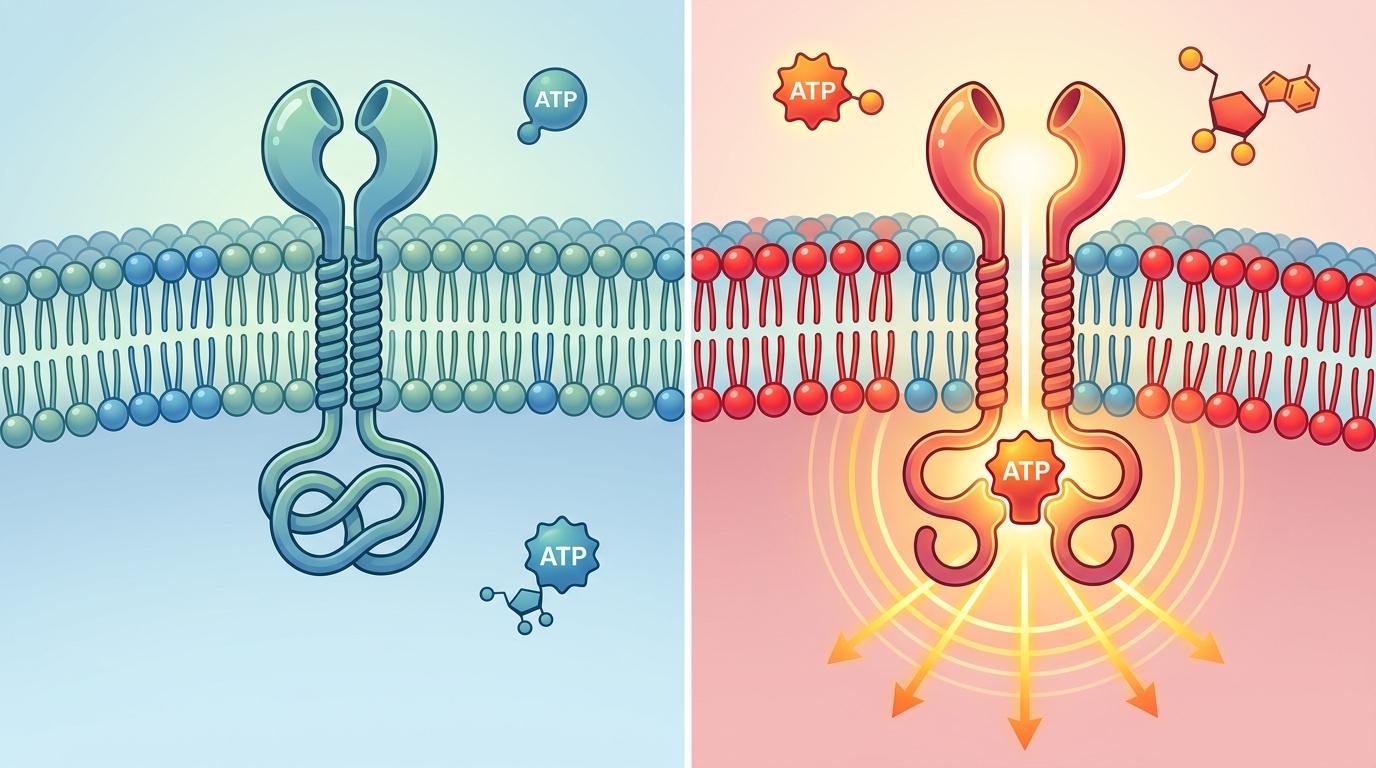
更关键的是,这种激活不是偶然的:阴离子脂质带负电,会和EGFR胞内近膜区的正电氨基酸残基形成静电相互作用,就像磁铁吸住金属片,把EGFR的结构“掰”成了激活状态。而在正常细胞的15%阴离子脂质环境下,这种静电拉力不够,必须等EGF来帮忙。
如果说阴离子脂质是EGFR的“油门踏板”,那胆固醇就是它的“刹车”。研究人员在纳米圆盘中加入胆固醇后发现,EGFR的构象变化被显著抑制——就算有EGF结合,它也很难切换到激活态。这是因为胆固醇会增加细胞膜的刚性,就像给插座套了个塑料壳,让插簧没法弹开。
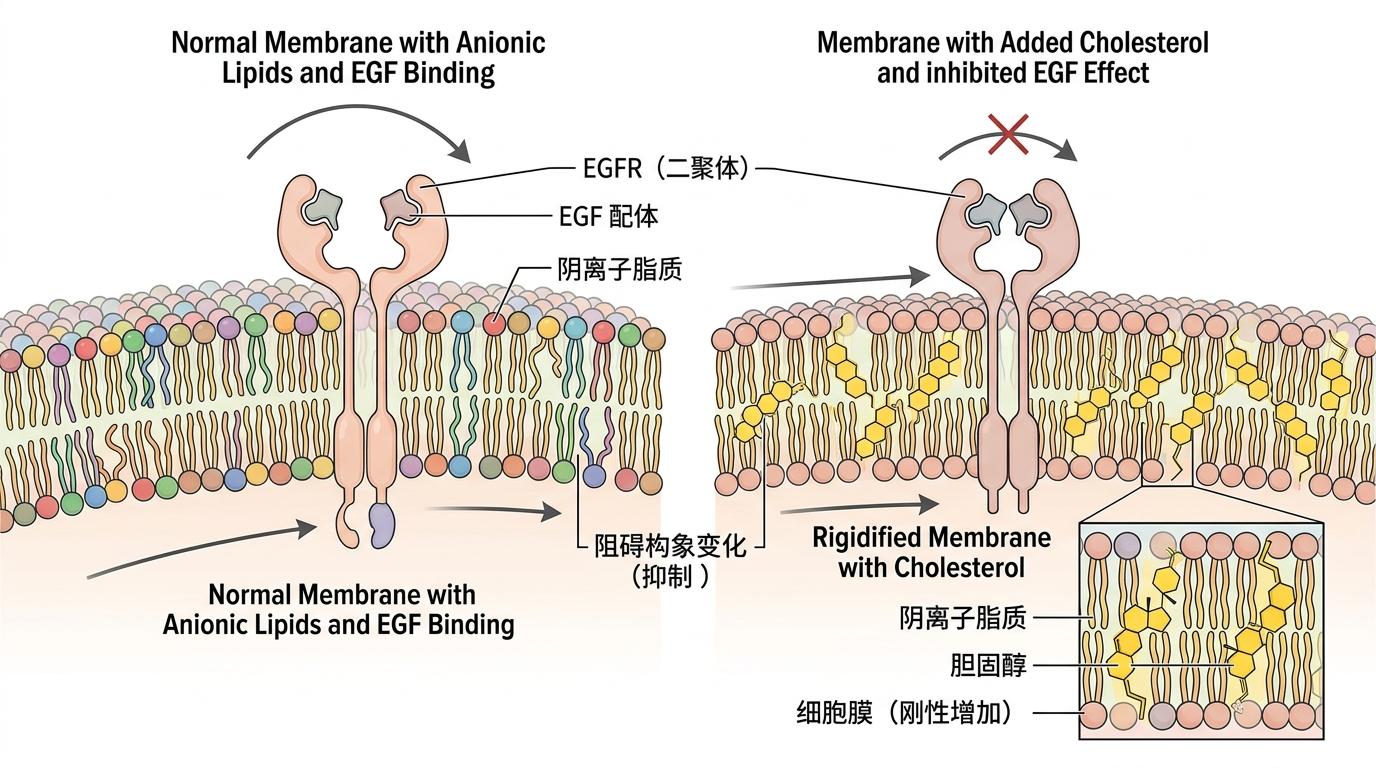
有意思的是,胆固醇的作用还分“内外”:细胞膜内叶的胆固醇会直接结合EGFR跨膜区的特定位点,稳定它的非活性构象;而外叶的胆固醇则通过形成“脂筏”,把EGFR限制在不能激活的区域。但癌细胞会破坏这种平衡:它们的脂质代谢会疯狂合成阴离子脂质,同时降低胆固醇的调控能力,让EGFR的油门被踩死,刹车却失灵。
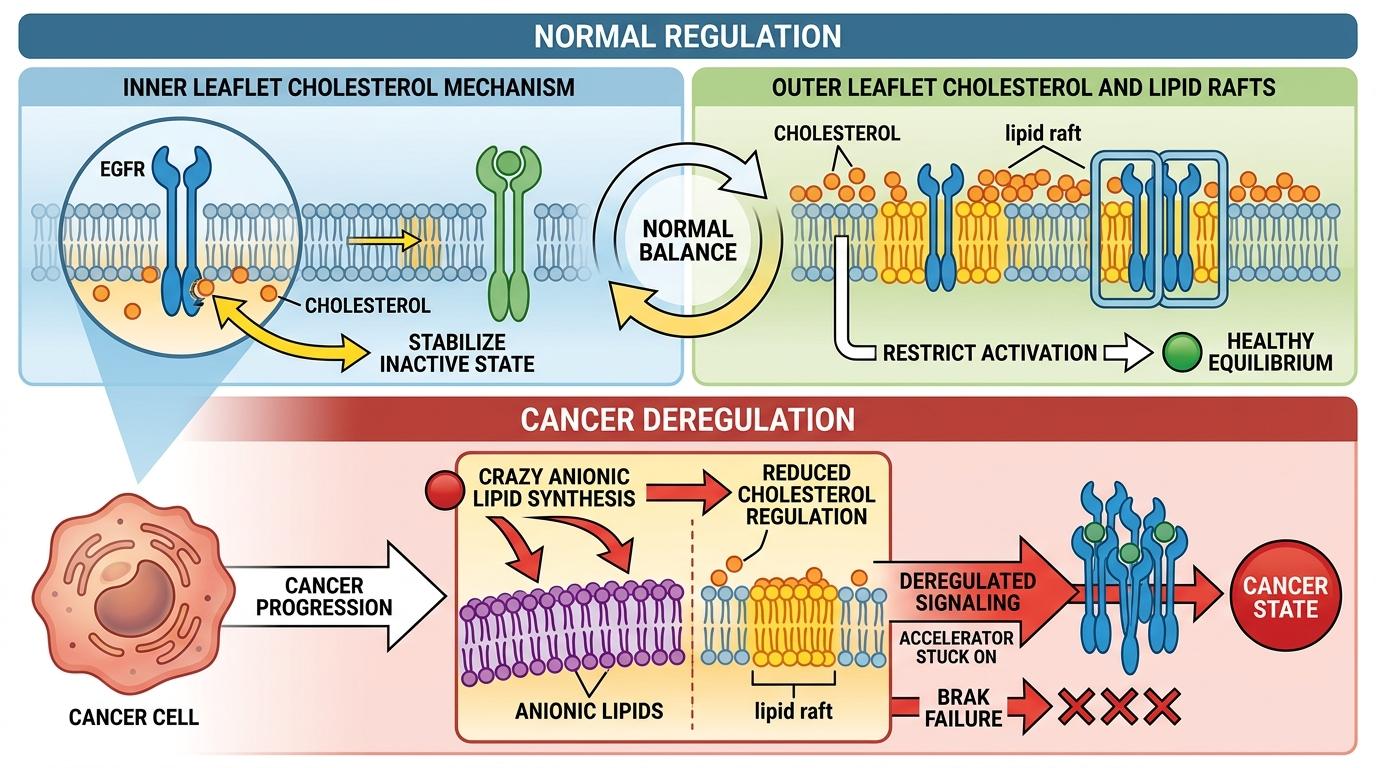
更值得注意的是,这种脂质调控不是EGFR独有的——其他受体酪氨酸激酶的膜邻近区域也有类似的保守碱性残基,这意味着细胞膜可能是一整类细胞信号的“隐形调控者”。
这一发现给癌症治疗带来了全新的思路:与其盯着EGFR这个“插座”做文章,不如去调控细胞膜的“电路环境”。比如,用药物中和细胞膜表面的负电荷,或者调整胆固醇的分布,就能把被焊死的增殖开关重新扳回去。
已经有初步的临床线索支持这个方向:抗抑郁药氟西汀能抑制鞘磷脂代谢酶,改变癌细胞膜的脂质组成,让EGFR从激活区移出,在胶质母细胞瘤小鼠模型里,联合化疗药能实现肿瘤完全消退;而他汀类降胆固醇药物和EGFR靶向药联用,能显著延长肺癌患者的生存期。
当然,这项研究也有局限:纳米圆盘模型毕竟是简化版的细胞膜,真实细胞里还有上千种脂质、蛋白和糖类相互作用,要把实验室的发现转化成临床疗法,还需要更多研究来厘清复杂的调控网络。
我们花了几十年时间,把细胞信号通路拆解成一个个精确的“开关”和“按钮”,却忽略了包裹着它们的“容器”本身就是个活的调控系统。细胞膜不再是被动的“外衣”,而是细胞信号的“舞台导演”——它决定着哪些蛋白能上台,以什么姿态传递信号。
“细胞的命运,藏在脂质的比例里。”当我们开始关注这些曾经被忽略的“背景板”,或许能找到攻克癌症的新钥匙。毕竟,癌细胞的疯狂生长,从来都不是单个蛋白的错,而是整个细胞环境失控的结果。