对抗知识焦虑,从看懂这条开始
App 下载
衰老细胞靠GPX4续命,抑制剂能精准清剿
小分子抑制剂|铁死亡|僵尸细胞|GPX4酶|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
小分子抑制剂|铁死亡|僵尸细胞|GPX4酶|分子细胞生物学|生命科学
你或许没听过“僵尸细胞”,但你的身体里一定住着它们。这些细胞是身体的“前卫士”——当DNA损伤或癌变风险出现时,它们会主动停止分裂,把隐患掐灭在萌芽里。但它们也是“赖着不走的麻烦制造者”:不分裂也不死亡,长期盘踞在组织里,分泌炎症因子搞破坏,从骨关节炎到癌症,都有它们的影子。
过去十年,科学家一直在找能精准清除这些细胞的“靶向药”,却始终没摸到它们的命门。直到帝国理工学院的团队,从一万多种化合物里揪出了四个不起眼的小分子,才终于发现:这些僵尸细胞,全靠一种叫GPX4的酶吊着一口气。
先给你拆解两个核心关键词:
帝国理工的研究团队发现,衰老细胞其实早就站在了铁死亡的边缘:它们的氧化应激水平是正常细胞的2-3倍,细胞内Fe²⁺含量也高得离谱,氧化脂质随时可能“炸锅”。但它们早有准备——大幅上调GPX4的表达,靠这只“灭火队长”硬生生把死亡挡在了门外。
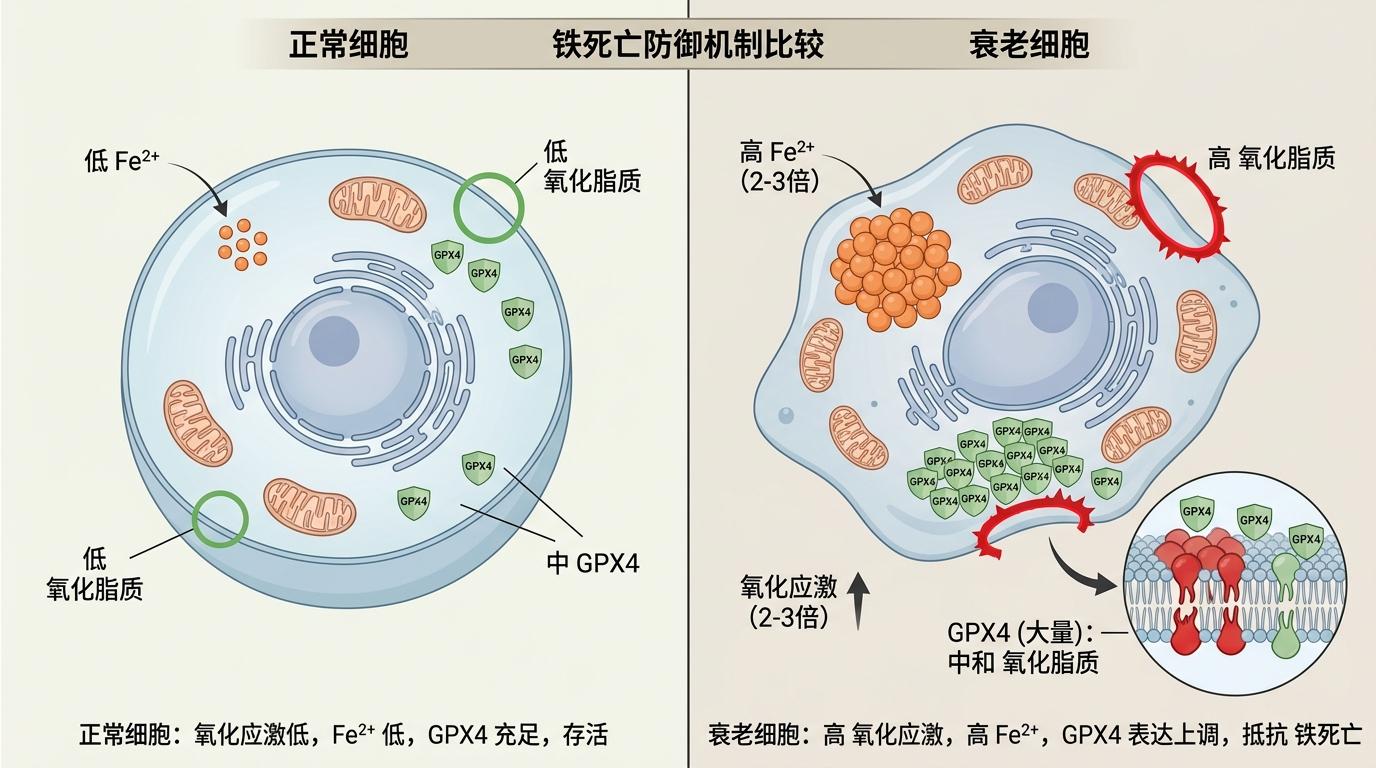
这就像一栋随时会起火的房子,衰老细胞靠24小时不停转的消防系统维持着平衡。而那四个小分子SCLA1-4,以及现有的GPX4抑制剂,就是精准切断消防系统电源的开关。
研究团队在三种癌症模型里验证了这个思路的威力:用化疗药把肿瘤细胞逼入衰老状态后,再用GPX4抑制剂补一刀,那些原本赖着不走的衰老肿瘤细胞,会被铁死亡彻底清剿。在黑色素瘤模型里,联合治疗组的肿瘤复发率比单独化疗组低了60%;前列腺癌模型中,肿瘤体积缩小了近一半。
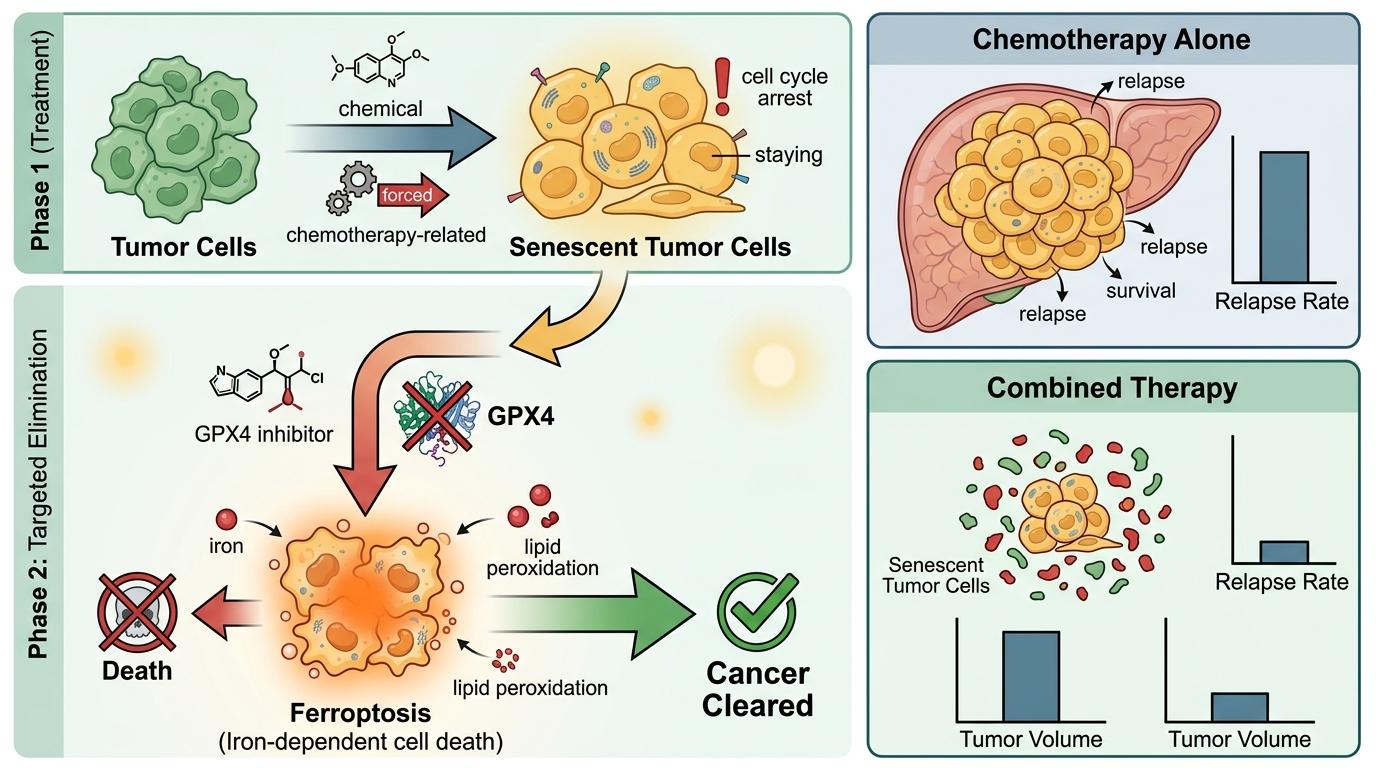
有意思的是,正常细胞虽然也需要GPX4,但它们的“火灾风险”远低于衰老细胞——氧化应激水平低,Fe²⁺含量也稳定,所以即使GPX4被部分抑制,也不会触发铁死亡。这就给了药物足够的“安全空间”:精准杀衰老细胞,不碰正常细胞。
不过也有个小插曲,研究人员一开始筛选的是一万多种亲电化合物,这类化合物能像魔术贴一样粘住蛋白的特定位点,原本是冲着其他靶点去的,没想到最后精准命中了GPX4,也算歪打正着。
当然,这个新靶点也不是完美的。
第一道坎是药物的特异性。目前的GPX4抑制剂大多是共价结合型,虽然能精准粘住GPX4,但也可能不小心粘到其他蛋白,带来潜在的毒副作用。比如Rubedo公司进入临床的RLS1496,虽然在纳摩尔浓度下就能选择性杀衰老细胞,但长期使用的安全性还需要验证。
第二道坎是衰老细胞的异质性。不同组织的衰老细胞,GPX4的表达水平不一样——肝脏的衰老细胞GPX4上调了3倍,皮肤的只上调了1.5倍,这意味着药物的剂量和效果会因组织而异。未来可能需要结合不同的生物标志物,给不同患者定制方案。
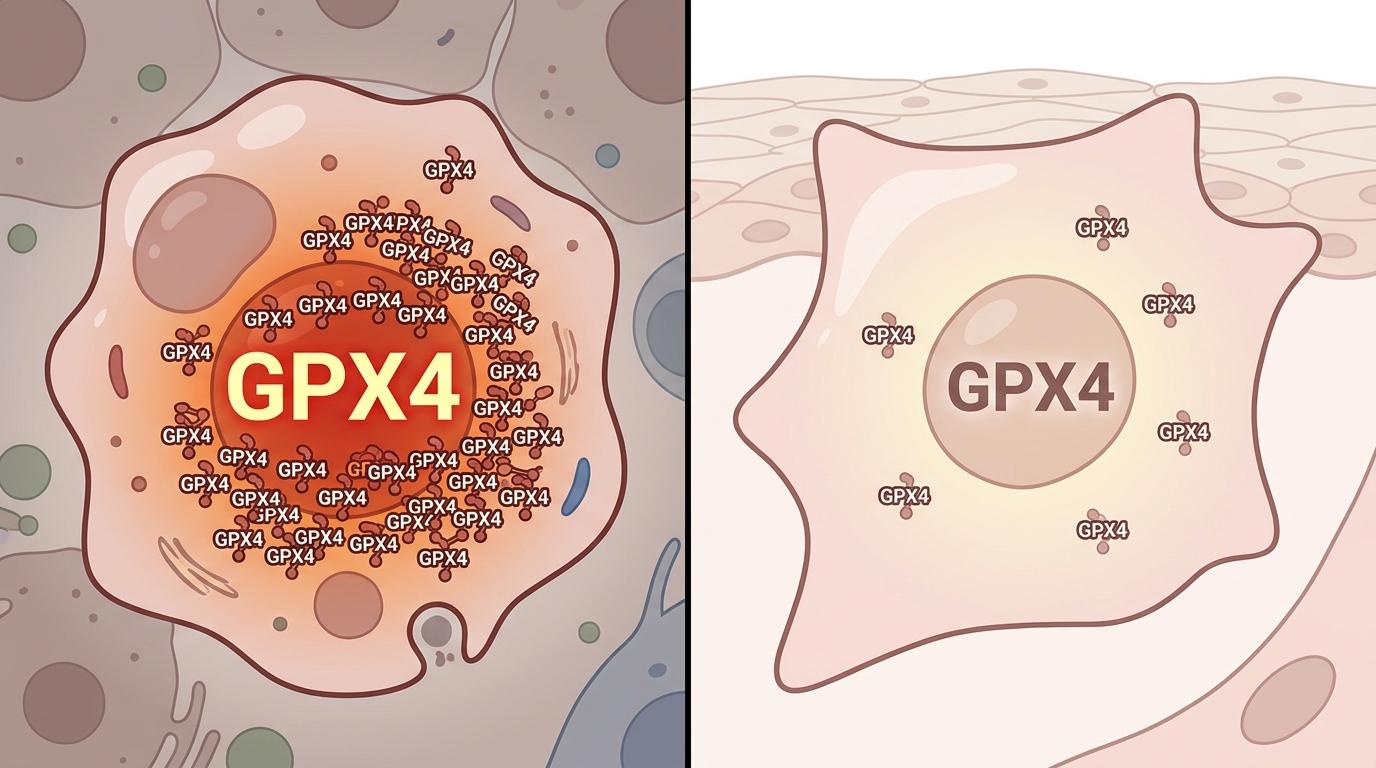
第三道坎是伦理和边界。衰老细胞不全是坏的:伤口愈合时,它们会分泌因子促进组织修复;胚胎发育时,它们还参与器官塑形。如果不分青红皂白全清除,可能会影响正常的生理功能。
从2012年铁死亡被正式命名,到今天找到衰老细胞的GPX4命门,人类用了14年,终于摸到了精准抗衰老的门槛。这不再是“吃抗氧化剂延缓衰老”的模糊思路,而是像狙击手一样,瞄准衰老细胞最脆弱的那个点扣动扳机。
未来十年,我们或许能看到第一批针对GPX4的抗衰老药物上市,不仅能延缓骨关节炎、阿尔茨海默病这类老年病的进展,还能让癌症患者的治疗更彻底。但更重要的是,这让我们意识到:衰老不是不可逆转的自然规律,而是一种可以被精准调控的细胞状态。
精准狙杀衰老,而非对抗时间。