对抗知识焦虑,从看懂这条开始
App 下载
HIV藏了个环状RNA帮自己疯狂复制
Grace Chen团队|HIV复制机制|Tat蛋白|环状RNA|circHIV|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
Grace Chen团队|HIV复制机制|Tat蛋白|环状RNA|circHIV|感染性疾病|医学健康
30年来,人类对付HIV的思路像在打地鼠:它突变,我们就换靶向药物;它躲进细胞潜伏,我们就想办法“唤醒”它。但耶鲁大学的Grace Chen团队,最近挖到了HIV藏得最深的一个“帮凶”——一种叫circHIV的环状RNA。这种没有首尾的闭合RNA,能死死抱住HIV的关键蛋白Tat,把病毒的复制效率拉到最高。更棘手的是,它比普通线性RNA稳定10倍以上,能在感染者的血浆里长期存在。我们一直以为已经摸透了HIV的基因套路,现在才发现,它还留着一手没被破解的调控密码。
2019年,Grace Chen带着团队启动项目时,只是凭着直觉:HIV的基因组这么复杂,说不定能产生circRNA——这种2013年才被证实普遍存在的RNA,最大特点是没有游离的首尾,像个闭合的圆环,能躲过细胞里的降解酶,活成“不死的调控者”。
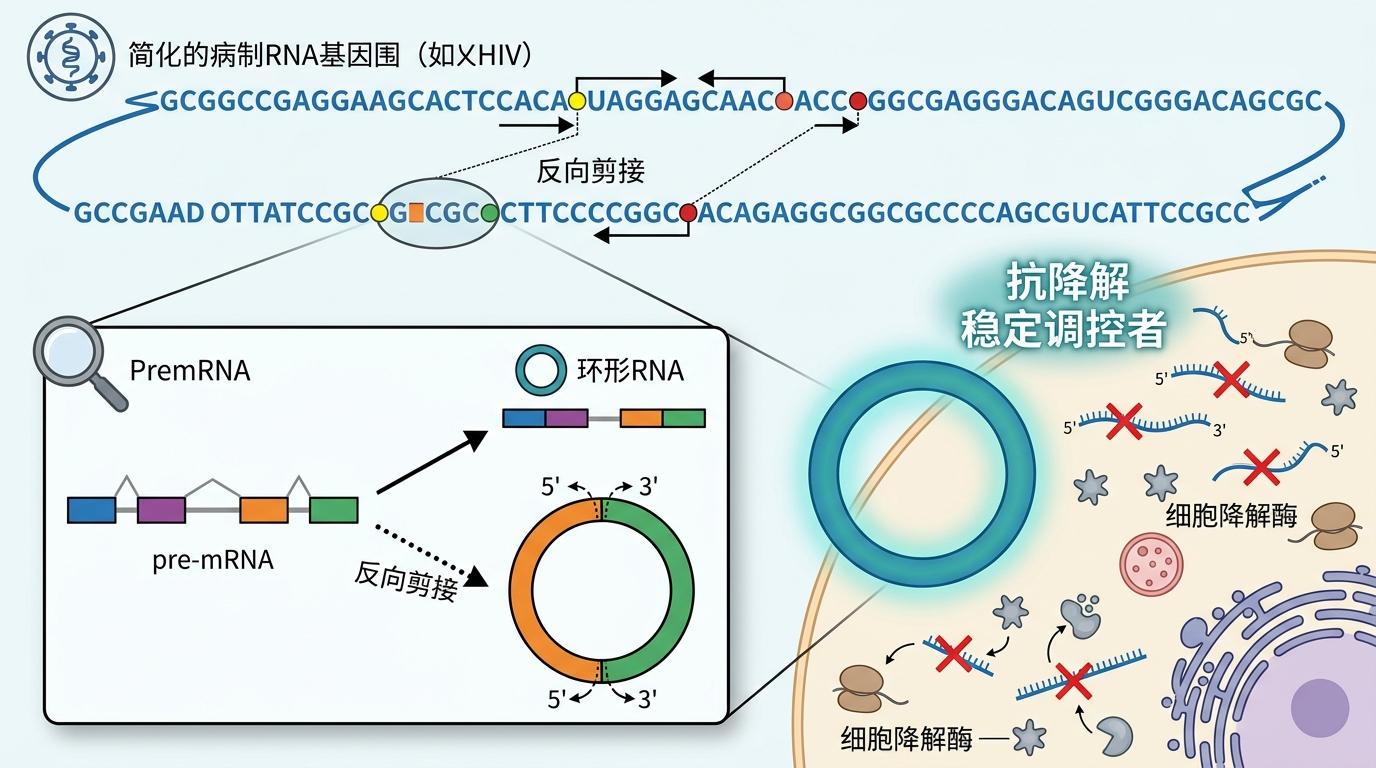
他们先给HIV感染的细胞做了RNA测序,果然在一堆线性RNA里,揪出了表达量极高的环状结构。为了确认这不是实验污染,他们又在感染者的血浆样本里找到了它,还给它起了名字:circHIV。
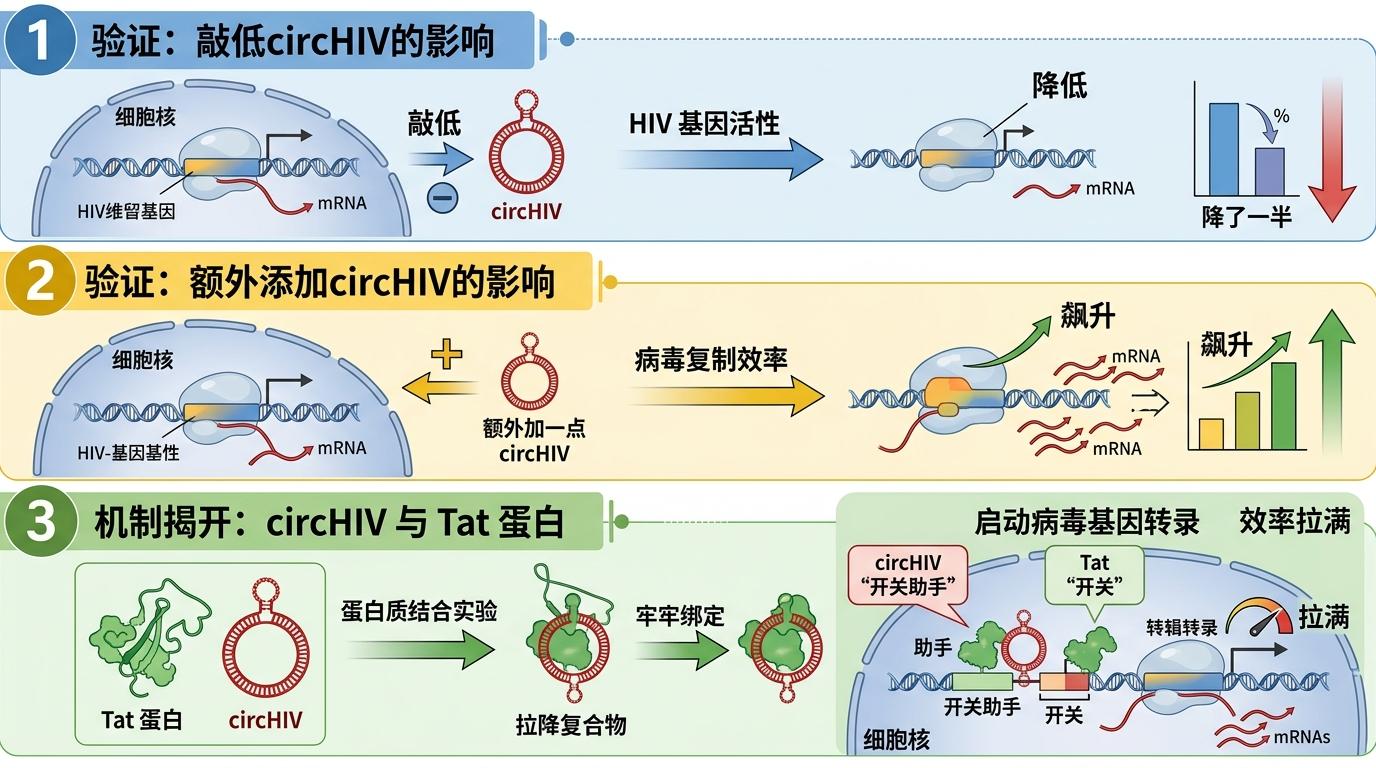
接下来的验证像一场精准的“拆弹实验”:把细胞里的circHIV敲低,HIV的基因活性直接降了一半;额外加一点circHIV,病毒的复制效率立刻飙升。最后用蛋白质结合实验一查,谜底彻底揭开——circHIV会和HIV的Tat蛋白牢牢绑定,而Tat正是启动病毒基因转录的“开关”。相当于HIV给自己找了个“开关助手”,能把转录效率拉满。
2020年初,关键数据刚收集完,新冠疫情就来了。实验室关了4个月,团队只能在家开线上会议,对着电脑里的测序数据反复推演。等终于能回实验室,他们却卡在了最基础的一步:没有未感染HIV的血浆对照样本。
没人犹豫,团队成员卷起袖子,每个人都捐了血浆。走廊对面的医生帮忙抽了血,样本很快到位。补完最后一组对照实验,结果和之前的推论完全吻合:circHIV只在感染细胞和感染者体内存在,是HIV独有的“身份标记”。
这背后是一场跨学科的接力:免疫学家找样本,分子生物学家做蛋白结合实验,生物信息学家分析测序数据。Chen说,这不是某一个人的功劳,是“一群人盯着同一个谜题,终于把它拼出了轮廓”。
circHIV的发现,给HIV治疗打开了一个新窗口。和容易突变的病毒蛋白不同,circHIV的环状结构是病毒复制的“刚需”——只要能打断它和Tat蛋白的结合,就能直接掐断病毒的转录动力。而且它在血浆里稳定存在,还能作为监测病毒活性的生物标志物:只要感染者体内的circHIV水平下降,就说明治疗真的起效了。
但从实验室到临床,还有几道坎要跨。首先是特异性:circHIV的序列和HIV的线性RNA高度相似,要设计只打circHIV的药物,不能误伤正常RNA;其次是递送,环状RNA分子量大、带负电,很难穿透细胞膜;更关键的是,我们还不知道circHIV会不会影响宿主的正常细胞功能——毕竟细胞里也有自己的circRNA,万一药物“认错了人”,可能会带来新的副作用。
我们总以为,对付病毒就是找到它的“致命弱点”,然后精准打击。但HIV的故事告诉我们,病毒比我们想象的更狡猾——它会利用细胞的规则,给自己搭建全新的调控网络。circHIV的发现,不是给HIV治疗画上了句号,而是打开了一扇门:原来病毒的基因里,还藏着这么多我们没读懂的暗码。
病毒的进化,永远走在药物前面,但人类的好奇心,总能追上它的脚步。 或许再过10年,我们回头看今天的发现,会意识到这是破解HIV潜伏难题的关键一步——毕竟,找到敌人的“帮凶”,才是真正打赢这场持久战的开始。