
2 个月前

2 个月前
我们的身体,从每一次呼吸到伤口的愈合,都依赖于细胞间一场无声的对话。但这场对话不仅关乎化学信号,更关乎一种我们长期忽视的语言——物理“触觉”。一个细胞,如同一个微型的生命体,能敏锐地感知其所在“土地”的软硬。它是在柔软如凝胶的组织中,还是在坚硬如磐石的骨骼上?这个看似简单的物理差异,却能深刻地决定它的增殖、分化,乃至最终的命运。然而,细胞究竟是如何“触摸”并解读这个世界的?这个谜题的答案,正指向细胞内部一个曾被误解的结构。
想象一下细胞内部是一个繁华的都市。其中,肌动蛋白纤维如同密布的街巷,负责城市的局部交通和建设,科学家们早已熟知它们在感知外界压力、产生牵引力方面的核心作用,并将其视为细胞“触觉”的主要来源。而另一套系统——微管,则像是贯穿全城的高速公路,长期以来,我们认为它的主要功能是运输物资、维持城市结构,以及在细胞分裂时充当拉开染色体的“轨道”。它被视为一个相对被动的结构,而非主动的感知者。
然而,生命总在挑战我们的既有认知。如果说肌动蛋白是细胞用来“抓握”和“感受”世界的“肌肉”,那么微管会不会是传递这些感觉的“神经”?这个问题的答案,在最近的一项研究中,获得了颠覆性的突破。
2026年1月30日,一篇发表在国际顶级期刊《Bone Research》上的研究报告,为我们揭开了微管的神秘面纱。由四川大学谢静、刘肖珩团队与中国科学院深圳先进技术研究院司龙龙团队合作完成的这项研究,首次系统性地揭示了软骨细胞在分裂过程中,其内部的微管网络如何动态响应微环境的机械硬度。
研究团队通过精密的材料科学技术,制造出不同硬度的培养基底,模拟了从健康软骨(约46千帕)到骨关节炎病变区域硬化软骨(约450千帕)的微环境。他们惊奇地发现:
这表明,微管远非被动的“高速公路”,而是一个高度敏感的“智能路网”,能够根据外界“路况”(环境硬度)进行实时调整。这一发现,将力学生物学的研究焦点,从肌动蛋白的“独角戏”,引向了整个细胞骨架协同作用的“交响乐”。
那么,细胞是如何将“触摸”到的硬度信号,转化为重组微管的具体指令的呢?研究团队通过RNA测序、蛋白质组学等先进技术,精准地锁定了一条此前未知的信号传导链条:ILK-Refilin B/p-Smad3轴。
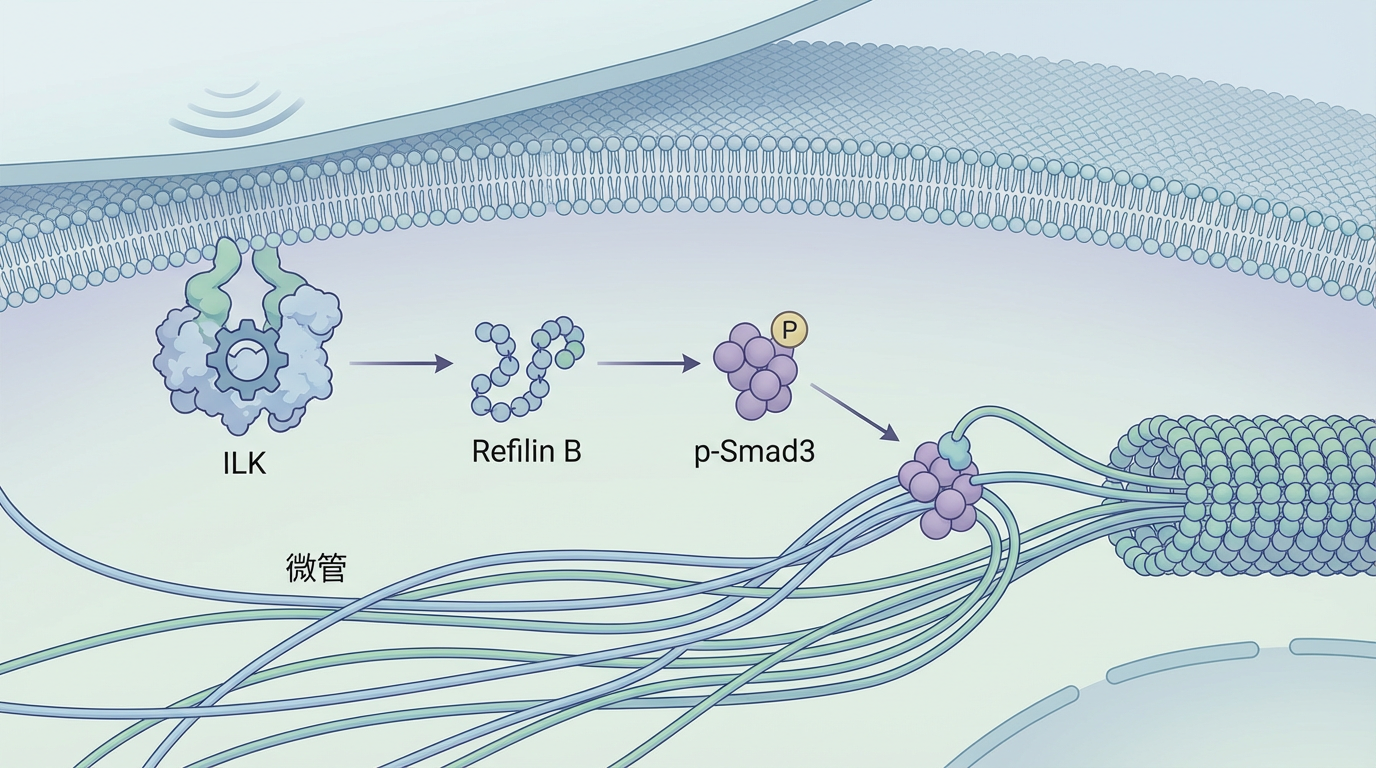
这个过程可以这样理解:
这条清晰的信号链,完美地解释了从物理感知(硬度)到化学响应(蛋白激活),再到结构重塑(微管组装)的全过程。它揭示了细胞内部一个前所未有的力学信号转导机制。
这项研究的深远意义在于,它打破了细胞骨架各组分功能独立研究的壁垒。细胞的力学响应并非单一组件的功劳,而是一场由肌动蛋白、微管、中间丝等共同参与的复杂协奏。肌动蛋白产生牵引力,像“触手”一样探索环境;而微管则根据这些信息,进行内部结构的战略性调整,尤其是在细胞分裂这种决定命运的时刻,确保一切精准无误。
这些信号最终还会通过LINC复合物等结构传递至细胞核,影响染色质的结构,从根本上改变基因的表达。这就像一个企业,外部市场环境的变化(微环境硬度),通过销售部门(肌动蛋白)和物流部门(微管)的反馈,最终影响了总部的决策(基因表达),决定了企业未来的发展方向(细胞命运)。
这一基础科学的突破,为我们理解和治疗多种疾病打开了全新的大门。
科学的每一次突破,既是答案,也是新的问题。尽管我们已经窥见了微管的力学感知秘密,但更广阔的未知领域仍在前方。
未来,借助人工智能进行复杂信号网络的模拟,结合更高分辨率的活细胞成像技术,科学家们有望构建出细胞力学响应的“数字孪生”模型,从而以前所未有的深度和速度,解码生命的力学奥秘。
这项研究不仅是细胞生物学领域的一次重要进展,更是一次深刻的哲学启示。它告诉我们,生命并非孤立于物理世界之外,恰恰相反,生命在最微观的尺度上,与环境的物理属性进行着最亲密的对话。我们对细胞的理解,正从一个“化学烧杯”演变为一个精密、智能、能够感知世界的“微型机器”。而读懂它们的语言,正是我们掌握自身健康与命运的关键一步。
点击充电,成为大圆镜下一个视频选题!