对抗知识焦虑,从看懂这条开始
App 下载
给疫苗装个“导航+引擎”,癌症免疫效果翻数倍
免疫系统激活|树突状细胞|黑色素瘤小鼠模型|癌症疫苗载体|华南理工大学|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
免疫系统激活|树突状细胞|黑色素瘤小鼠模型|癌症疫苗载体|华南理工大学|肿瘤学|医学健康
想象一下:给晚期黑色素瘤小鼠注射一针疫苗,再配合常用的免疫药物,80%的小鼠能活过100天——而且就算再给它们注射肿瘤细胞,身体也能直接把癌细胞“赶尽杀绝”。这不是科幻电影的桥段,而是华南理工大学团队在实验室里做到的事。他们没发明新的抗癌药物,只是给癌症疫苗换了个“载体”——这个载体既能精准把肿瘤抗原送到免疫细胞门口,还能直接激活免疫系统的“警报开关”。为什么一个小小的载体,能让癌症疫苗的效果发生天翻地覆的变化?
要理解这个载体的厉害,得先搞懂癌症疫苗的核心难题:它既要把肿瘤的“通缉令”(也就是抗原)送到免疫系统的“情报站”——树突状细胞(DCs)手里,又要同时给免疫系统发“警报”,让它赶紧启动免疫反应。以前的疫苗要么是“通缉令”送不到位,要么是“警报”响得不够大,结果免疫系统要么没看见敌人,要么懒得动。
这个叫Aze-Chol NP的纳米载体,相当于把“情报投递”和“警报触发”合二为一了。你可以把它想象成一个带警报器的快递盒:盒子表面的氮杂环丁烷结构就是警报器,一碰到树突状细胞表面的TLR9受体——这个专门识别外来入侵者的“警报开关”,就会立刻触发信号,让树突状细胞从“休眠状态”切换到“战斗状态”;而盒子里装的肿瘤抗原,会直接被递送到树突状细胞内部,让它赶紧把“通缉令”传达给负责杀敌的CD8+T细胞。
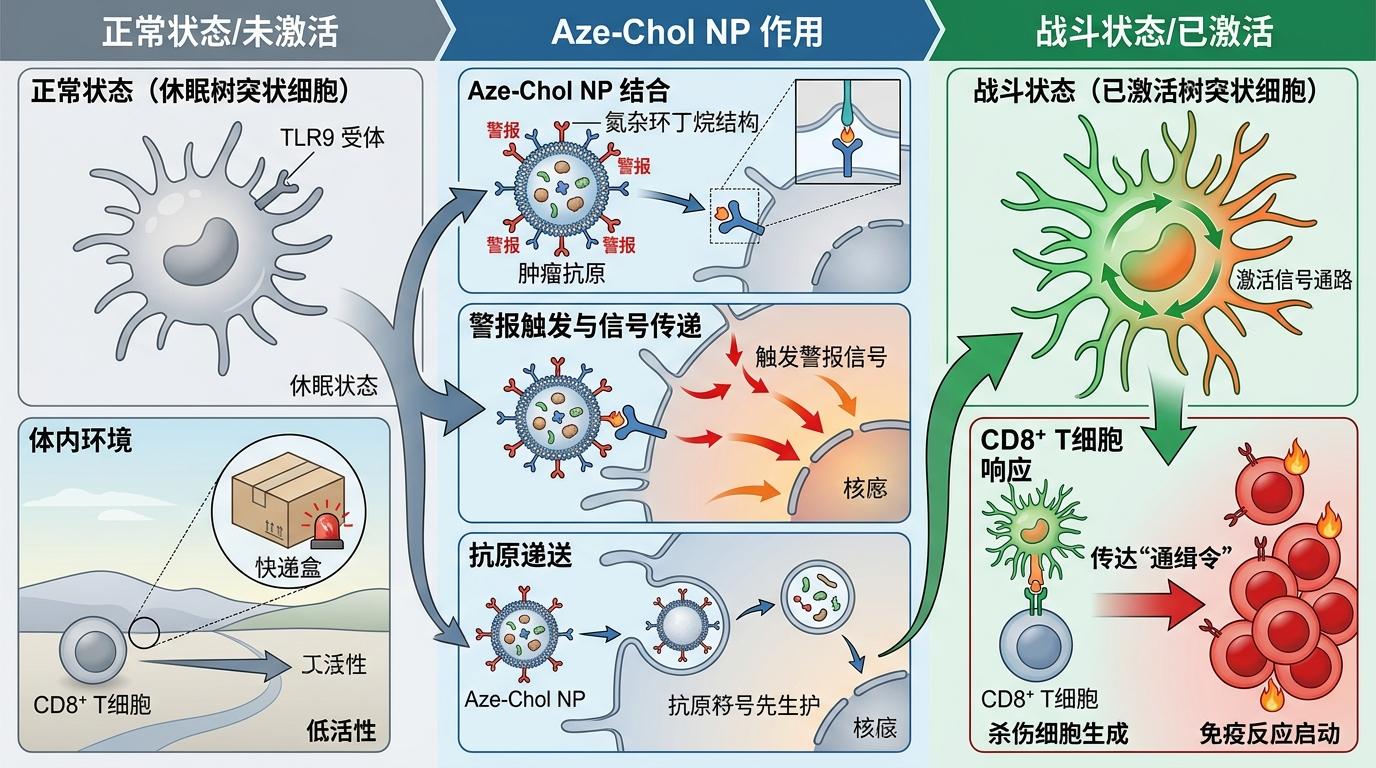
更关键的是,这个“快递盒”大小刚好在19-50纳米,能精准钻进淋巴结——那里是树突状细胞最集中的地方,不会像传统疫苗那样大部分被肝脏“截留浪费”。实验数据显示,它能让树突状细胞摄取抗原的效率提升3.5倍,还能让促炎细胞因子的分泌量最高翻488倍。
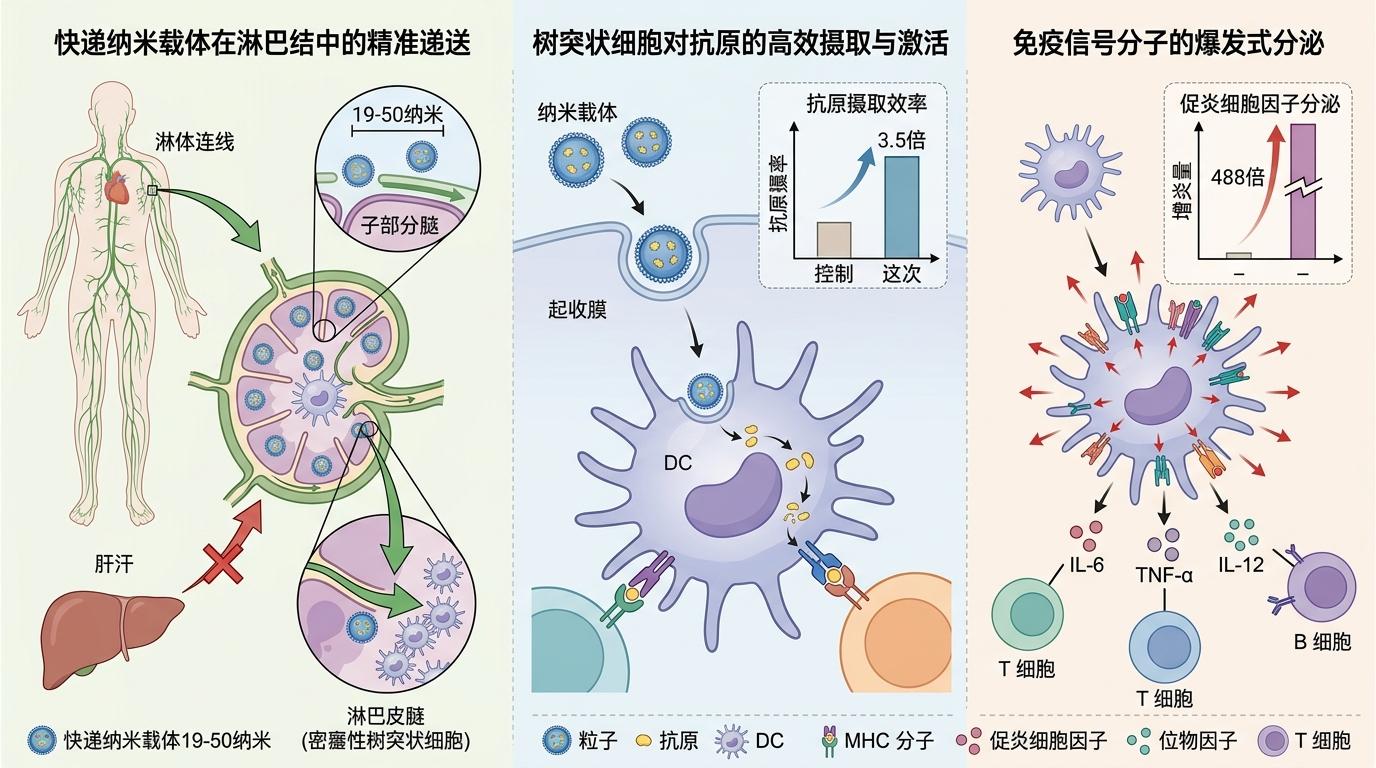
光有疫苗还不够,很多晚期肿瘤会在自己周围建一个“免疫抑制屏障”,就算T细胞接到了“通缉令”,也打不进去。这时候就得配合免疫检查点抑制剂,比如抗PD-L1抗体——它的作用就是拆掉肿瘤的“屏障”,让T细胞能顺利杀进去。
有意思的是,这个纳米疫苗和抗PD-L1抗体的组合,不是简单的“1+1=2”,而是产生了强烈的协同效应。在黑色素瘤和HPV肿瘤模型里,单独用疫苗只能延缓肿瘤生长,单独用抗体的小鼠也很难活过60天,但两者结合后,80%的小鼠活过了100天,而且体内形成了长期的免疫记忆——就算再给它们注射肿瘤细胞,也能在几天内完全清除。
这背后的逻辑很清晰:疫苗负责训练出一批精准识别肿瘤的“特种部队”CD8+T细胞,抗体负责拆掉肿瘤的“防御工事”,让T细胞能直接冲到肿瘤内部杀敌。更重要的是,这个组合还能让免疫系统记住肿瘤的特征,就算肿瘤卷土重来,也能快速反应。
当然,它也不是完美的。目前的实验都还在小鼠身上,要用到人身上,还得解决几个问题:比如怎么控制免疫激活的强度,避免过度激活导致的炎症反应;不同肿瘤的“通缉令”不一样,怎么快速定制对应的疫苗;还有大规模生产的成本和稳定性,都是需要跨越的门槛。
其实这个载体的思路,代表了癌症疫苗的一个重要转向:以前的疫苗是“抗原+佐剂”分开加,佐剂负责激活免疫,抗原负责提供靶点,但两者经常“不同步”——佐剂激活了免疫,抗原还没送过来;或者抗原送到了,佐剂的效果已经过了。
而Aze-Chol NP这种“载体即佐剂”的设计,相当于把佐剂直接做成了载体的一部分,抗原一被递送到树突状细胞,佐剂就立刻激活免疫反应,完美实现了“递送+激活”的同步。这种思路比传统的“混合佐剂”效率高得多,实验显示,它激活的抗原特异性CD8+T细胞数量,是传统CpG佐剂的3倍。
这也给癌症疫苗的未来指了个方向:与其找更强的佐剂,不如把载体和佐剂整合在一起,让疫苗的每一个部分都发挥最大作用。比如未来可以用人工智能设计更精准的载体,让它能识别不同的树突状细胞亚型,或者能根据肿瘤微环境的酸碱度自动释放抗原,进一步提升疫苗的效率。
现在的癌症免疫治疗,有点像一场现代化战争:免疫检查点抑制剂是“拆弹部队”,负责拆掉肿瘤的防御;CAR-T是“特种部队”,直接冲进肿瘤内部杀敌;而癌症疫苗,就是“军事院校”,负责训练出一批能精准识别敌人的士兵。
Aze-Chol NP的意义,不是发明了新的“士兵”,而是给“军事院校”修了一条直达“战场”的高速路,还装了个能立刻吹响集结号的警报器。它让癌症疫苗从“纸上谈兵”真正变成了“能打胜仗”的武器。
精准递送+同步激活,才是癌症疫苗的破局关键。 未来,随着载体技术的不断优化,也许我们能给每个癌症患者定制出专属的疫苗,让免疫系统变成一个永远在线的“肿瘤监控器”,真正实现“一次接种,终身防护”。