内容由AI生成,思考得你完成
App 下载
内容由AI生成,思考得你完成
App 下载
当一位糖尿病患者躺在手术台上,医生植入的钛合金支架不仅要撑住骨骼,还要扛住比普通人高3倍的感染风险——高血糖会拖垮免疫防线,让细菌在植入物表面筑成难以攻破的生物膜,传统抗生素要么杀不死菌,要么连带着伤了正常细胞。更棘手的是,涂在支架表面的抗菌药,往往在植入时的摩擦里就掉了大半,等不到感染高发期就失效。
重庆医科大学的团队给这个死局开了个新方子:他们把二维的药物涂层,变成了三维的「药物仓库」,不仅能装下更多药,还能精准只杀细菌、不伤宿主细胞,甚至在比格犬的临床级模型里验证了效果。这到底是怎么做到的?
你可以把传统植入物的抗菌设计想象成在手机背面贴个退热贴——面积有限,一蹭就掉,药效撑不了多久。重庆医科大学的团队彻底换了思路:他们用3D打印做出了仿骨小梁结构的多孔钛支架,就像一块布满微小蜂窝的海绵,再在蜂窝内壁刻出纳米级的凹凸纹路——这就是「体积工程三维药物储库」,把原本只有表面的药物承载空间,拓展到了整个支架的立体结构里。
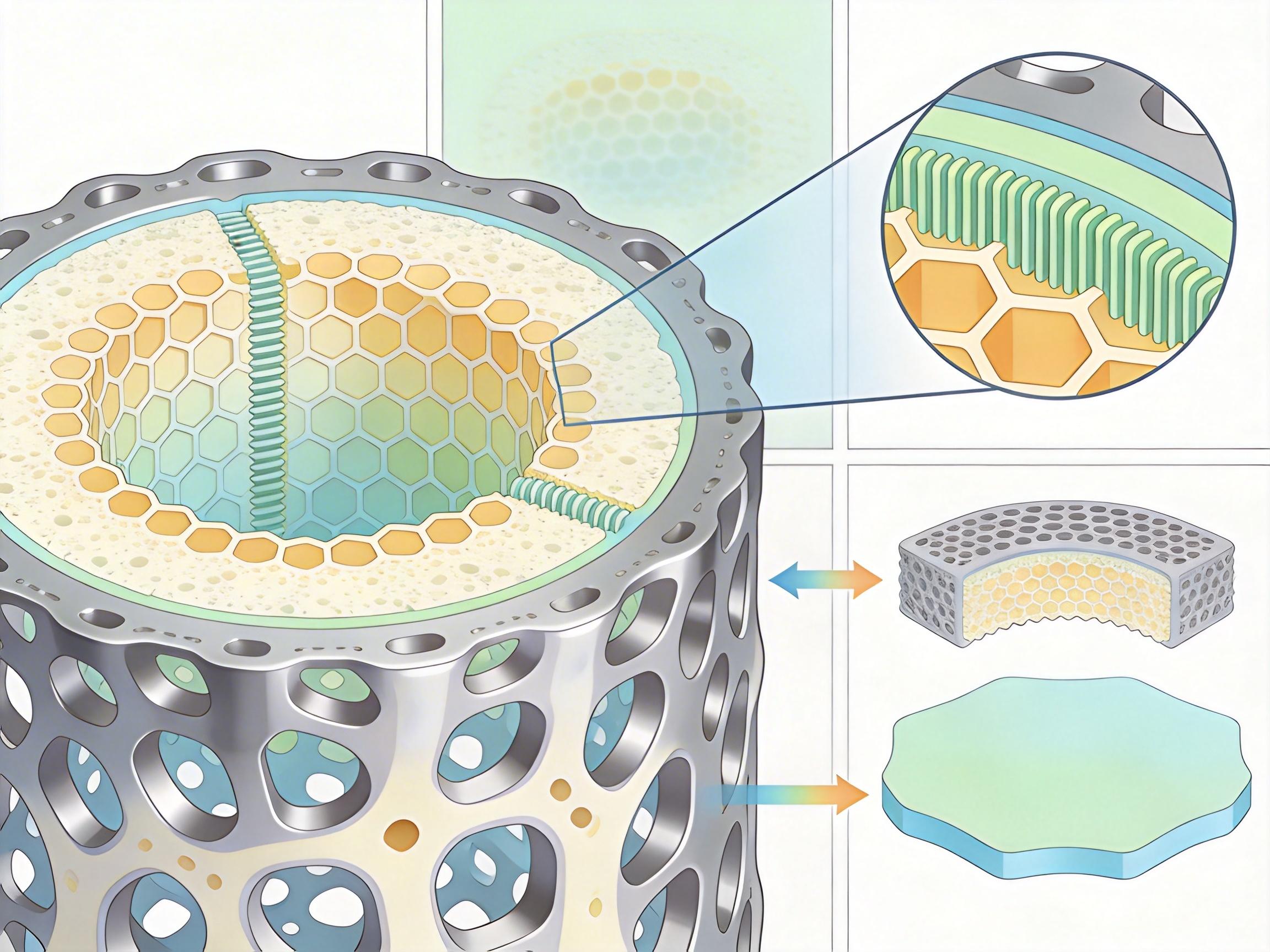
数据最能说明问题:这种多孔结构让支架的比表面积提升了3.57倍,相当于把一张A4纸折成了立体纸雕,能装下的药物量翻了好几倍。更关键的是,药物被藏在了孔壁内侧,植入时的摩擦碰不到这些「仓库」,体外摩擦测试显示,它的药物留存率是传统平面涂层的8倍以上,能稳稳覆盖感染急性期和慢性愈合期的全程需求。
简单说:以前是给支架「刷外墙」,现在是给支架「建内库」——不仅装得多,还不容易丢。
解决了药物储存的问题,下一个难题是:怎么让药物只杀细菌、不伤正常细胞?团队设计了一套「双管齐下」的机制——一边诱导细菌「铜死亡」,一边给宿主细胞「装防护盾」。
先说杀细菌的部分:他们在药物仓库里装了铜掺杂碳量子点、聚多巴胺和葡萄糖氧化酶。聚多巴胺就像个「加热开关」,近红外光一照就能局部升温,把细菌的细胞膜「烫」出缝隙;铜离子趁机钻进细菌体内,专门破坏它们的能量代谢核心——三羧酸循环,就像掐断了细菌的供电系统,让它们发生类似「铜死亡」的代谢崩溃。更巧妙的是,支架表面的苯硼酸基团还能像磁铁一样抓住细菌,让杀菌效率再翻一倍。
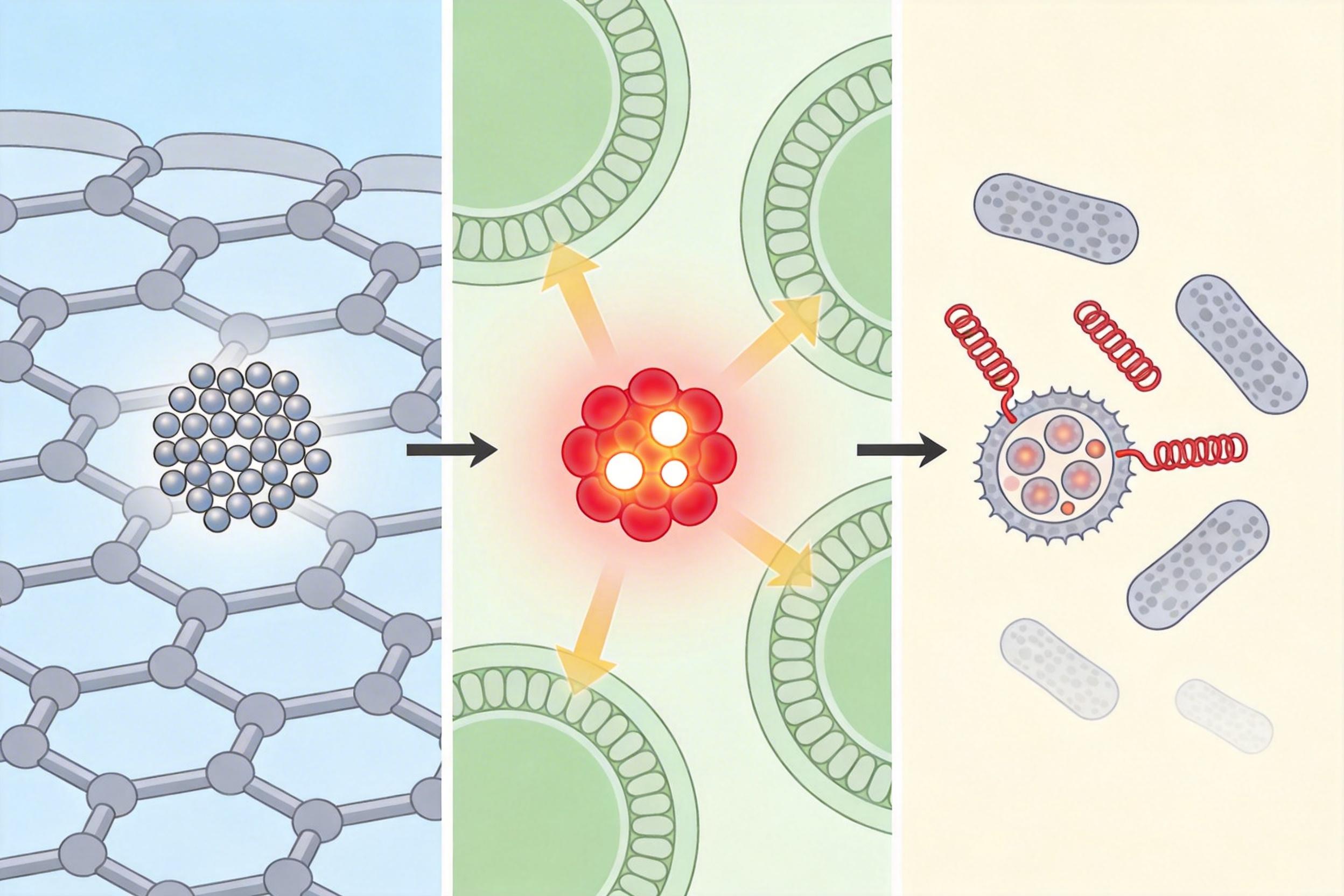
然后是保护宿主细胞的「饥饿策略」:葡萄糖氧化酶会消耗局部的葡萄糖,营造出一个「低糖饥饿环境」,这个信号会激活宿主巨噬细胞的AMPK–SIRT1通路——相当于给细胞的线粒体装了个「稳定器」,既能修复受损的线粒体,又能增强细胞的抗氧化能力,让铜离子对正常细胞的毒性降低了70%以上。
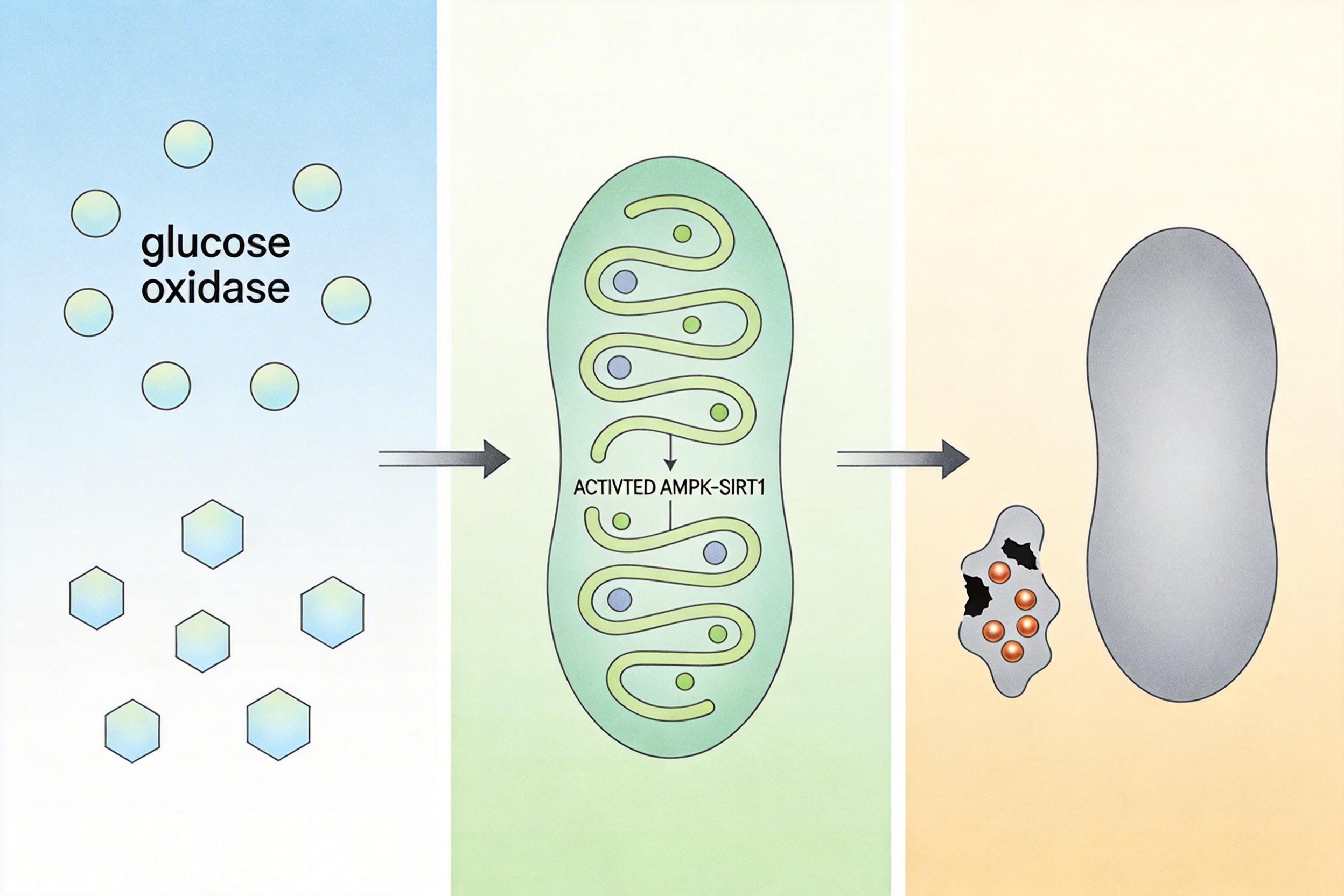
直给的逻辑链:
团队在比格犬的临床级种植体模型里做了验证:植入这种带3D药库的支架后,比格犬的感染率从80%降到了10%,新生骨量是传统支架的2.3倍——这意味着它已经具备了临床转化的潜力。
但我认为,这项研究真正的价值,不止是解决了糖尿病植入物感染的问题,更是提出了一种「维度升级」的设计思路:从二维表面到三维体积,从单一抗菌到双向调控,它打破了「抗菌必然伤细胞」的固有认知。当然,它也还有待解决的问题:比如长期植入后的药物代谢路径、不同细菌的耐药性应对,以及大规模生产的成本控制。
不过可以确定的是,这种「立体储库+精准调控」的模式,给植入物抗感染设计打开了新方向——未来的植入物,可能不再是一个冷冰冰的金属支架,而是一个能智能识别敌我的「微型治疗站」。
当我们谈论精准医疗时,往往聚焦于基因检测、靶向药物这些「高大上」的技术,但重庆医科大学的这项研究告诉我们:有时候,换个维度思考问题——比如把二维涂层变成三维仓库,就能给一个临床难题带来突破性的解法。
给植入物建个3D药库,杀得死菌,护得住人。 这句话或许能概括这项研究的核心:医学的进步,从来都不是只追求更复杂的技术,而是在每一个细节里,找到更精准的平衡——平衡杀菌与护胞,平衡短期疗效与长期安全,平衡技术创新与临床实用。
未来,当糖尿病患者再接受植入手术时,他们不用再担心感染的阴影,因为那个小小的3D药库,会在他们体内默默守护,一边杀敌,一边疗伤。