对抗知识焦虑,从看懂这条开始
App 下载
胃癌检测惊现巨大差异,精准治疗基石何在?
免疫疗法|靶向药物|PD-L1|HER2|胃癌分子检测|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
免疫疗法|靶向药物|PD-L1|HER2|胃癌分子检测|肿瘤学|医学健康
在现代肿瘤治疗的战场上,每一位胃癌患者的体内都隐藏着一张特殊的“通行证”。这张通行证上印刻着独特的分子密码,例如HER2和PD-L1。读懂这些密码,医生就能为患者匹配上精准的靶向药物或免疫疗法,如同用正确的钥匙打开一扇通往“生门”的窄门。然而,如果这张通行证的读取过程出现偏差,甚至被误读,那么患者不仅可能错失最佳治疗时机,还可能被引导至一条无效甚至有害的治疗路径。这并非危言耸-听,而是一项最新研究敲响的警钟。
近期,一项发表于国际权威期刊《Gastric Cancer》的研究,对日本全国306家医疗机构的胃癌分子检测现状进行了一次“摸底考试”,结果令人震惊。这项覆盖了2022至2023年数据的调查显示,不同医院对同一种疾病的“通行证”解读能力,存在着天壤之别。
数据显示,在判断HER2是否为强阳性(IHC 3+,意味着患者可从靶向治疗中显著获益)时,各家机构给出的阳性率竟在 0% 到 61% 之间剧烈波动。同样,在评估PD-L1表达水平(CPS≥5,是免疫治疗获益的重要指标)时,不同机构的阳性率更是从 0% 横跨至 100%。这意味着,同一位患者,仅仅因为检测地点的不同,其命运可能被完全改写。
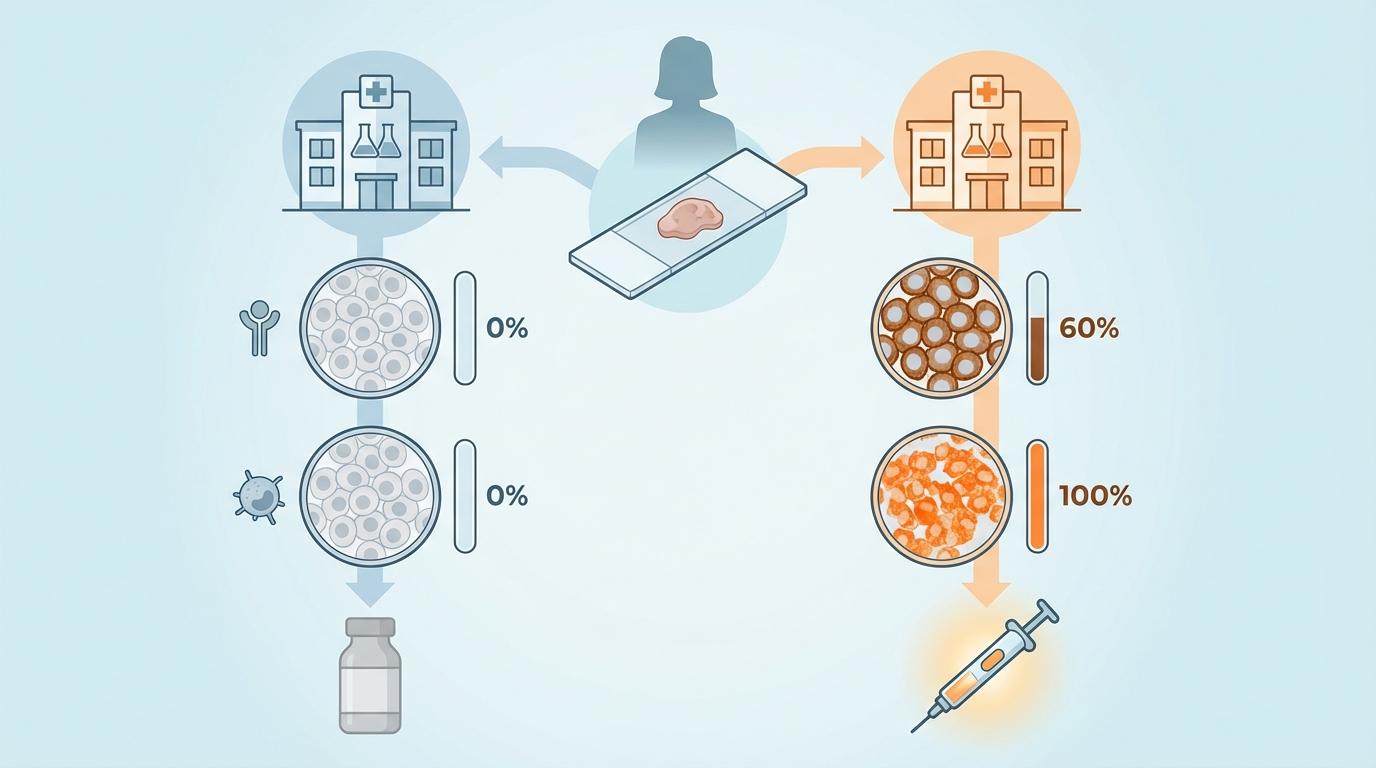
这份报告如同一面镜子,映照出全球胃癌精准诊疗背后一个深刻的困境:在我们追求更新、更强的治疗药物时,作为一切精准治疗起点的病理检测,其流程的标准化程度,远未跟上药物研发的步伐。这座精准医疗大厦的基石,正因标准不一而出现裂痕。
为何会出现如此惊人的差异?研究将矛头指向了从样本离体到报告出具的全流程,揭示了一条环环相扣的“失误链”。
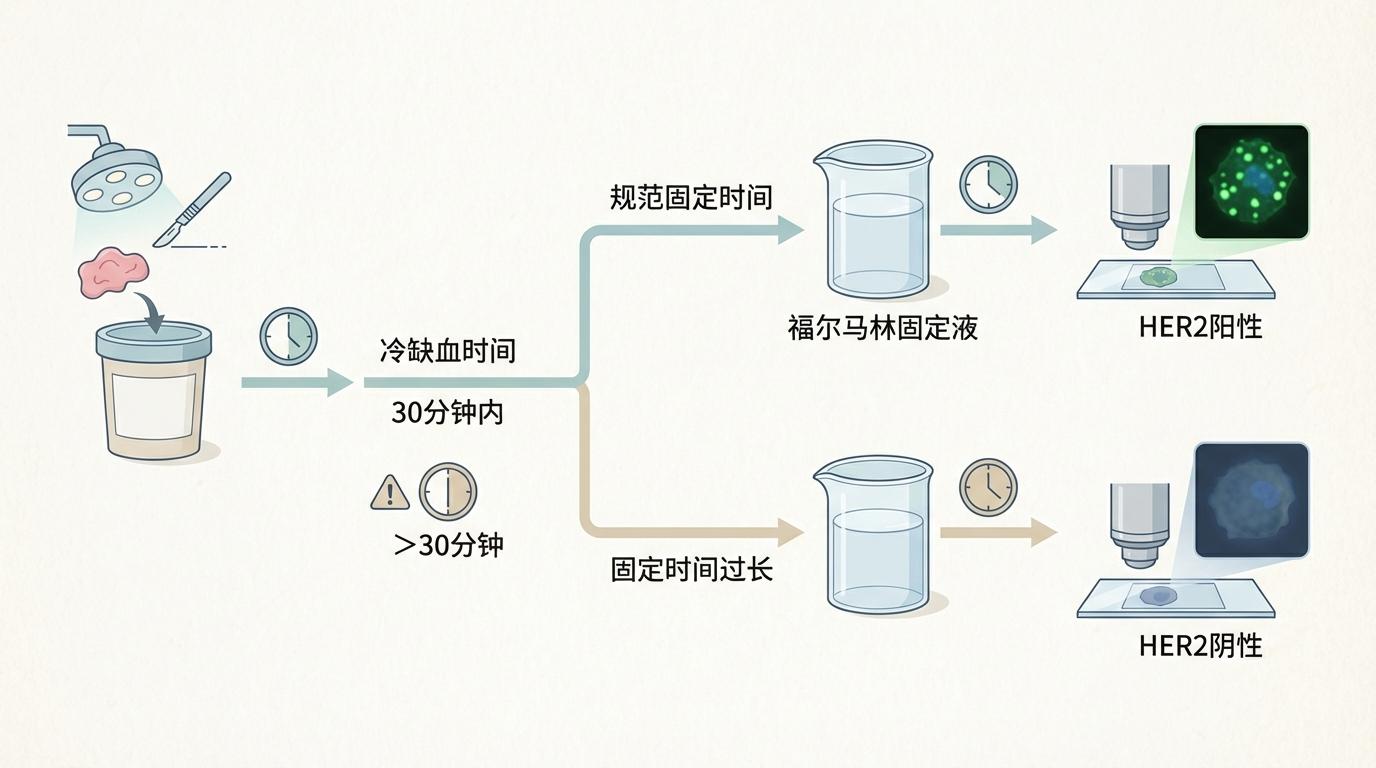
分析阶段:试剂与机器的“罗生门” 进入实验室,不同的检测试剂盒如同不同品牌的“解码器”。调查显示,70%的机构使用罗氏的试剂盒,15%使用安捷伦的,其余则五花八门。虽然主流试剂盒性能优异,但不同产品间的细微差异,加上各实验室操作流程的不统一,可能导致染色结果的深浅浓淡出现偏差,为后续判读埋下隐患。
分析后阶段:病理医生的“一念之间” 最后一道关卡,掌握在病理医生的显微镜下。免疫组化(IHC)染色并非简单的“非黑即白”,尤其是在界限模糊的病例中,对染色强度(如HER2的1+、2+)和阳性细胞比例(如PD-L1的CPS评分)的判断,考验着医生的经验和眼力。这种主观性,正是导致机构间差异的最后一个,也是最关键的因素。没有统一、严格的培训和质控,两位经验丰富的医生对同一张切片,也可能得出截然不同的结论。
诊断的失准,意味着精准治疗的落空。面对这一严峻现实,唯一的出路在于建立并执行覆盖全流程的标准化操作规范(SOP)。这不仅是技术问题,更是关乎医疗质量和患者生命的系统工程。
幸运的是,无论是国际还是国内,对这一问题的重视程度正与日俱增。从美国病理学家协会(CAP)到中国的各类专家共识,都在不遗余力地推动检测流程的规范化。例如,《胃癌Claudin18.2临床检测专家共识(2025版)》等文件的出台,正是为了给新兴靶点的检测“立规矩”,避免重蹈覆辙。“中国胃癌MDT精准诊疗高质量发展专项行动”等项目的启动,也旨在将标准化的理念传递到“最后一公里”。
展望未来,填补“诊断鸿沟”不仅依赖于人的努力,更需要技术的加持。
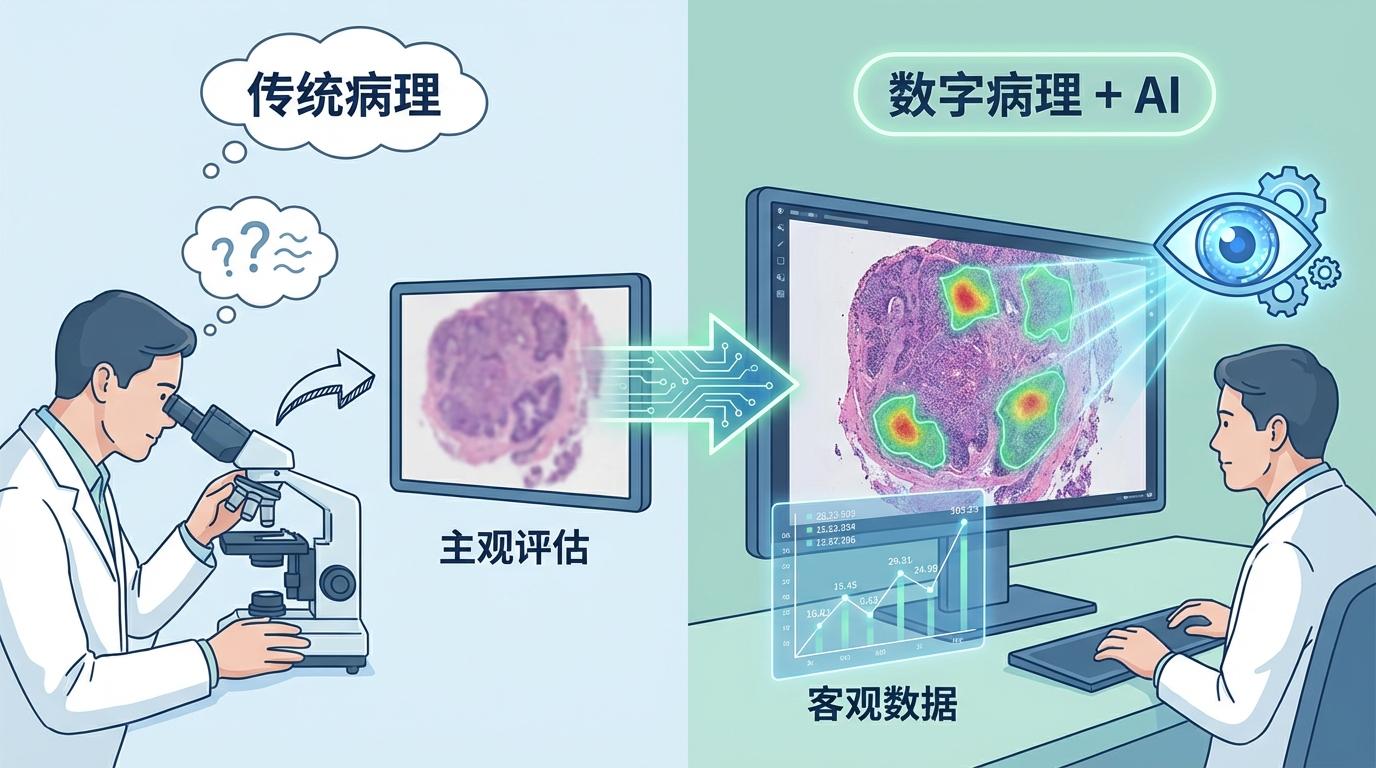
结语
日本的这项全国性调查,为全球胃癌精准治疗领域敲响了警钟。它告诉我们,通往治愈的道路上,不仅需要仰望星空,追逐前沿的药物创新,更需要脚踏实地,夯实每一个看似平凡的诊断细节。因为,只有当每一份病理报告都无限接近真相,我们手中的“神药”才能精准地找到它的目标。标准化,正是这份精准的承诺,是连接科学突破与患者生命的坚固桥梁。