对抗知识焦虑,从看懂这条开始
App 下载
BRCA2突变藏耐药暗门,提前预判换治疗方案
耐药机制|RB1基因|CDK4/6抑制剂|乳腺癌患者|BRCA2突变|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
耐药机制|RB1基因|CDK4/6抑制剂|乳腺癌患者|BRCA2突变|肿瘤学|医学健康
当安吉丽娜·朱莉因BRCA2突变切除乳腺时,全世界只记住了这个基因是“乳腺癌导火索”。但很少有人知道,它还藏着另一个更棘手的秘密——让10%的乳腺癌患者刚用上标准治疗就失效。
每年230万乳腺癌患者里,70%是激素受体阳性型,CDK4/6抑制剂联合内分泌治疗是他们的“救命药”。但总有10%的人,肿瘤像提前读过治疗剧本,早早卸掉了药物的“刹车装置”RB1基因,让治疗彻底失灵。直到2026年《自然》杂志的一篇论文,才把这层窗户纸捅破:这10%的患者,大多天生带着BRCA2突变。为什么BRCA2突变会和耐药绑定?这背后藏着肿瘤的双重诡计。
你可以把RB1基因想象成细胞的“刹车踏板”,正常细胞里有两个备份——就像汽车的左右刹车,坏了一个还有另一个。但BRCA2突变的肿瘤细胞,从诞生起就少了一个RB1备份,医学上叫“半合子状态”。这相当于出厂时就少装了一个刹车,肿瘤的“进化门槛”直接被踩低。
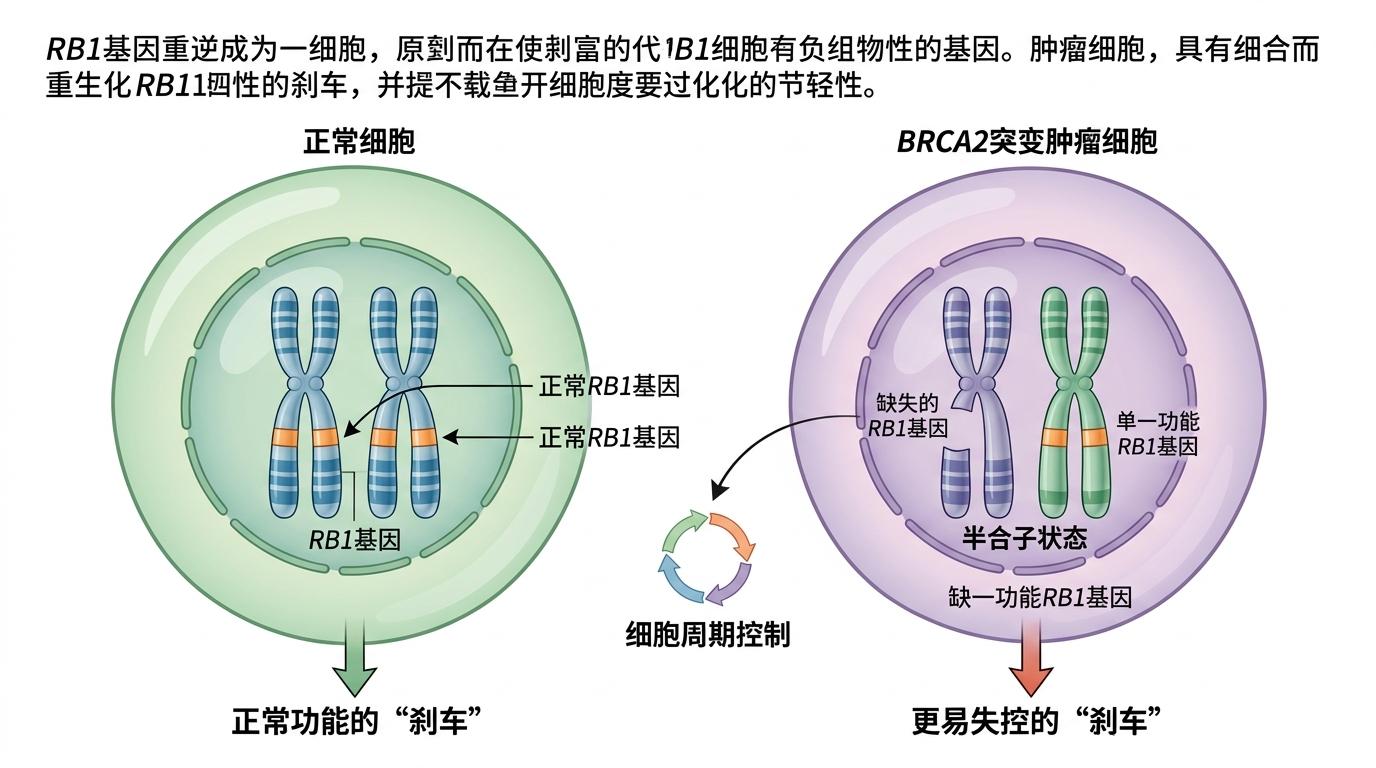
这只是第一步。BRCA2的本职工作是帮细胞精准修复DNA损伤,一旦它突变失效,细胞就只能用错误率极高的“野路子”修DNA——这就是“同源重组缺陷(HRD)”。当CDK4/6抑制剂开始施压,仅剩的那个RB1备份,会在这种混乱的DNA修复中更容易被彻底破坏。
两个机制叠加,就像单边刹车的汽车开在布满坑洼的路上——失控只是时间问题。纪念斯隆凯特琳癌症中心的团队分析了5800多份患者数据后发现:BRCA2突变患者的肿瘤,丢失RB1的概率是普通患者的5倍。
过去,医生只能等患者治疗无效后再换方案,但这次的研究,第一次让“预判耐药”成为可能。
团队用患者来源的肿瘤异种移植模型验证:BRCA2突变的肿瘤对CDK4/6抑制剂确实反应极差,反而对PARP抑制剂的敏感度极高。PARP抑制剂的原理恰好针对BRCA2突变导致的HRD——就像给DNA修复的“野路子”再上一把锁,让肿瘤细胞的DNA损伤彻底无法修复,最终死亡。
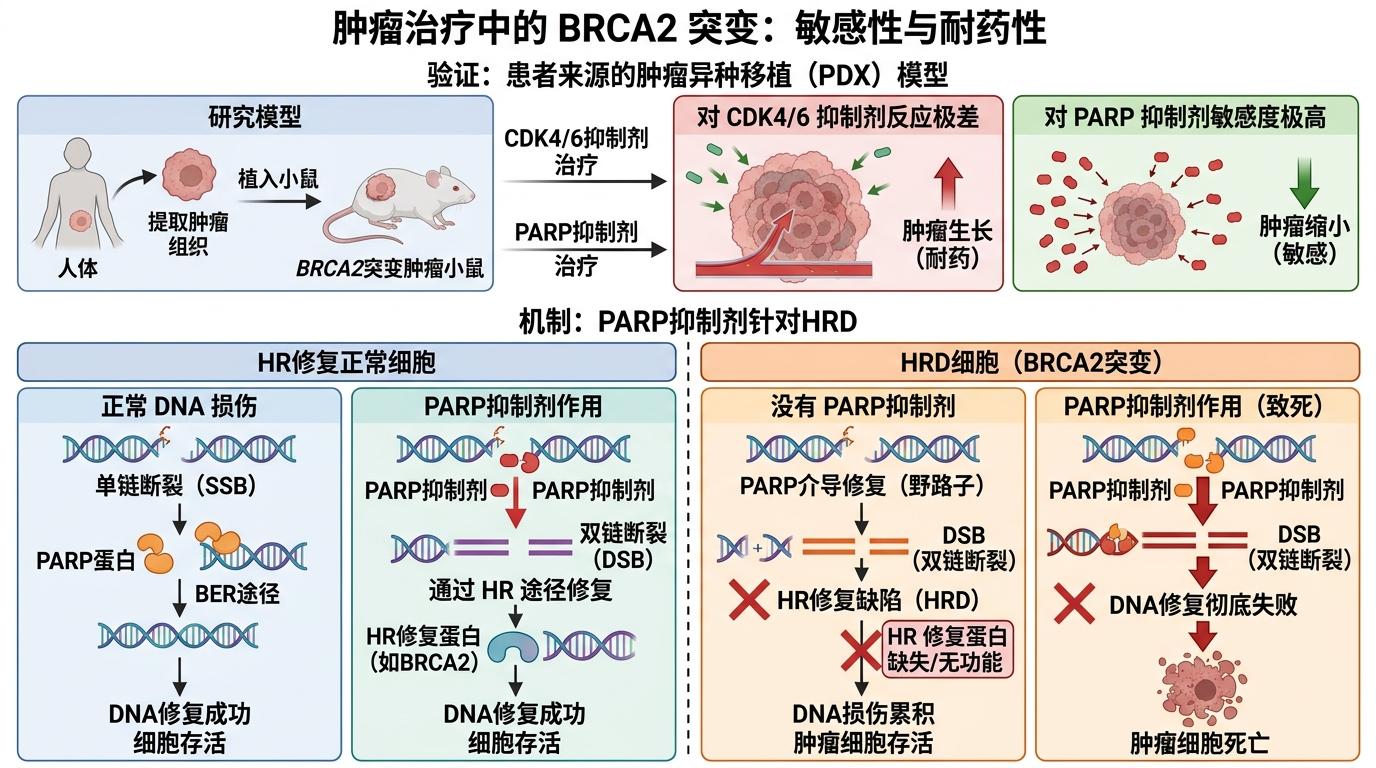
更有意思的是,部分肿瘤在PARP抑制剂治疗后,会出现“回复突变”——重新找回精准修复DNA的能力。这时,原本失效的CDK4/6抑制剂反而可能重新起效。这意味着“先PARP后CDK4/6”的序贯治疗,能把两种药物的价值最大化。
基于这个发现,全球III期临床试验EvoPAR-Breast01已经启动,直接对比PARP抑制剂联合内分泌治疗,和传统CDK4/6抑制剂方案的疗效。如果试验成功,BRCA2突变的乳腺癌患者,从治疗第一天起就能用上最适合的药。
更值得关注的是,这项研究的意义远不止BRCA2突变本身。
团队发现,RB1半合子状态在所有激素受体阳性乳腺癌中占比近50%——也就是说,近一半的患者,从一开始就带着耐药的“潜在开关”。只是BRCA2突变的患者,按下这个开关的概率更高。这意味着,未来或许能通过检测RB1的拷贝数状态,提前预判更多患者的耐药风险。
当然,这项研究也有局限:目前的结论只针对激素受体阳性的乳腺癌患者,是否适用于三阴性等其他亚型,还需要更多数据验证。而且PARP抑制剂的高昂价格,也可能让很多患者望而却步——精准医疗的可及性,始终是绕不开的问题。
从BRCA2突变增加患癌风险,到发现它影响治疗效果,医学对这个基因的认知,走了二十多年。而这次的研究,最珍贵的不是找到了一种新的治疗方案,而是让我们第一次看到:肿瘤的耐药不是随机发生的,它有迹可循,甚至可以提前预判。
“预判比治疗更重要”——这句话正在从实验室走向临床。未来的癌症治疗,或许不再是医生和肿瘤的“事后博弈”,而是一场提前布局的精准对决。当我们能在肿瘤出招前就看清它的路数,胜利的天平,才会真正向患者倾斜。