对抗知识焦虑,从看懂这条开始
App 下载
细胞炎症秘密通道:高尔基体竟操纵免疫反应?
Autophagy期刊|李民教授团队|蛋白质分泌通路|白细胞介素-1β|高尔基体|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
Autophagy期刊|李民教授团队|蛋白质分泌通路|白细胞介素-1β|高尔基体|分子细胞生物学|生命科学
在每一个细胞构成的微观都市里,蛋白质如同货物,被精准地生产、包装,并运送到指定地点。长久以来,我们认为这条物流网络井然有序,由内质网工厂生产,高尔基体这一“中央邮局”分拣打包,再通过既定路线“出港”。然而,对于一些没有“邮寄标签”(信号肽)的特殊货物,比如强大的炎症信使——白细胞介素-1β(IL-1β),它们如何被送出细胞,一直是个谜。它们的存在,仿佛暗示着这座城市里,存在着不为人知的秘密通道。
就在不久前,这个谜团被揭开了惊人的一角。中山大学的李民教授团队在国际权威期刊《Autophagy》上发表了一项突破性研究,颠覆了我们对细胞内蛋白质运输和免疫调控的传统认知。他们发现,细胞的“中央邮局”——高尔基体,不仅仅是分拣中心,它本身竟能开辟一条秘密的“出口通道”,专门用于运输IL-1β这类炎症因子。
这项于2025年12月8日在线发表的研究,精准地描绘了这一过程:
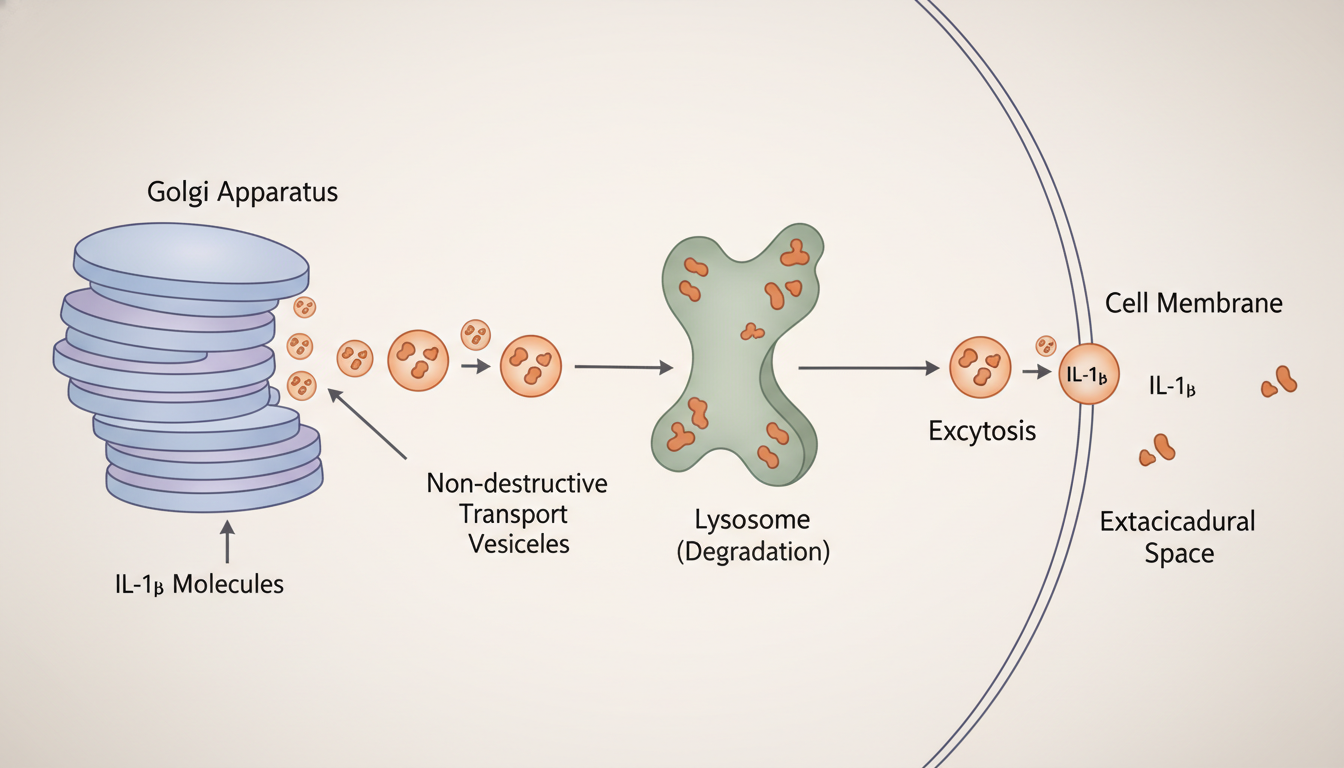
这一发现,如同一张新绘制的地图,首次清晰地将高尔基体、非经典自噬与炎症因子的分泌直接联系起来,揭示了细胞免疫调控的一条全新路径。
要理解这一发现的深刻意义,我们必须重新认识“自噬”这个概念。
自噬(Autophagy),源于希腊语,意为“自我吞噬”。它通常被描绘成细胞的“清洁工”和“回收中心”。在经典自噬中,细胞会形成一个双层膜的“垃圾袋”(自噬体),包裹住老化、受损的蛋白质或细胞器,然后送往“焚化炉”(溶酶体)进行降解,实现资源回收再利用。
然而,生命远比教科书复杂。近年来,科学家们发现了非经典自噬(NCA)。它像是自噬家族中的“多面手”,并不总是以降解为目的。它借用一部分自噬机器,但往往只形成单层膜结构,执行着更加多样化的任务,比如抵御入侵的病原体、参与膜修复,以及如今我们看到的——调控蛋白质的“非主流”分泌。
李民教授团队的发现,正是非经典自噬功能多样性的有力证明。他们发现,在高尔基体这个细胞的交通枢纽上,一种特殊的质子泵(V-ATPase)能够组装起来,像一个“信号塔”,吸引并激活了自噬关键蛋白ATG16L1。值得注意的是,ATG16L1蛋白的特定区域(WD40结构域)在多种非经典自噬中都扮演着关键角色,这暗示它可能是启动这类特殊任务的“通用开关”。一旦这个开关被打开,LC3蛋白(自噬过程的标志性分子)就会被招募并“脂化”,附着在高尔基体来源的膜上,形成运输IL-1β的“囊泡快艇”,最终将其送出细胞。
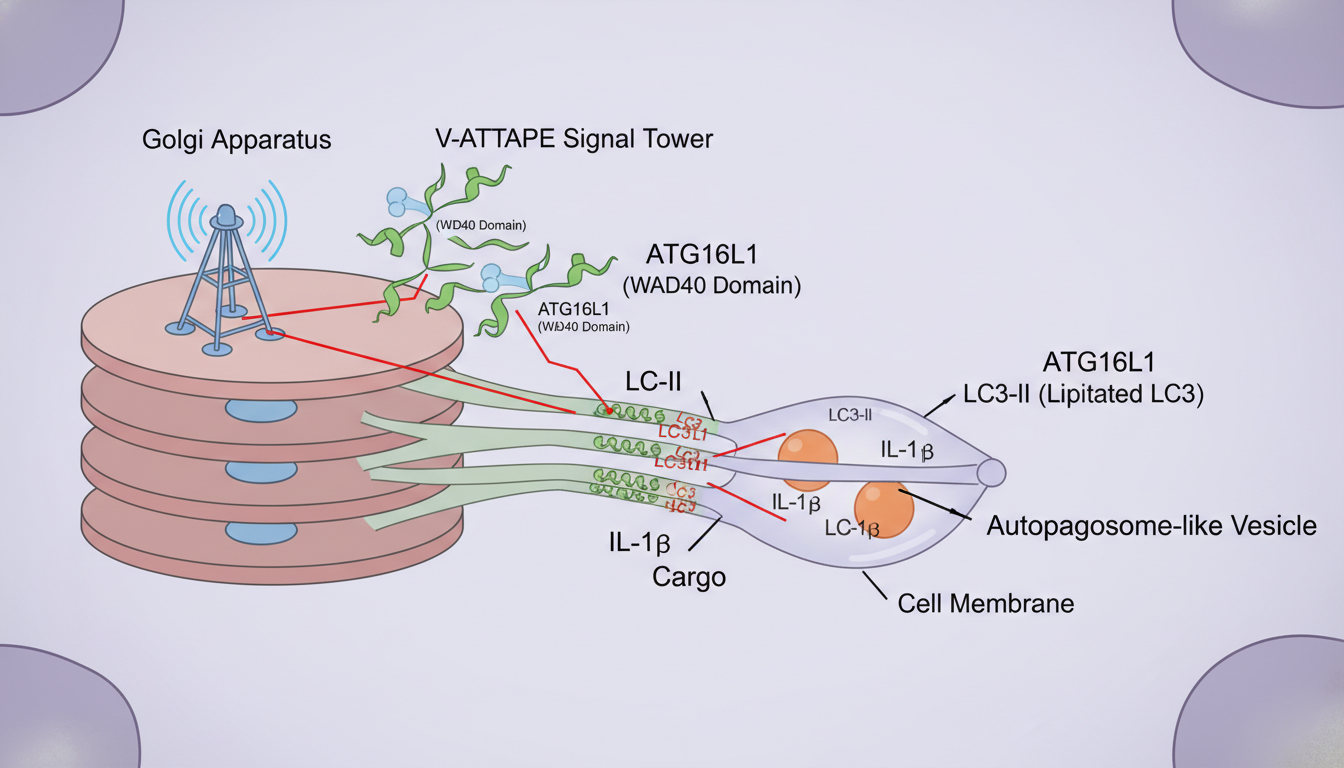
这一发现极大地拓展了我们对高尔基体的认知。它不再仅仅是蛋白质经典分泌途径上的一个被动站点,而是一个能够主动感知信号、启动特定运输通路、直接参与免疫调控的“智能哨所”。
在此之前,科学家们已经知道,V-ATPase-ATG16L1轴在细胞对抗细菌入侵的“异源自噬”中发挥作用,它能感知到被细菌破坏的囊泡,并启动自噬进行清除。而李民团队的研究表明,同样的分子机器,在不同的细胞“地点”(高尔基体),可以被赋予全新的“使命”(分泌炎症因子)。
这揭示了细胞运作的一个核心原则:模块化和情景依赖性。细胞并不会为每个功能都设计一套全新的工具,而是像乐高积木一样,将有限的分子模块(如V-ATPase-ATG16L1轴)在不同的时间、地点进行重组,以应对千变万化的内外环境信号。这不仅高效,而且极具适应性。
IL-1β是一种强大的促炎细胞因子,它像一把双刃剑。在正常情况下,它是身体抵抗感染和损伤的“战斗号角”;但如果失控,它就会引发剧烈的炎症风暴,导致关节炎、痛风、动脉粥样硬化甚至某些癌症等多种疾病。
目前,临床上针对IL-1β的药物,大多是直接中和它或其受体,这相当于在战场上全面“禁言”,可能会影响正常的免疫防御。而新发现的这条高尔基体分泌通路,为我们提供了全新的干预思路。
这项开创性的工作也留下了一系列引人深思的问题,为未来的研究指明了方向:
细胞这座微型城市的复杂与精妙,远超我们的想象。每一次深入探索,都像是在熟悉的街区发现了一条隐藏的小巷,通往一个全新的世界。从高尔基体出发的这条秘密运输线,不仅重塑了我们对细胞内部运作的理解,更可能为人类对抗炎症性疾病,提供一把前所未有的精准钥匙。