内容由AI生成,思考得你完成
App 下载
内容由AI生成,思考得你完成
App 下载
当你被病毒入侵时,淋巴结里正上演一场精密的招募战——CD8 T细胞,也就是我们常说的“杀手T细胞”,会被树突状细胞唤醒,变身能精准猎杀感染细胞的战士。过去科学家一直以为,这场唤醒是一次性的:树突状细胞和T细胞绑定24小时,完成激活后T细胞就独自出发增殖分化。但2025年马克斯·普朗克研究所的团队用活体显微镜盯着淋巴结看了数小时后,发现了一个被忽略的秘密:唤醒不是一锤子买卖,那些真正能打高亲和力T细胞,还会回来接受第二次“特训”。为什么只有它们能获得二次机会?这背后的机制,可能改写疫苗和免疫疗法的思路。
你可以把初始激活阶段看作T细胞的“入伍体检”——淋巴结里,树突状细胞像招兵官,拿着抗原“通缉令”,和路过的T细胞挨个配对。只要T细胞的受体能认出抗原,再加上共刺激信号和细胞因子的“盖章”,就算通过体检,能脱离树突状细胞开始迁移。这一阶段持续约24小时,所有能识别抗原的T细胞都能拿到“入伍通知书”,不管它们的受体和抗原结合得牢不牢。
但自然的筛选远不止于此。
那些受体和抗原结合力强的高亲和力T细胞,会在激活后表达一种叫CXCR3的趋化因子受体——相当于拿到了一张“特训营通行证”。它们会重新回到淋巴结的亚滤泡微环境,再次和树突状细胞绑定数小时,接受第二次激活。而低亲和力的T细胞,就只能停留在第一阶段,后续增殖和分化的潜力都远不如前者。
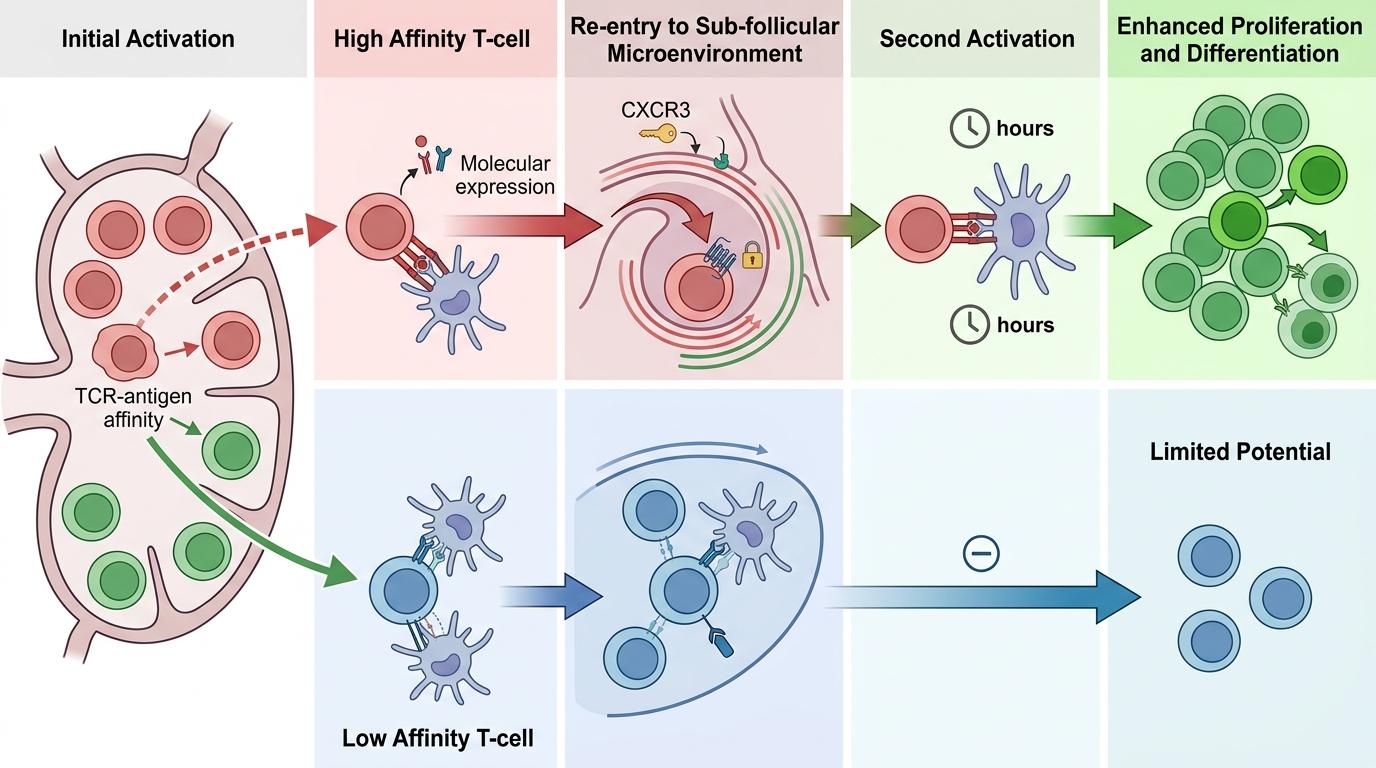
这不是科学家的推测,而是用活体显微镜拍下来的事实:高亲和力T细胞像收到召回指令的士兵,精准回到指定区域,而低亲和力的同类则在淋巴结里漫无目的地游走。
第二次激活的关键,是一种叫白细胞介素-2(IL-2)的信号分子——你可以把它看作T细胞增殖分化的“能量包”。但这个能量包不是随便就能拿到的,它需要CD4辅助T细胞的“闪电投递”。
研究人员观察到,CD4辅助T细胞会在CD8 T细胞和树突状细胞绑定的区域短暂停留,放下IL-2就立刻转移到下一个树突状细胞,像战场上骑着摩托车送弹药的通讯员,绝不恋战。而CD8 T细胞只有在和树突状细胞稳定结合的状态下,才能高效接住这些IL-2信号,表现为STAT5磷酸化水平显著升高——这是T细胞开始快速增殖的明确标志。
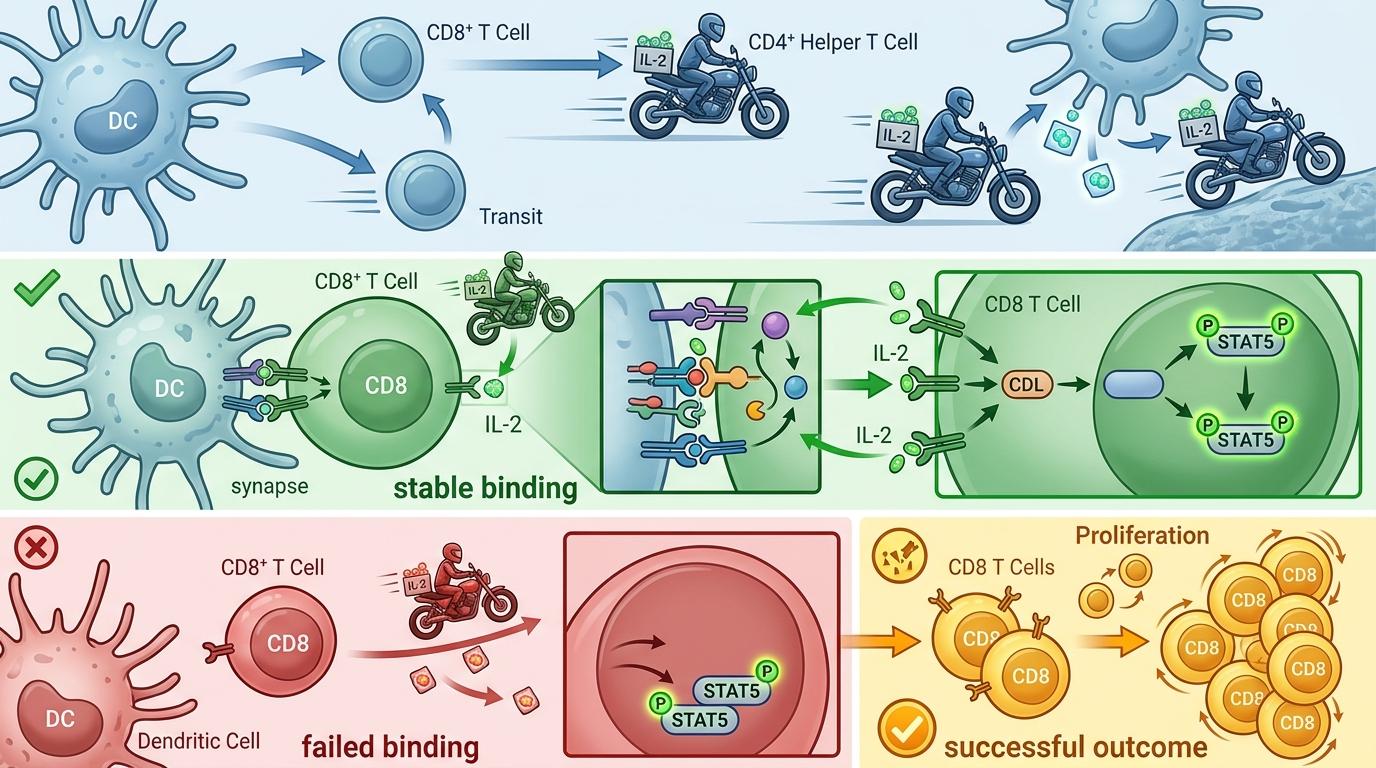
更巧妙的是调节性T细胞的“动态管控”:它们不会在任何一个细胞群里停留,而是像巡逻兵一样在细胞间穿梭,通过竞争性吸收IL-2,避免T细胞过度激活导致自身免疫损伤。这种精密的平衡,让只有最需要能量的高亲和力T细胞,能拿到足够的IL-2完成扩增。
这里的核心是“旁分泌”——信号不是由细胞自己产生给自己,而是由相邻的细胞精准递送到需要的位置,这比T细胞自分泌IL-2的效率高得多,也更能保证资源向最有效的战士倾斜。
这个发现最直接的意义,落在了疫苗和细胞免疫疗法上。
过去的疫苗设计,大多只关注如何让更多T细胞完成初始激活,但根据双阶段机制,真正决定免疫效果的是能进入第二阶段的高亲和力T细胞。如果能通过疫苗配方的调整,比如优化抗原递呈方式,或者增强CXCR3的表达,就能引导更多高亲和力T细胞进入特训营,这样疫苗诱导的免疫反应会更强,持续时间也会更久。
在CAR-T细胞疗法中,这个机制也提供了新的优化方向:现在的CAR-T细胞往往是在体外激活后直接回输,但如果能在回输前让它们表达CXCR3,或者在体内模拟淋巴结的亚滤泡微环境,帮助它们完成第二次激活,就能提升CAR-T细胞的增殖能力和杀伤效率,尤其是针对实体瘤的治疗。
当然,这个机制也有尚未解开的谜题:比如CXCR3的表达是如何被高亲和力TCR信号调控的?调节性T细胞的巡逻路线又是如何被精准控制的?这些问题的答案,会让我们离精准调控免疫反应更近一步。
当我们把镜头拉近到淋巴结的亚微米尺度,会发现免疫系统的精密程度远超想象——它不是简单的“激活即战斗”,而是有一套层层筛选的机制,把有限的资源集中给最能打的战士。
免疫的本质,是精准的选择与协作。
这个发现也让我们意识到,我们对免疫系统的了解还只是冰山一角。那些过去被忽略的细胞间互动,那些持续数小时的微小信号传递,恰恰是决定免疫反应强弱的关键。未来的免疫疗法,不再是简单地“激活免疫”,而是要学会“引导免疫”——引导最有效的细胞,去到最需要的位置,完成最精准的任务。