
3 个月前

3 个月前
一场寂静的战争
清晨六点,老张的右手又开始不受控制地颤抖。他试图端起水杯,却洒了一身。这是帕金森病的典型信号——但在他大脑深处,一场更隐秘的战争早已打响。黑质区的多巴胺神经元正被异常折叠的α-突触核蛋白吞噬,而小胶质细胞这支"免疫卫队"在混乱中进退失据。它们的指挥官,一个名为TREM2的受体蛋白,此刻正站在战争转折点上:早期是修复者,晚期却可能沦为破坏帮凶。
时间就是一切
2026年1月13日,河南大学魏建设团队在《npj Parkinson's Disease》发表的综述中,首次系统提出"分期精准干预"理论。基于对数百项研究的分析,他们揭示:TREM2介导的小胶质细胞反应具有显著的时空特异性。在帕金森病早期,当α-突触核蛋白病理负荷较低时,TREM2如同精明的指挥官,激活DAP12/SYK信号轴,调动PI3K-AKT-mTOR通路,促进小胶质细胞吞噬异常蛋白、修复组织损伤。此时增强TREM2功能,能有效保护神经元。
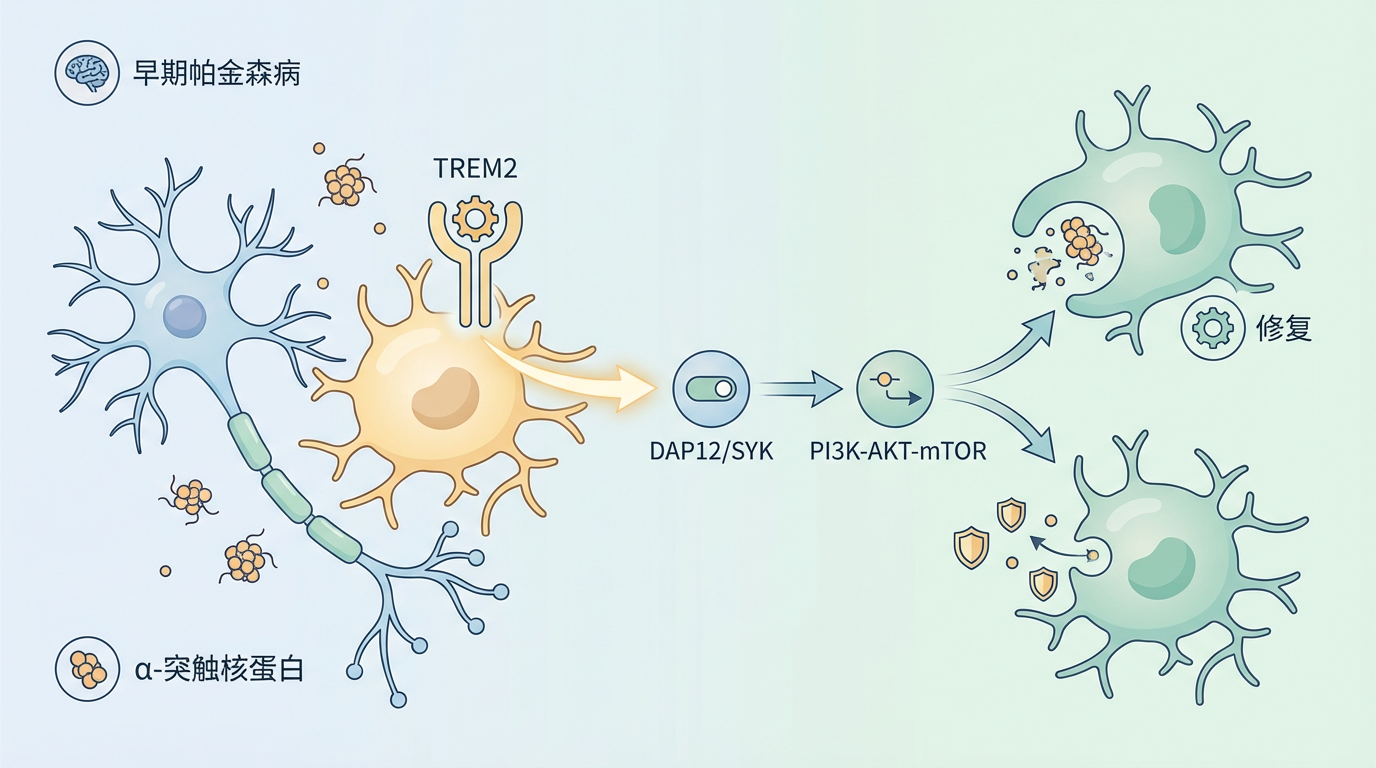
但随着病程进入晚期,持续累积的α-突触核蛋白、线粒体损伤产生的活性氧、以及肠道泄漏引发的系统性炎症形成"三重压力",小胶质细胞的吞噬-溶酶体系统不堪重负。此时TREM2信号变得矛盾——它仍试图组织防御,却导致细胞陷入慢性炎症状态,释放的IL-1β、TNF-α等促炎因子反而加速神经元死亡。这种"保护-受限"的转折点,由病理负荷阈值、遗传背景(如TREM2 R47H突变)和脑区微环境共同决定。
精准制导的武器库
这一发现直接改变了治疗策略的设计逻辑:
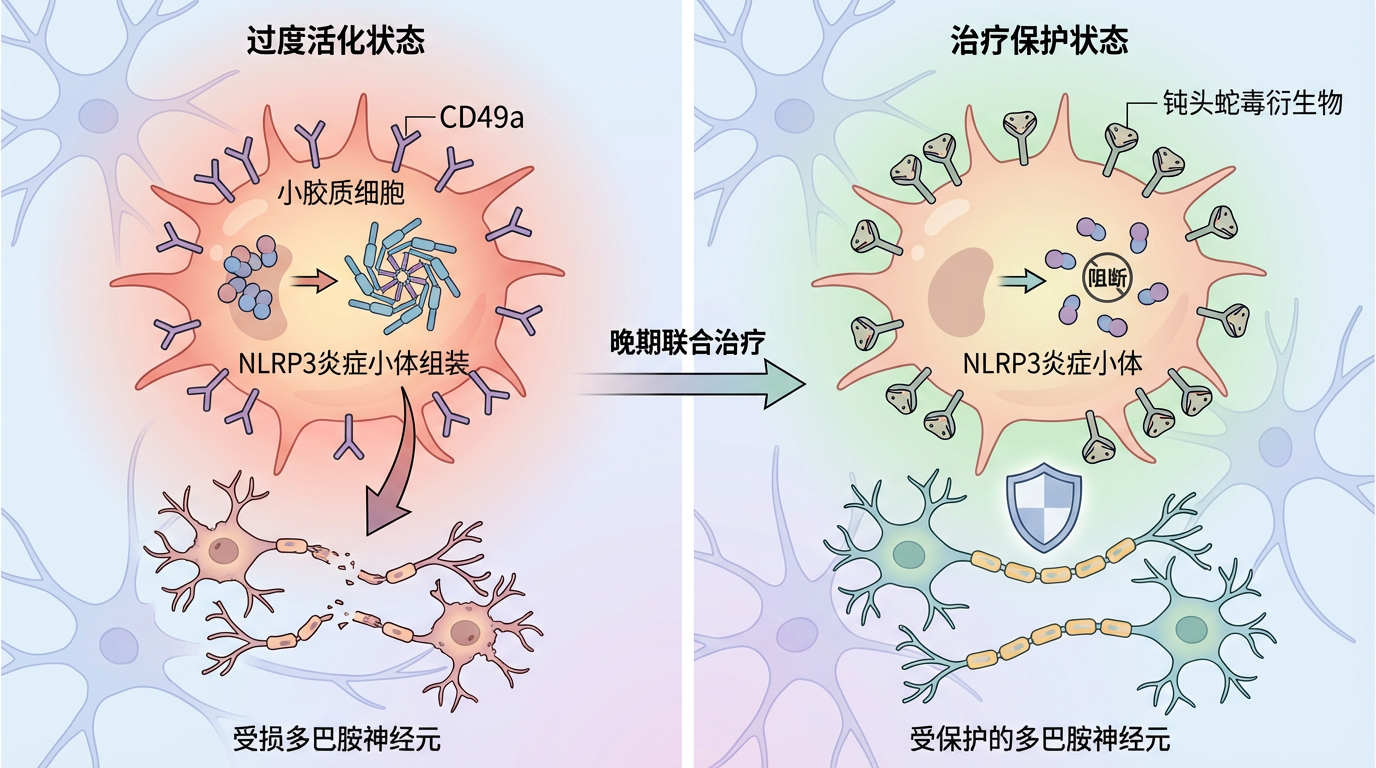
超越帕金森的启示
TREM2的调控机制在神经退行性疾病中展现出惊人保守性。在阿尔茨海默病中,TREM2促进小胶质细胞包裹β-淀粉样蛋白斑块;在渐冻症(ALS)中,它参与清除TDP-43蛋白聚集体。这种共性让魏建设团队提出的分期框架具有跨疾病潜力——当2026年诺华公司启动VHB937抗体治疗ALS的II期试验时,入组标准就特别排除了晚期重度患者,避免重蹈AL002抗体在阿尔茨海默病II期试验中加剧脑萎缩的覆辙。
未来战场地图
真正的变革或许来自技术的融合。单细胞空间转录组技术正在绘制帕金森患者脑内免疫微环境的"三维战争地图":哈佛团队通过单细胞Merfish技术发现,TREM2 R47H突变会导致黑质区小胶质细胞代谢基因表达异常。而可穿戴设备实时监测的震颤数据,通过AI算法能关联炎症标志物波动,构建个体化的"干预时间窗"模型。

老张的智能手表突然震动提醒——今日运动波动异常,建议复诊。他并不知道,这些数据正汇入一个动态管理系统,未来可能在他脑内炎症转折点来临前,精准投递纳米载体包裹的TREM2调节剂。从一刀切的药物试验,到时空调控的免疫重编程,这场对抗神经退行性疾病的战争,正进入精准制导的新纪元。
点击充电,成为大圆镜下一个视频选题!