对抗知识焦虑,从看懂这条开始
App 下载
消化开关的分子密码:肠激酶CUB2域如何精准调控
胰腺炎|胰蛋白酶原|冷冻电镜|CUB2结构域|肠激酶|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
胰腺炎|胰蛋白酶原|冷冻电镜|CUB2结构域|肠激酶|分子细胞生物学|生命科学
你或许从未听说过肠激酶,但它却是你每顿饭的“隐形开关”——没有它,吃进去的肉、蛋、谷物都会变成无法吸收的“大块头”,直接引发严重腹泻和营养不良。更关键的是,这个开关一旦“乱跳闸”,胰蛋白酶原会在胰腺里提前激活,把胰腺当成“消化对象”,直接诱发凶险的胰腺炎。海军军医大学的团队最近用冷冻电镜“拍”清了这个开关的核心结构,终于搞懂了它是怎么精准启动消化,又怎么失控闯祸的。这背后,藏着一个被忽略了几十年的关键分子——CUB2结构域。
你可以把肠激酶(EP)想象成一台嵌在小肠壁上的“精密切割机”,它的任务是精准找到胰蛋白酶原的“启动按钮”——一段叫DDDDK的氨基酸序列,切下这一段,胰蛋白酶原就会变身为能消化蛋白质的胰蛋白酶,进而激活整个消化酶家族。
过去科学家只知道,肠激酶的重链负责“抓牢”底物,轻链负责“切割”,但具体是哪个部位精准定位DDDDK序列,一直是个谜。这次的冷冻电镜结构终于揭晓:重链上的CUB2结构域就是关键的“定位导航仪”。它像一个带凹槽的“抓手”,表面的E574和N619两个氨基酸残基,就像凹槽里的“定位销”,通过电荷互补死死“咬住”胰蛋白酶原上带负电的DDDDK序列。
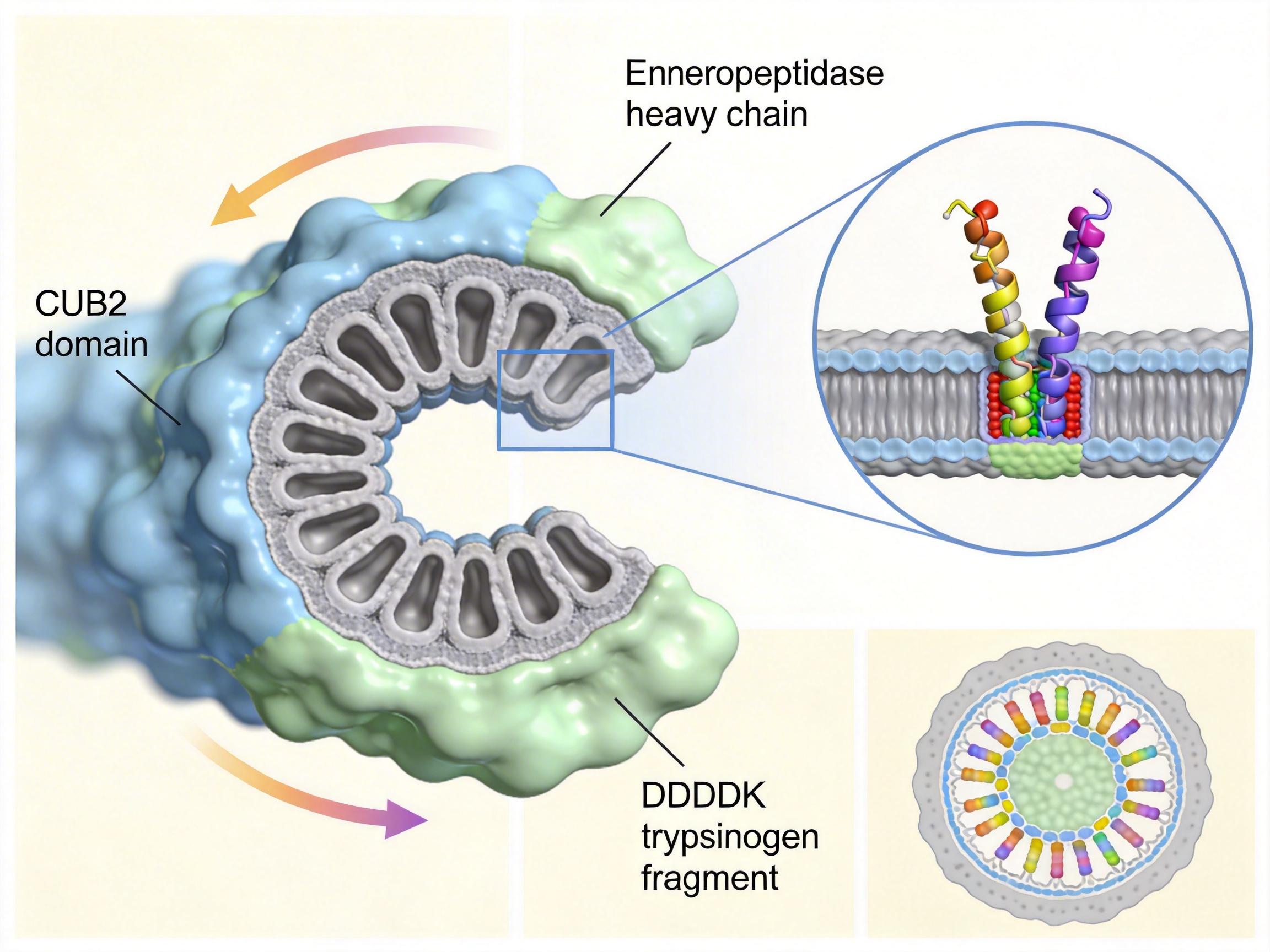
研究团队做了两个关键突变实验:把E574换成不带电的丙氨酸(E574A),肠激酶的切割效率反而提升了——原来这个残基像个“刹车”,通过负电荷排斥避免过度激活;把N619换成丙氨酸(N619A),切割效率直接暴跌——这个残基是“定位销”的核心,没了它,肠激酶就找不到精准的切割位点。
但真实的机制比这更精确:CUB2结构域不仅负责定位,还会带动肠激酶的其他结构域调整姿态,让轻链的催化口袋刚好对准DDDDK的切割位点,整个过程像航天飞船对接一样丝毫不差。
基于CUB2结构域的定位机制,团队提出了一个全新的“肠激酶蛋白水解循环模型”,把消化启动的过程拆成了清晰的四步:
这个模型解决了一个长期的疑问:为什么单独的肠激酶轻链几乎没有活性?因为没有CUB2结构域的“定位导航”,轻链根本找不到精准的切割位点,只会做无用的“随机切割”。而在生理状态下,CUB2结构域还像一个“守门员”,只允许胰蛋白酶原结合,避免肠激酶误切其他蛋白质,维持消化的稳态。
更重要的是,这个模型解释了胰腺炎的发病逻辑:当肠激酶通过胰十二指肠反流进入胰腺后,CUB2结构域依然会精准结合胰腺里的胰蛋白酶原,在胰腺内部启动切割激活,导致胰腺被自身的酶“消化”,引发炎症甚至坏死。
这次研究最直接的应用,就是为胰腺炎等疾病提供了新的治疗靶点。过去治疗胰腺炎,要么用广谱的蛋白酶抑制剂“一刀切”,要么只能靠禁食、补液等支持疗法,副作用大且效果有限。
现在我们知道,CUB2结构域是肠激酶激活胰蛋白酶原的核心,那么就可以设计专门针对CUB2结构域的抑制剂:比如模拟DDDDK序列的肽类分子,抢占CUB2的结合位点,让它无法结合胰蛋白酶原;或者通过小分子药物改变E574和N619的电荷环境,让肠激酶“刹车失灵”或者“定位不准”。
研究团队还解析了现有药物纳法莫司他与肠激酶的结合结构:这种药物会和轻链的催化位点形成共价结合,直接“堵死”切割通道。但现有药物的问题是特异性不够,可能会抑制其他蛋白酶。而基于CUB2结构域的药物,只会精准阻断肠激酶对胰蛋白酶原的激活,副作用会小得多。
不过这项研究也有局限:目前只解析了肠激酶与胰蛋白酶原结合的静态结构,而真实的生物过程是动态的,CUB2结构域在结合底物时的构象变化细节,还有待更精准的时间分辨冷冻电镜技术来揭示。
从微观的分子互作到宏观的消化疾病,这场持续了几十年的研究,终于为我们打开了一扇理解消化稳态的新窗口。过去我们只知道“吃进去的东西会被消化”,现在我们能看清每一个分子的“动作”——CUB2结构域的定位、轻链的切割、胰蛋白酶的激活,每一步都像精密的钟表齿轮,环环相扣。
精准的分子互作,才是生命稳态的核心。这个道理不仅适用于消化过程,也适用于所有的生物机制。未来,当我们能像调节钟表齿轮一样,精准调控这些分子的活性时,很多现在的“难治之症”,或许都会变成可防可治的“普通疾病”。而这一切的起点,就是看清这些微小分子的“一举一动”。