对抗知识焦虑,从看懂这条开始
App 下载
85%肠癌免疫治疗无效,这种益生菌破了局
香港中文大学|肠道微生物|抗PD-1疗法|微卫星稳定型肠癌|链状双歧杆菌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
香港中文大学|肠道微生物|抗PD-1疗法|微卫星稳定型肠癌|链状双歧杆菌|肿瘤学|医学健康
当医生告诉一位晚期肠癌患者“你对免疫治疗耐药”时,这句话的分量等同于判了半死刑——全球85%的肠癌患者属于“微卫星稳定型”(MSS),他们的肿瘤像裹了层密不透风的壳,免疫细胞根本打不进去。抗PD-1这类曾创造抗癌奇迹的疗法,在他们身上的有效率不到5%。
直到香港中文大学和西安交通大学的团队,从我们每个人的肠道里找到了破局的钥匙:一种叫链状双歧杆菌的益生菌。它不仅能直接抑制肿瘤生长,还能让原本“沉睡”的免疫细胞醒过来,和抗PD-1疗法联手,在MSS肠癌模型里打出了远超单一疗法的效果。这不是科幻,是刚发表在顶级医学期刊《GUT》上的真实研究。
先得搞懂MSS肠癌为什么难治:这类肿瘤的基因突变少,免疫细胞很难“认出”它们是敌人;就算有少量免疫细胞摸到肿瘤附近,也会被肿瘤释放的“催眠信号”困在原地——这就是免疫治疗耐药的核心。
过去科学家试过各种办法:给免疫细胞“打鸡血”、用药物撕开肿瘤的保护层,但要么效果有限,要么副作用大得让人扛不住。而这次的研究团队换了个思路:从肠道里找帮手。
他们先对比了308名肠癌患者和288名健康人的肠道菌群,发现肠癌患者肠道里的链状双歧杆菌数量明显更少,而对免疫治疗有反应的患者,这种菌的含量又显著高于无反应者。接下来的动物实验更直接:给患MSS肠癌的小鼠喂链状双歧杆菌,再配合抗PD-1治疗,肿瘤的生长速度比只做免疫治疗的小鼠慢了近一半。
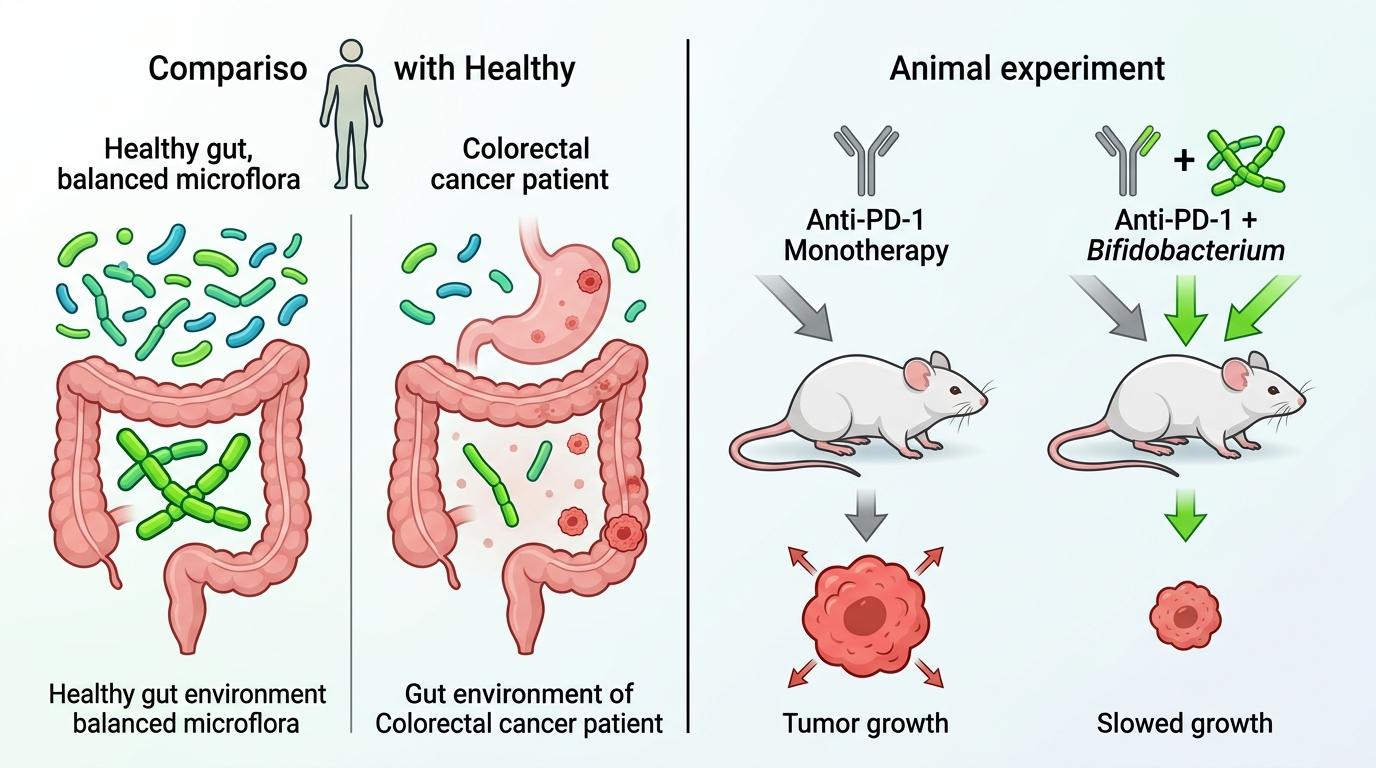
更关键的是,当他们把小鼠体内的CD8+ T细胞——也就是免疫体系里的“杀手细胞”——清除后,链状双歧杆菌的效果就消失了。这说明,这种益生菌的核心作用,就是激活这群原本被肿瘤“催眠”的杀手。
链状双歧杆菌到底是怎么叫醒杀手细胞的?答案藏在它的代谢产物里。
研究人员通过代谢组分析发现,链状双歧杆菌在肠道里会产生大量乙酸盐——一种短链脂肪酸。你可以把它想象成益生菌发给免疫细胞的“集结号”:它会通过CD8+ T细胞表面的单羧酸转运蛋白4(MCT4)钻进细胞里,激活一条叫JNK/MAPK的信号通路,就像按下了杀手细胞的“启动键”。
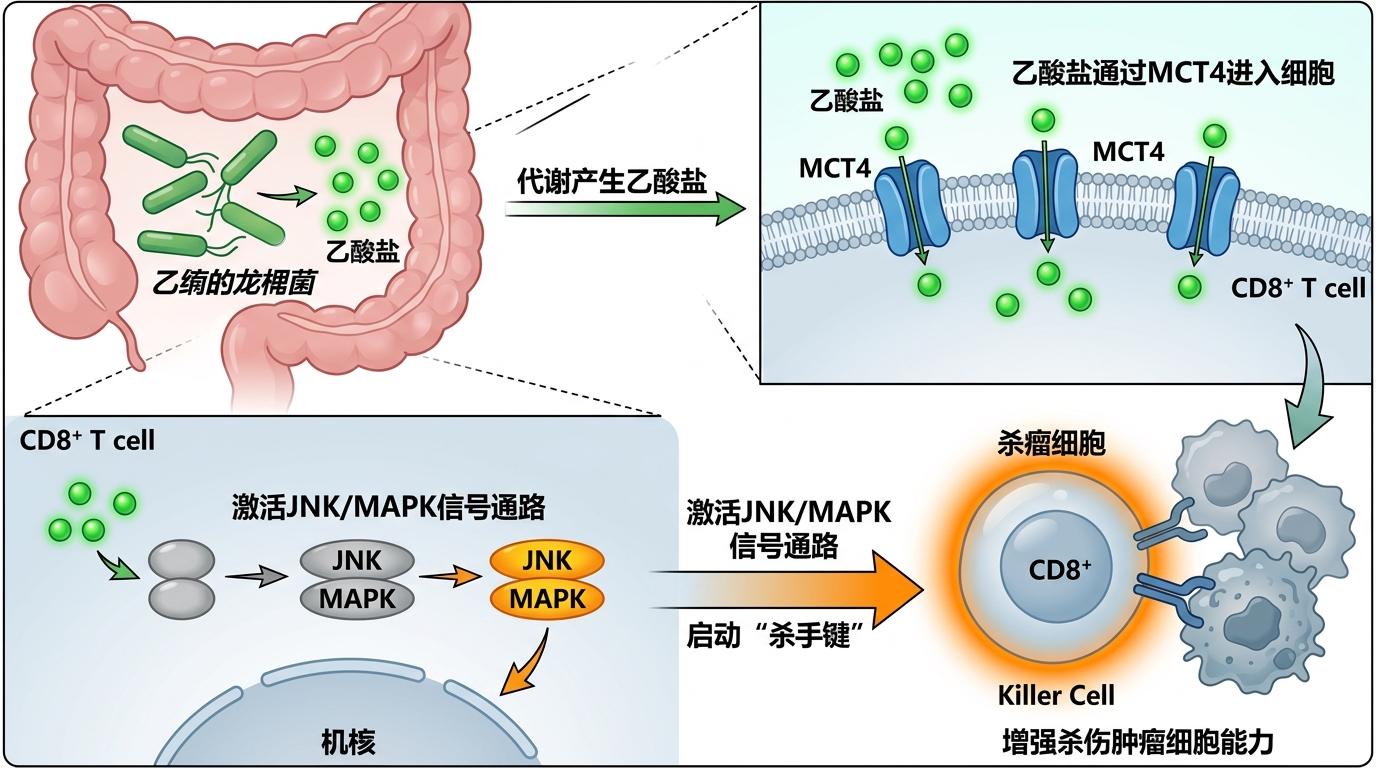
启动后的CD8+ T细胞会发生两个关键变化:一是分泌更多的干扰素-γ和颗粒酶B,这两种物质是它们杀伤肿瘤细胞的“武器”;二是减少表面PD-1蛋白的表达——而抗PD-1疗法的作用,正是解除PD-1带来的免疫抑制。相当于益生菌先把杀手细胞从沉睡中摇醒,抗PD-1疗法再帮它们去掉身上的枷锁,两者一联手,原本“冷得像冰”的肿瘤微环境,瞬间就变成了免疫细胞的“战场”。
这里得补个关键细节:乙酸盐的作用是精准针对CD8+ T细胞的,不会乱激活其他免疫细胞引发炎症,这也是益生菌疗法副作用小的原因。而且动物实验显示,就算直接给小鼠喂乙酸盐,也能达到类似的效果,这为后续开发更便捷的治疗药物提供了可能。
当然,这项研究离真正走进临床还有一段路要走。
首先,益生菌的效果有很强的菌株特异性——不是所有双歧杆菌都能激活CD8+ T细胞,只有链状双歧杆菌有这个本事。市面上常见的益生菌制剂大多是混合菌株,不一定能达到研究中的效果。
其次,个体差异是绕不开的问题。每个人的肠道菌群基础都不一样,有的人体内本来就有不少链状双歧杆菌,有的则几乎没有,这可能会导致治疗效果参差不齐。未来可能需要先检测患者的肠道菌群,再定制个性化的益生菌补充方案,也就是“精准微生态治疗”。
还有安全性的问题:虽然链状双歧杆菌是人体肠道本来就有的益生菌,但给晚期癌症患者长期服用,会不会引发潜在的感染风险?尤其是那些免疫功能已经很弱的患者,这需要更大规模的临床试验来验证。
不过这些问题都挡不住一个趋势:肠道微生物正在成为癌症治疗的新靶点。除了链状双歧杆菌,已经有研究发现 Akkermansia 菌、Faecalibacterium 菌等也能增强免疫治疗效果,未来说不定能找到更多“抗癌益生菌”,组成一支肠道里的“抗癌军团”。
我们总把癌症当成一场和癌细胞的正面战争,却常常忘了,我们的身体里还有一支隐藏的盟友——肠道菌群。它们不是无关紧要的“过客”,而是参与免疫调节、影响治疗效果的关键角色。
这项研究最动人的地方,不在于它找到了一种新的抗癌药物,而在于它让我们重新审视和自身微生物的关系:那些在肠道里默默生存的细菌,可能就是我们对抗癌症最天然的武器。
肠道里的小居民,正在改写抗癌的大格局。