对抗知识焦虑,从看懂这条开始
App 下载
软纳米颗粒敲开免疫大门,精准激活抗癌力
力学信号蛋白通道|外泌体|巨噬细胞|软纳米颗粒|同济大学|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
力学信号蛋白通道|外泌体|巨噬细胞|软纳米颗粒|同济大学|肿瘤学|医学健康
当医生告诉你肿瘤“太硬”的时候,你可能以为是指肿块的触感——但在细胞的微观世界里,“硬”还是“软”,是能决定生死的信号。2026年4月,同济大学的实验室里,一群科学家用一种软乎乎的纳米颗粒,让巨噬细胞吐出了3倍于平时的外泌体,这些被“机械编程”的小囊泡,居然能精准唤醒沉睡的抗癌T细胞,把肿瘤的免疫抑制防线撕开一道口子。更让人意外的是,这一切的开关,居然是细胞表面一个能“摸”到力学信号的蛋白通道。
你可以把巨噬细胞想象成一个带感应门的快递站,平时只会按部就班地往外送包裹(外泌体)。而这次科学家送来的,不是催单的信号,是一个轻轻按在感应门上的软球——低模量纳米颗粒。
这个软球的关键作用,是触发细胞表面的Piezo1通道。这是一种像弹簧一样的机械敏感蛋白,只要感受到合适的压力,就会“啪”地打开通道门,让钙离子(Ca²⁺)涌进细胞。
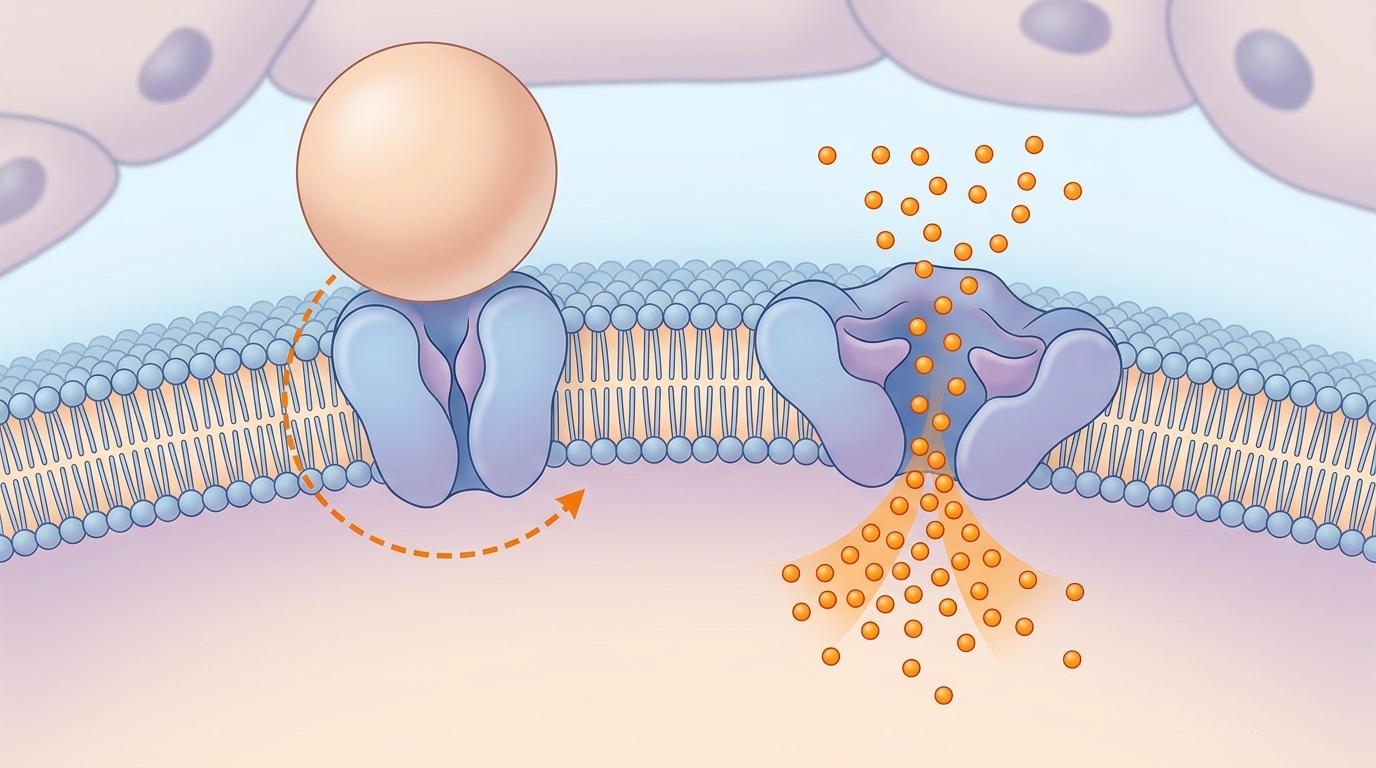
接下来是一套精确到分子级的连锁反应:
但真实的机制比这个快递站类比更精确:Piezo1通道对力的感知精准到15皮牛顿——相当于一根头发丝重量的百万分之一,只有软颗粒的压力能刚好触发它,硬颗粒反而会让通道“失灵”。
这些被软颗粒“催出来”的外泌体,和普通外泌体不一样。蛋白质组学分析显示,它们带着一套专门激活T细胞的“密码”——能精准调控TCR信号通路,就像给T细胞递上了一把打开抗癌武器的钥匙。
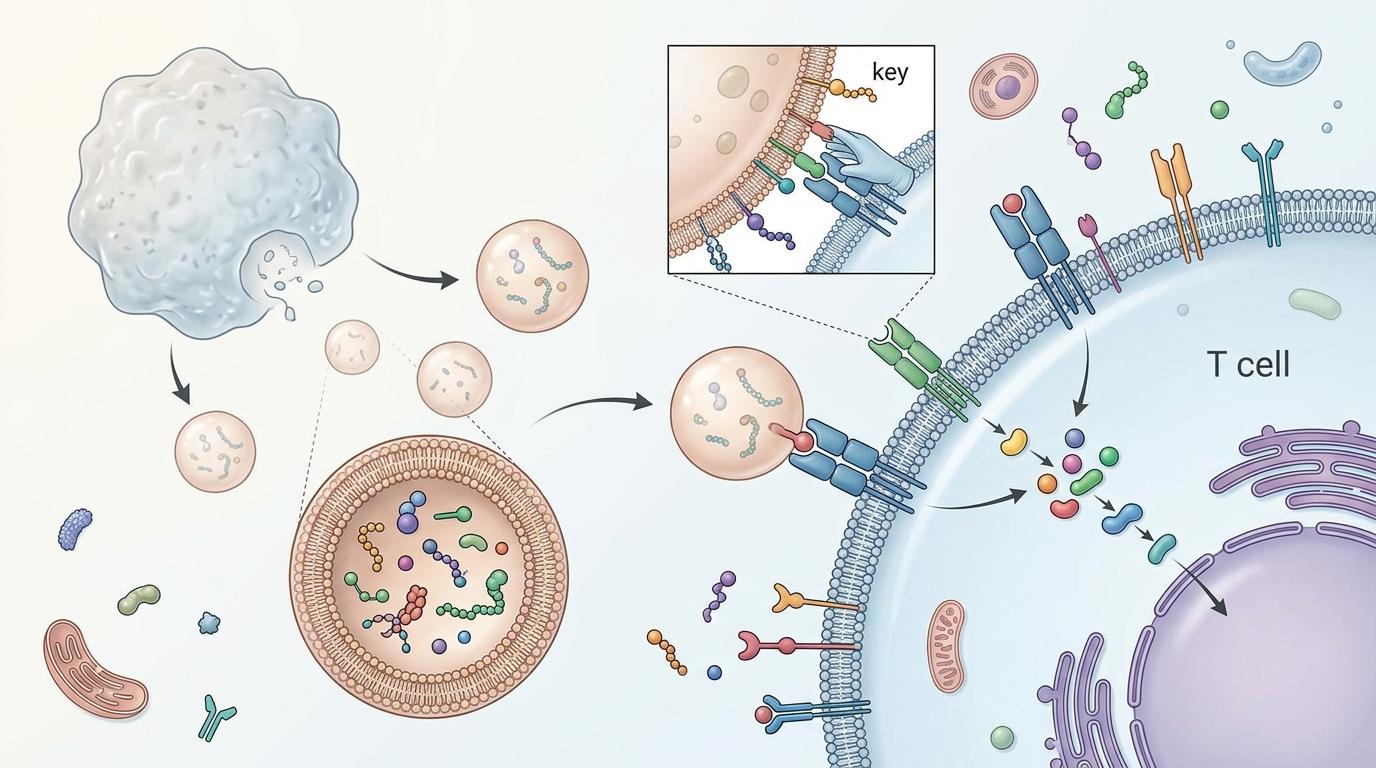
在实验室的培养皿里,这些外泌体能让T细胞的活化效率显著提升;到了小鼠的4T1乳腺癌模型里,效果更直观:注射了纳米力学工程化外泌体的小鼠,脾脏里的CD8+杀伤性T细胞数量大幅扩增,肿瘤微环境里的免疫抑制细胞减少了近一半,肿瘤体积比对照组缩小了50%。
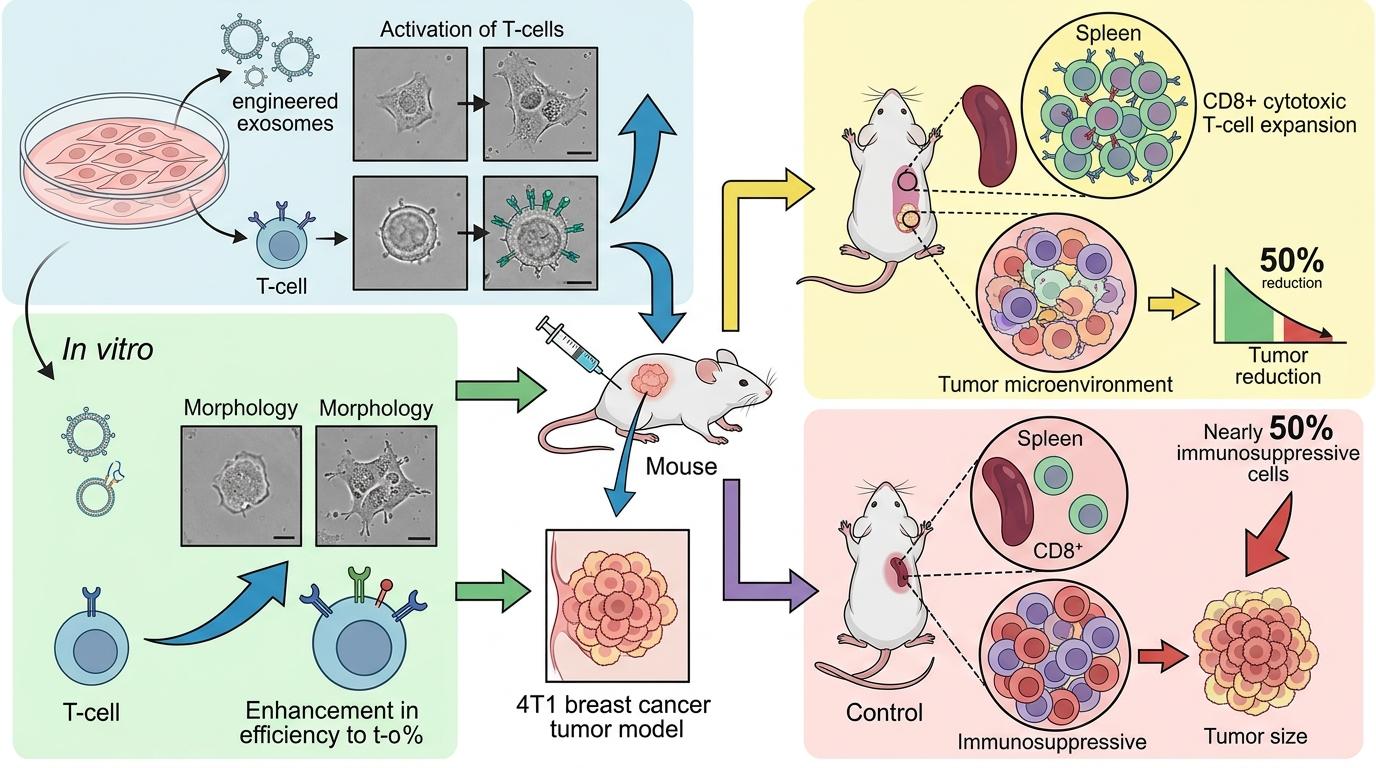
更值得关注的是,这种方法比传统用LPS诱导的外泌体疗法更安全。LPS是一种强炎症刺激物,容易引发全身免疫反应,而软颗粒的机械刺激是精准作用在细胞表面的“开关”,不会乱触发其他免疫通路。
当然,这项研究也有未解决的问题:目前只验证了巨噬细胞来源的外泌体,其他免疫细胞比如树突状细胞,会不会对这种力学刺激有不同的反应?不同肿瘤的“硬度”不同,软颗粒的参数要不要跟着调整?这些都是未来要啃的硬骨头。
把这种疗法推到临床,科学家们还得解决三个现实问题。
第一是标准化。外泌体的分离纯化至今没有统一标准,超速离心法容易破坏外泌体结构,免疫亲和法成本太高,要大规模生产符合临床要求的外泌体,得先找到高效又稳定的纯化技术。
第二是安全性。虽然小鼠实验里没发现明显毒性,但外泌体在人体内的长期代谢路径、会不会触发潜在的免疫反应,还需要系统的长期研究。不同来源的外泌体安全性差异很大,得建立一套标准化的安全评价体系。
第三是个性化。不同患者的肿瘤微环境“硬度”不同,免疫状态也千差万别,怎么根据每个患者的情况调整纳米颗粒的参数,实现真正的精准治疗,还需要结合AI和单细胞测序技术,建立个性化的治疗模型。
当我们谈论癌症治疗时,总是在找“杀死肿瘤的药物”,但这项研究给我们指了另一条路:不是直接攻击肿瘤,而是给免疫细胞递一把精准的“力学钥匙”,让它们自己觉醒。
从宏观的肿瘤硬度,到微观的15皮牛顿力,再到分子级的信号通路,科学家们正在把“看不见的力学信号”变成“可操控的治疗工具”。这不仅是肿瘤免疫治疗的一个新突破,更重要的是,它让我们意识到:细胞的世界里,除了化学信号,力学信号同样是决定生死的关键。
软力激活免疫,精准对抗癌症——这可能是未来抗癌治疗的一个全新方向。