对抗知识焦虑,从看懂这条开始
App 下载
AI改写生物制造规则:酶与代谢路径的革命
生物制造效率|AI酶设计|陈国强教授团队|清华大学生命科学学院|大语言模型|合成生物学|生命科学|人工智能
对抗知识焦虑,从看懂这条开始
App 下载
生物制造效率|AI酶设计|陈国强教授团队|清华大学生命科学学院|大语言模型|合成生物学|生命科学|人工智能
当实验室里的科研人员还在对着数万条酶序列发愁,计算着按传统方法筛选完需要耗时数年时,AI已经在几天内给出了数十种自然界从未有过的酶设计方案。这不是科幻小说里的情节,而是2026年生物制造领域正在发生的现实——清华大学生命科学学院陈国强教授团队的研究,正让AI成为破解生物制造核心难题的关键钥匙。我们不禁要问,AI究竟是如何突破自然进化的局限,重新定义生物制造的效率边界?
你可以把酶理解成生物体内的“精密螺丝刀”——每种酶只负责拧开特定的“螺丝”,催化特定的生物反应。但自然界的酶总有缺陷:要么活性低,要么适配性差,甚至根本没有能催化特殊反应的酶。传统的定向进化法,就像给螺丝刀随机磨齿再试,不仅耗时数年,还未必能得到趁手的工具。
AI的出现彻底改变了这个逻辑。它先学习数据库里海量酶的DNA和氨基酸序列,理解序列和功能的对应关系,再根据目标反应的需求,直接设计出全新的序列组合。比如美国贝克实验室用RFdiffusion模型,能从无到有生成适配复杂活性位点的蛋白骨架,设计出的丝氨酸水解酶,催化效率达到2.2×10^5 M^-1 s^-1,结构和设计模型的偏差小于1埃。
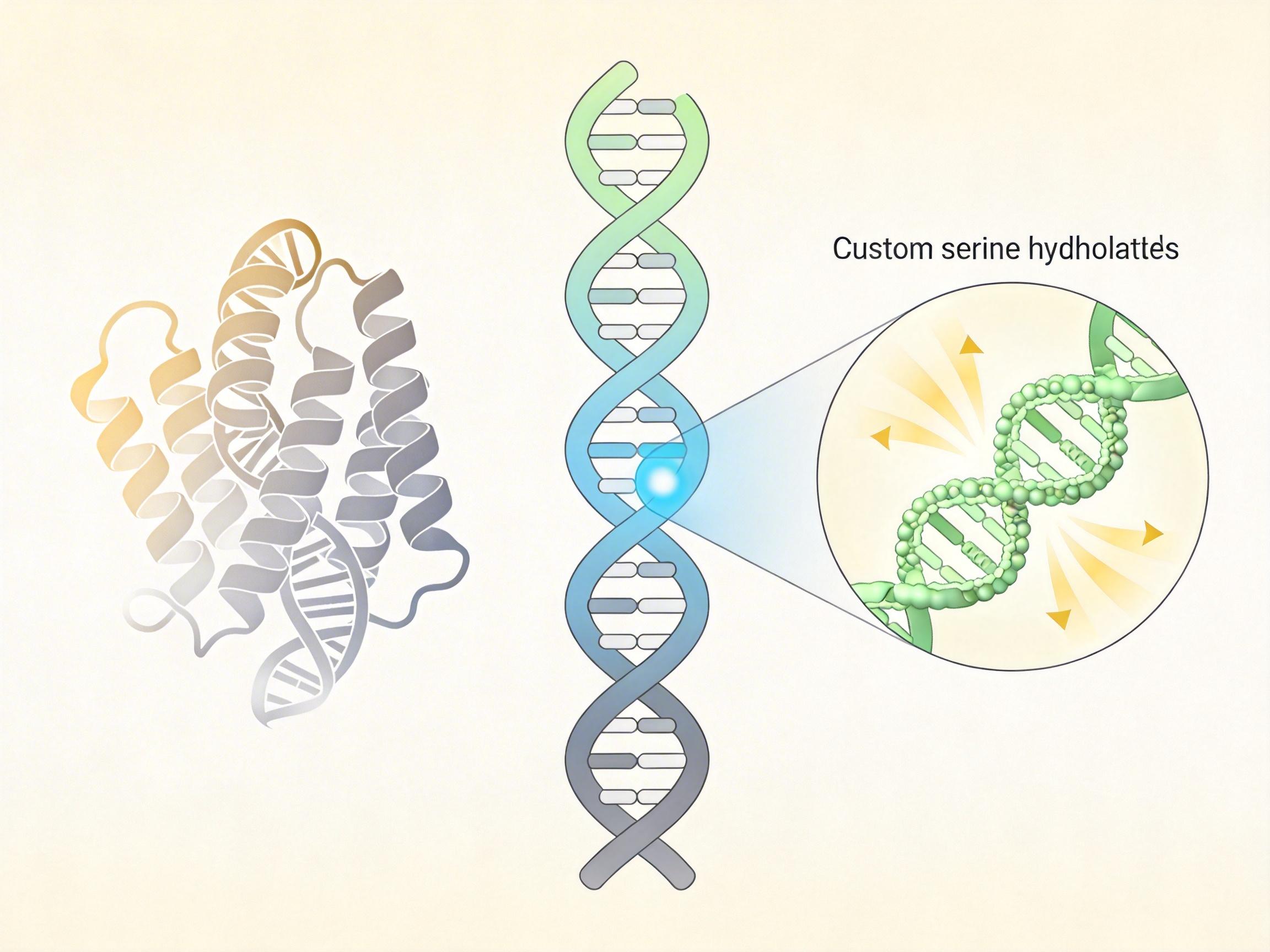
科研人员只需要把AI设计的序列合成为DNA,再用细菌细胞验证活性——原本按年计算的工作量,现在几天就能完成。更重要的是,AI能造出自然界从未进化出的酶,为生物制造打开了全新的可能性。
如果说酶是生物制造的“螺丝刀”,那代谢路径就是微生物细胞里的“生产线”——一系列酶分工协作,把原料变成目标产物。传统的代谢路径优化,就像在密密麻麻的旧厂房里重新布线,全靠科研人员凭经验摸索,不仅效率低,还容易漏掉关键节点。
AI则是这个工厂的“智能设计师”。它能快速检索全球已发表的代谢路径和产率数据,通过算法排列组合,找出产量最高的路径方案。荷兰代尔夫特理工大学的团队用这种方法,把酿酒酵母中p-香豆酸的产量提升了137%;清华陈国强教授团队用机器学习预测代谢动力学,指导生物燃料生产,效果比经典动力学模型更精准。
更厉害的是,AI能整合多组学数据,预测细胞在不同环境下的代谢响应,甚至设计出动态调控的“智能生产线”——实时调整酶的活性,避免代谢瓶颈和毒性积累。这就好比给生产线装了传感器和自动调节器,能根据原料和环境变化自动优化流程。
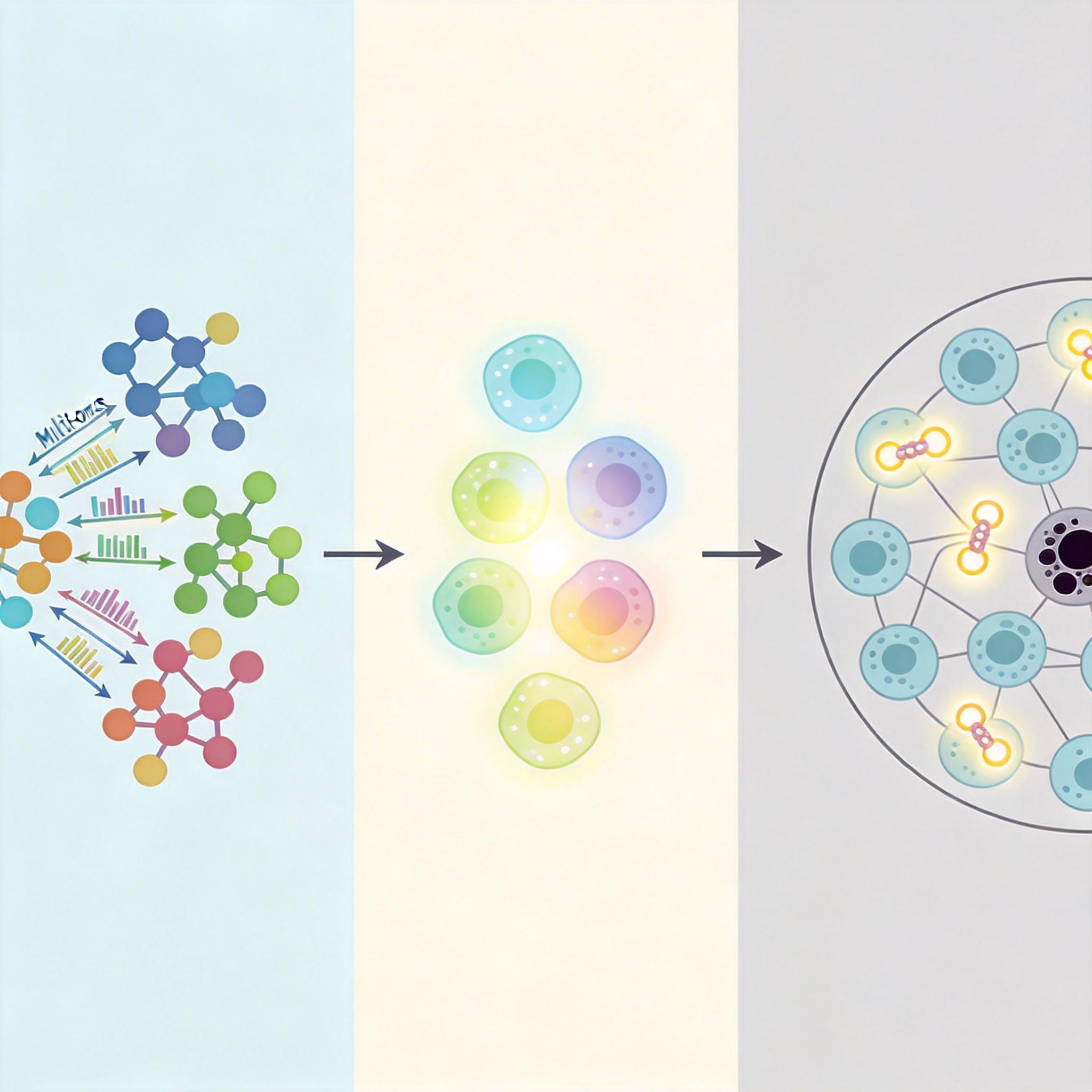
当然,AI的能力也有边界。目前它还很难完全模拟生物系统的动态复杂性,设计出的酶活性有时仍不如天然酶,工业化应用前还需要大量实验验证。但不可否认的是,它已经把代谢路径优化的效率提升了数十倍。
AI在生物制造领域的狂飙突进,也带来了新的挑战——人才缺口。传统的生物学家不懂AI算法,计算机工程师又不了解生物系统的复杂性,能打通两者的跨学科人才成了稀缺资源。
数据显示,生物制造企业中36%难以招聘到懂AI的过程开发人员,28%找不到合适的下游生产人才。为了应对这个问题,高校开始调整课程体系:江南大学把AI内容融入合成生物学课程,美国芝加哥大学推出“AI驱动的材料与系统分子工程”双学位项目;企业也在通过内部培训和产学研合作,加速培养复合型人才。
这些努力正在见效:Biodesign Challenge竞赛中,67%的非STEM背景学生用AI辅助工具完成了生物设计项目,对科学基础建设的满意度达到4.0/5。但要填补人才缺口,还需要更多跨学科的教学改革和产业实践,让“生物+AI”的复合型人才成为常态。
当AI能设计出自然界没有的酶,能给微生物工厂重新布线,生物制造就不再是对自然的被动模仿,而是对生命系统的主动设计。这不仅能加速药物、新材料的开发,还能推动绿色制造的发展——用生物合成替代传统化学工艺,减少碳排放和环境污染。
当然,这场革命也伴随着隐忧:AI模型的可解释性不足,设计出的生物系统可能存在未知风险,伦理和监管的挑战也随之而来。但正如陈国强教授所说,AI已经成为生物制造的核心驱动力,未来的生物制造,必然是AI与生物学深度融合的产物。
AI懂算法,生物学家懂生命,两者结合才能创造未来。