
3 个月前

3 个月前
2025年12月28日,被誉为“GLP-1先驱”的美国内分泌学家乔尔·哈本纳(Joel Habener)因心脏病与世长辞,享年88岁。他的离去,让医学界再次将目光投向那场由他意外开启的、至今仍在席卷全球的健康革命。
故事要追溯到20世纪70年代。当时,糖尿病已是医学界关注的焦点,但肥胖远未成为今日的公共卫生危机。在麻省总医院的分子内分泌学实验室里,哈本纳决定避开热门的胰岛素研究,转而探索一个“冷门”方向——胰高血糖素,一种与胰岛素作用相反的升糖激素。他设想,若能抑制它,或许能为糖尿病治疗开辟新径。
重组DNA技术的兴起为他提供了工具,但研究材料却成了难题。一个偶然的机会,实验室一位同事的亲戚从事水产工作,这给了哈本纳一个大胆的想法:利用琵琶鱼。这种深海鱼的胰岛细胞不像哺乳动物那样分散,而是集中在一个如大理石般大小的器官“布罗克曼体”中,极易提取。于是,哈本纳的博士后们成了码头的常客,在渔船边现场解剖,将最新鲜的样本速冻在液氮罐中带回实验室。
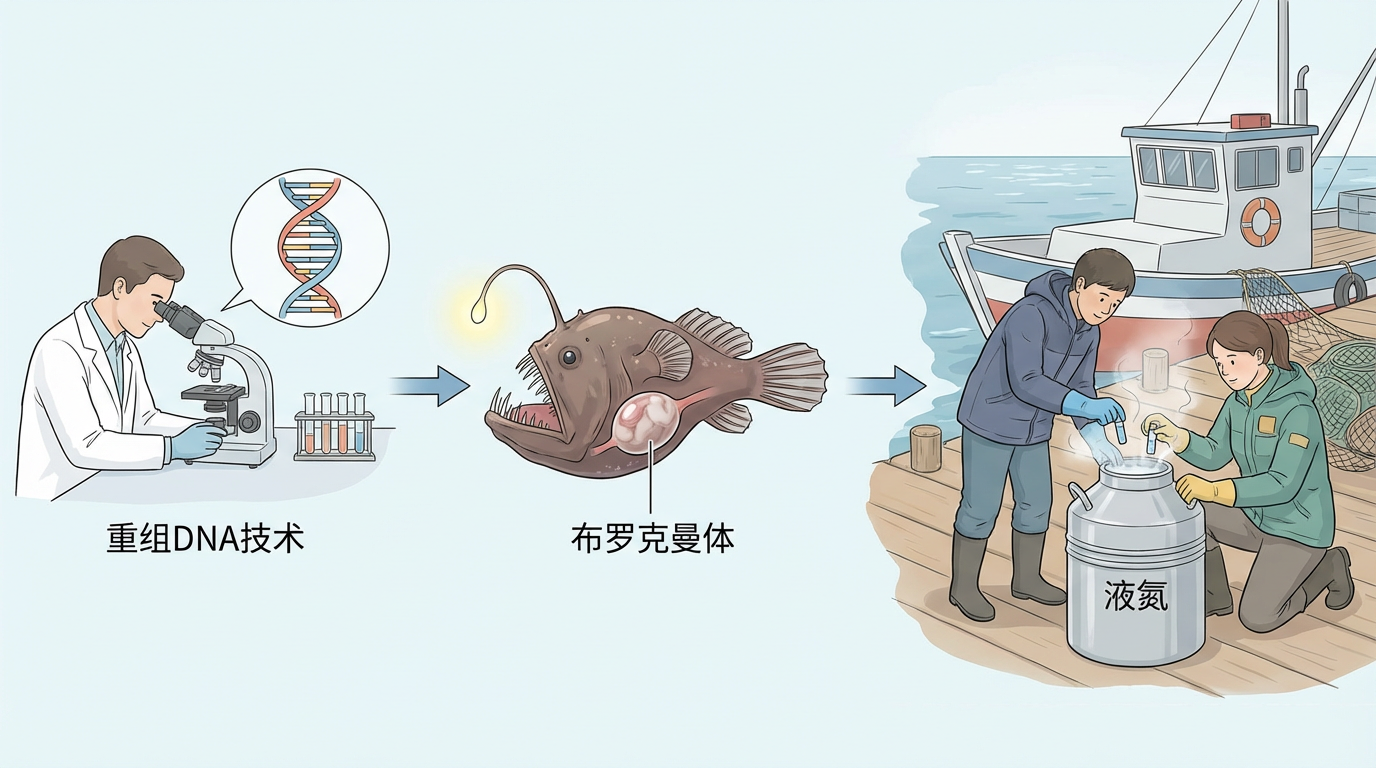
正是这条相貌平平的鱼,带来了一个颠覆性的发现。通过克隆琵琶鱼的胰高血糖素基因,哈本纳团队发现,胰高血糖素并非直接生成,而是从一个更大的“前体蛋白”上切割而来。更重要的是,与它一同被切割下来的,还有一种从未被发现过的神秘蛋白。后续研究证实,这种蛋白能在血糖升高时,精准地促进胰岛素分泌。它,就是胰高血糖素样肽-1(GLP-1)。
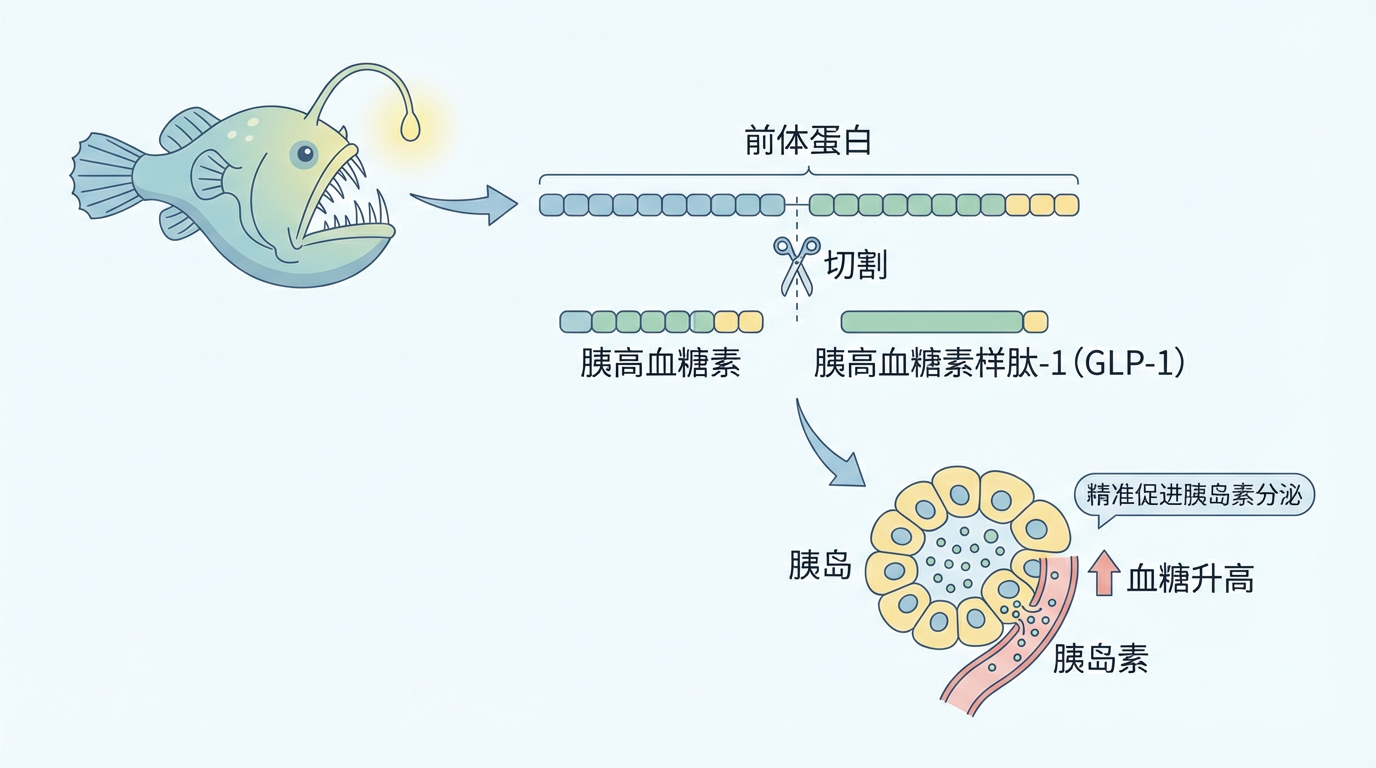
“我想应该用‘意外发现’来形容,”哈本纳晚年回忆道。发现GLP-1的那晚,他半开玩笑地告诉妻子:“我们今天有了一个有趣的发现,我要去斯德哥尔摩了。”
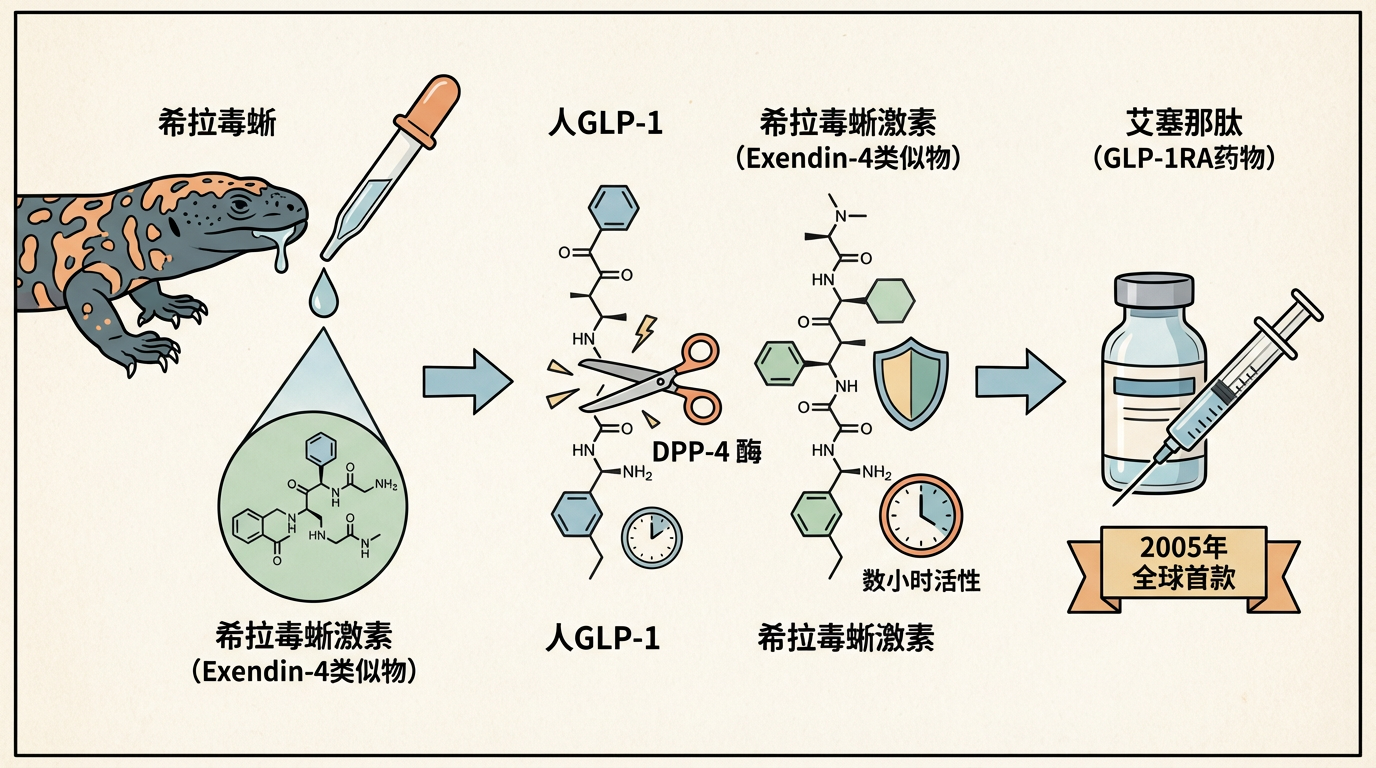
哈本纳的发现,为学界寻找了半个多世纪的“肠促胰素”揭开了神秘面纱。然而,将这一基础发现转化为药物的道路,漫长而曲折。最大的障碍在于,天然的GLP-1在人体血液中只能存活不到两分钟,就会被一种叫做DPP-4的酶迅速分解,这使其无法直接成药。
真正的突破来自另一个“偶然”。科学家们在一种名为“希拉毒蜥”的蜥蜴唾液中,发现了一种名为Exendin-4的激素,其结构与GLP-1惊人相似,却能抵抗DPP-4的分解,在体内维持数小时的活性。这一发现,直接催生了2005年全球首款GLP-1受体激动剂(GLP-1RA)药物——艾塞那肽的诞生。
药物的进化史就此拉开序幕。从每日两次注射的艾塞那肽,到2009年诺和诺德推出的每日一次的利拉鲁肽,再到2014年礼来公司实现每周一次给药的度拉糖肽,科学家们通过持续的分子结构创新,不断延长药物的半衰期,极大提升了患者的用药便利性。
而在这条持续创新的道路上,一个最初被视为“副作用”的现象,彻底改变了GLP-1的命运。临床试验中的患者普遍报告恶心、食欲减退。研究人员很快意识到,这并非简单的副作用,而是GLP-1的另一种强大机制:它能作用于大脑中枢,抑制食欲;同时延缓胃排空,增加饱腹感。这个“副作用”的华丽转身,让GLP-1药物从单纯的降糖药,一跃成为对抗肥胖的革命性武器。
这场革命的到来恰逢其时。目前,全球有超过10亿人受肥胖困扰,约5亿人患有2型糖尿病。GLP-1药物的出现,以前所未有的方式改变了这一切。
然而,没有一种药物是完美的。GLP-1的巨大成功背后,也伴随着一系列挑战与争议。
尽管挑战重重,GLP-1的故事远未结束。一场更深层次的创新浪潮正在涌来。
回顾GLP-1疗法从发现到风靡全球的历程,我们看到了一曲由科学偶然与持续创新共同谱写的交响乐。哈本纳在码头边解剖的一条鱼,是这场革命充满戏剧性的序章,充满了科学发现的偶然之美。而此后四十余年,从蜥蜴唾液中寻找灵感,到一次次对分子结构进行精妙改造,再到不断拓展其临床应用边界,则是一代代科学家与工程师们以坚定的毅力,将偶然转化为必然的漫长征途。
这场革命远未终结。它正在深刻地提醒我们,医学的每一次重大突破,不仅在于创造一个“神奇分子”,更在于它如何重塑我们对疾病的理解、对健康的追求,以及对一个更公平、更普惠的未来的思考。这或许是乔尔·哈本纳和所有GLP-1先驱们,留给世界最宝贵的遗产。
点击充电,成为大圆镜下一个视频选题!