
3 个月前

3 个月前
在人体与癌症的战争中,免疫系统扮演着边防警察的角色,时刻巡逻,识别并清除那些叛变的细胞。然而,一些癌症是天生的伪装大师,它们几乎不携带任何可供识别的特征——即“新抗原”,这使得它们在免疫系统的雷达下悄然遁形。这些肿瘤在免疫学上被称为“冷肿瘤”,因为它们缺乏免疫细胞的浸润,像一片沉寂的荒漠。对于这类低突变负担的肿瘤,即使是强大的免疫检查点抑制剂(如PD-1抗体)也常常束手无策,因为它们的作用机制是“松开刹车”,但如果连能战斗的T细胞“驾驶员”都没有,再好的油门也无济于事。如何将这些“冷肿瘤”转化为免疫系统可以识别和攻击的“热肿瘤”,一直是癌症免疫治疗领域最棘手的瓶颈之一。
就在这个难题面前,一则突破性的消息传来。2025年12月23日,复旦大学附属华山医院的钦伦秀、苏英晗团队,联合徐州医科大学及海军军医大学国家肝癌科学中心的苏长青团队,在国际期刊 《信号转导与靶向治疗》 上发表了一项里程碑式的研究。他们设计了一种“智能生物导弹”——一种经过基因工程改造的溶瘤腺病毒,它能像精准的快递员一样,将“死亡标签”(即新抗原)直接递送到肿瘤细胞内部。
这项研究的核心成果是一个名为 NeoViron 的多功能溶瘤腺病毒平台。它不仅能携带并扩增肿瘤特异性的新抗原,还能同时表达一种名为 Flt3L 的关键生长因子。在低突变负荷的肝内胆管癌动物模型中,NeoViron展现了惊人的效果:它不仅显著抑制了肿瘤的生长,还成功阻止了癌细胞的转移。这一发现,为那些对现有免疫疗法反应不佳的“冷肿瘤”患者,点燃了新的希望之光。
NeoViron的成功并非偶然,它精妙地设计了一套协同作战的“四重打击”机制,将一场原本毫无胜算的遭遇战,变成了一场精心策划的围剿战:
第一重:精准标记,暴露敌人。 NeoViron首先像间谍一样潜入肿瘤细胞,利用其内部的机制,大量生产并展示出肿瘤的新抗原。这相当于在伪装的敌人身上强行贴上醒目的“通缉令”,使其在免疫系统面前无所遁形。
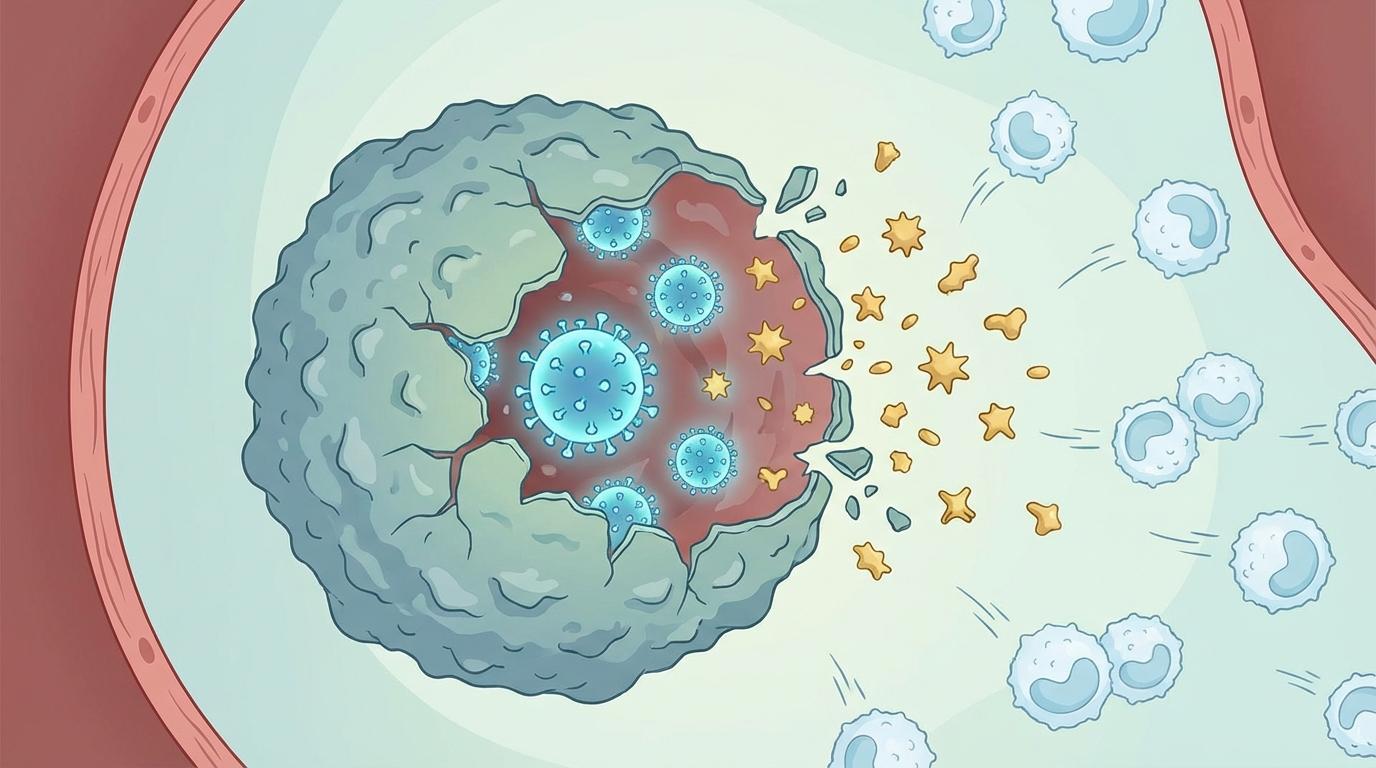
第二重:引爆肿瘤,制造“犯罪现场”。 病毒在肿瘤细胞内复制到一定程度后,会使其裂解死亡,即“溶瘤效应”。这个过程不仅直接杀伤了癌细胞,还释放出大量肿瘤内部的抗原,形成一个“原位抗原库”,为免疫系统提供了更多识别敌人的线索。
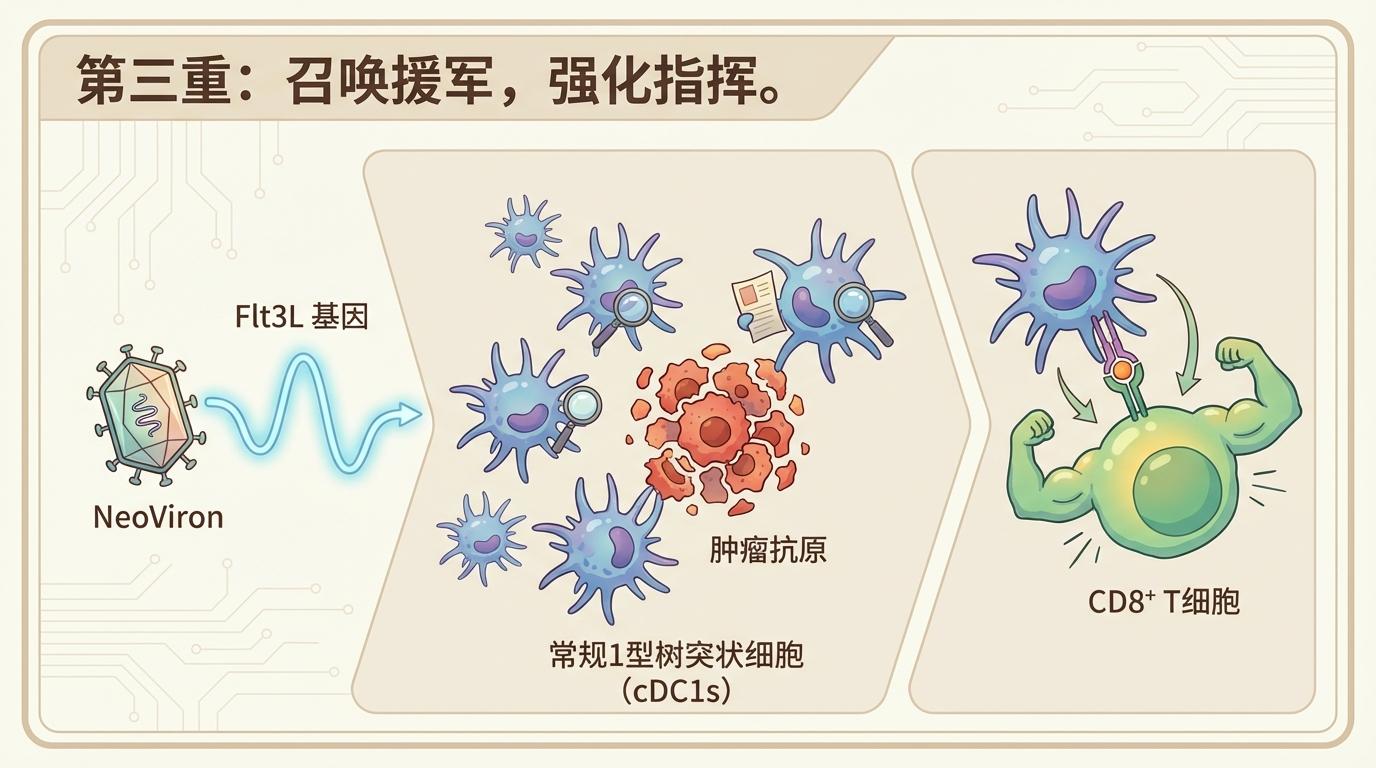
这项研究最令人振奋的发现之一,是NeoViron与抗PD-1疗法联用后的深远影响。这种联合疗法不仅增强了CD8+ T细胞的直接杀伤力,更重要的是,它成功扩增了两类特殊的T细胞亚群:组织驻留记忆T细胞(Trm) 和 干细胞样T细胞(Tstem)。
CD69+ CD8+ 组织驻留记忆T细胞(Trm) 就像是驻扎在曾经的战场上的“哨兵”。它们不再全身循环,而是长期“定居”在肿瘤组织原位,时刻警惕着任何复发的迹象,一旦发现残余或新生的癌细胞,便能迅速发起攻击。这完美解释了NeoViron为何能有效阻止肿瘤转移。
TCF1+ CD8+ 干细胞样T细胞(Tstem) 则像是免疫系统的“后备军工厂”。它们具有强大的自我更新和分化能力,能源源不断地补充效应T细胞,确保了抗肿瘤免疫反应的持久性。这为实现对癌症的长期控制乃至根除提供了可能。
通过单细胞测序分析,研究团队清晰地描绘出这条免疫激活路径:干细胞样T细胞在NeoViron的刺激下,分化为具有超强细胞毒性的组织驻留记忆T细胞,从而构建起一道坚固而持久的抗癌防线。
人类利用微生物对抗癌症的历史可以追溯到一个多世纪前。19世纪末,医生威廉·科利(William B. Coley)观察到细菌感染能让一些患者的肿瘤消退,从而开创了“科利毒素”疗法。这便是“以毒攻毒”思想的雏形。然而,直到合成生物学和基因编辑技术飞速发展的今天,我们才真正有能力将病毒和细菌从不可控的“毒物”,改造为可设计、可编程的“智能活药”。
在此之前,新抗原疫苗(如合成长肽、mRNA疫苗)在高突变肿瘤中已显示出疗效,但在“冷肿瘤”中却因抗原稀少、递送效率低下而举步维艰。NeoViron的出现,巧妙地利用溶瘤病毒作为载体,一次性解决了新抗原的“生产”和“递送”两大难题,实现了“1+1>2”的效果。
NeoViron的成功,为攻克“冷肿瘤”这一免疫治疗的“硬骨头”提供了全新的、极具潜力的通用平台。它不仅为肝内胆管癌等低突变肿瘤带来了曙光,其设计理念也可能适用于胰腺癌等其他难治性癌症。
当然,从动物模型走向临床应用,仍有漫长的道路要走。如何实现病毒的全身性、靶向性递送,如何克服人体内可能存在的预存抗体,以及如何筛选出最适合这种疗法的患者,都是未来需要解决的关键问题。但无论如何,这项研究已经清晰地指明了方向:通过精准的生物工程设计,我们可以主动为肿瘤“画像”,指挥免疫系统发起一场有的放矢的歼灭战。这不仅是对现有免疫疗法的有力补充,更可能开启一个由“智能活药”主导的个性化癌症治疗新纪元。
点击催更,成为大圆镜下一个视频选题!