对抗知识焦虑,从看懂这条开始
App 下载
中年才发病的怪病,病根在出生头7天
名古屋大学|CAG序列扩增|雄激素受体基因|肯尼迪病|脊髓延髓肌萎缩症|罕见遗传病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
名古屋大学|CAG序列扩增|雄激素受体基因|肯尼迪病|脊髓延髓肌萎缩症|罕见遗传病|医学健康
想象一下:一个人四十岁时开始肌肉萎缩、握不住杯子,医生却告诉你,他的病在出生第1天就已经启动了。这不是科幻设定,而是脊髓延髓肌萎缩症(SBMA,又称肯尼迪病)的真实病理。这种只找中年男性的遗传病,曾让医生困惑了几十年——明明症状到中年才显现,为什么患者血液里的异常指标早在确诊前十年就悄悄变化?直到日本名古屋大学的团队盯着小鼠的‘新生儿期’做了实验,才撕开了这个时间差的真相。
SBMA的病根是雄激素受体(AR)基因的CAG序列异常扩增——简单说就是一段遗传密码重复得太多,造出了带毒性的突变蛋白。过去所有人都以为,这些蛋白要到中年雄激素水平稳定后才会作乱,但实验结果推翻了这个想当然的假设。
研究者用携带人类突变AR基因的小鼠做实验,在出生第1天和第7天解剖雄性小鼠的脊髓,惊讶地发现运动神经元的细胞核里已经堆满了突变AR蛋白。更关键的是,这事和新生儿期的‘迷你青春期’直接相关——出生后几天里人体会出现一波自然的雄激素小高峰,正是这波激素把原本待在细胞质里的突变蛋白‘拽’进了细胞核。给雌性小鼠补睾酮,同样能诱导突变蛋白入核。
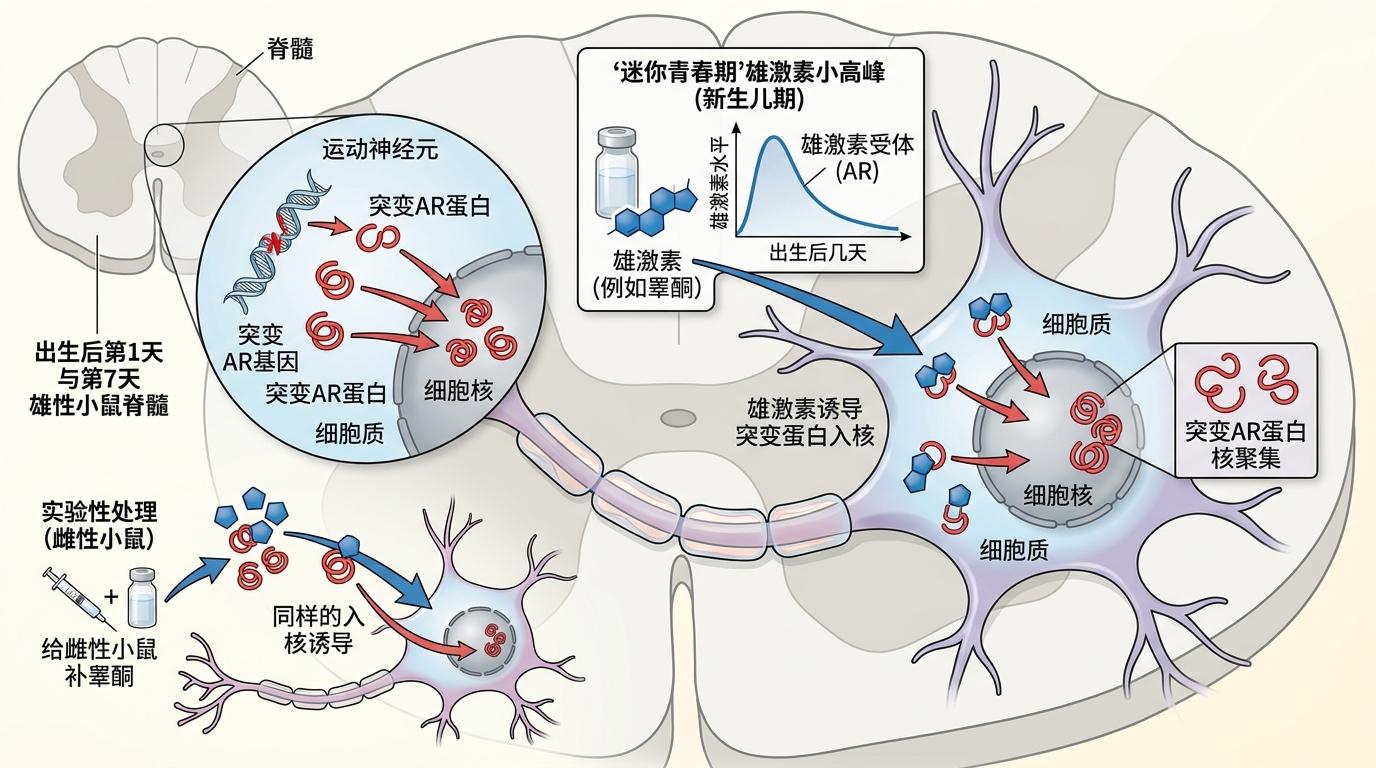
这时候的突变蛋白还没形成晚期才会出现的聚集体,就像小偷刚摸进家门,还没来得及搬空东西——但它已经在最核心的位置安了家。
既然致病蛋白在新生儿期就已启动,那在这个窗口短暂干预,能不能改变中年后的结局?
研究者在小鼠出生第1天做了一次脑室内注射,用的是靶向突变AR的反义寡核苷酸(ASO)——一种能精准‘沉默’特定基因的分子工具。注射后第7天,脊髓里的突变AR蛋白明显减少,第21天就基本恢复正常。但就是这短短几周的抑制,给小鼠的成年期带来了翻天覆地的变化:它们的生存期比对照组延长了近30%,转棒测试的平衡能力、握力测试的肌肉强度都显著改善,脊髓运动神经元的萎缩程度也大幅减轻。
更意外的是,这些改善和晚期的蛋白聚集体无关——治疗组和对照组小鼠到13周龄时,脊髓里的聚集体含量并没有差别。这说明真正决定疾病走向的,是早期致病蛋白在细胞核里的‘潜伏’,而非晚期才出现的可见病变。
后来团队又找到了更精准的靶点:突变AR会诱导转录因子REST的剪接异常,产生一种叫Rest4的截短蛋白——它就像没装刹车片的刹车,原本该被REST抑制的谷氨酸能突触基因被异常激活,导致运动神经元过度兴奋。针对Rest4的ASO同样能在新生儿期一次注射,就让小鼠成年后的运动能力明显提升。
过去SBMA被归为运动神经元病,但新的研究发现,肌肉才是最早被攻击的靶点。在小鼠模型中,6个月大的突变小鼠已经出现肌肉肌力下降、纤维萎缩,但此时脊髓里的运动神经元数量还没明显减少。
突变AR蛋白会直接在肌肉细胞里积累,破坏线粒体功能、干扰代谢通路,甚至影响肌肉干细胞的修复能力。更关键的是,肌肉病变会反过来加剧神经损伤——肌肉产生的神经营养因子减少,相当于给运动神经元断了‘补给’。这也解释了为什么单独针对肌肉的ASO治疗,也能显著改善小鼠的症状:它打断了‘肌肉损伤→神经退化’的恶性循环。
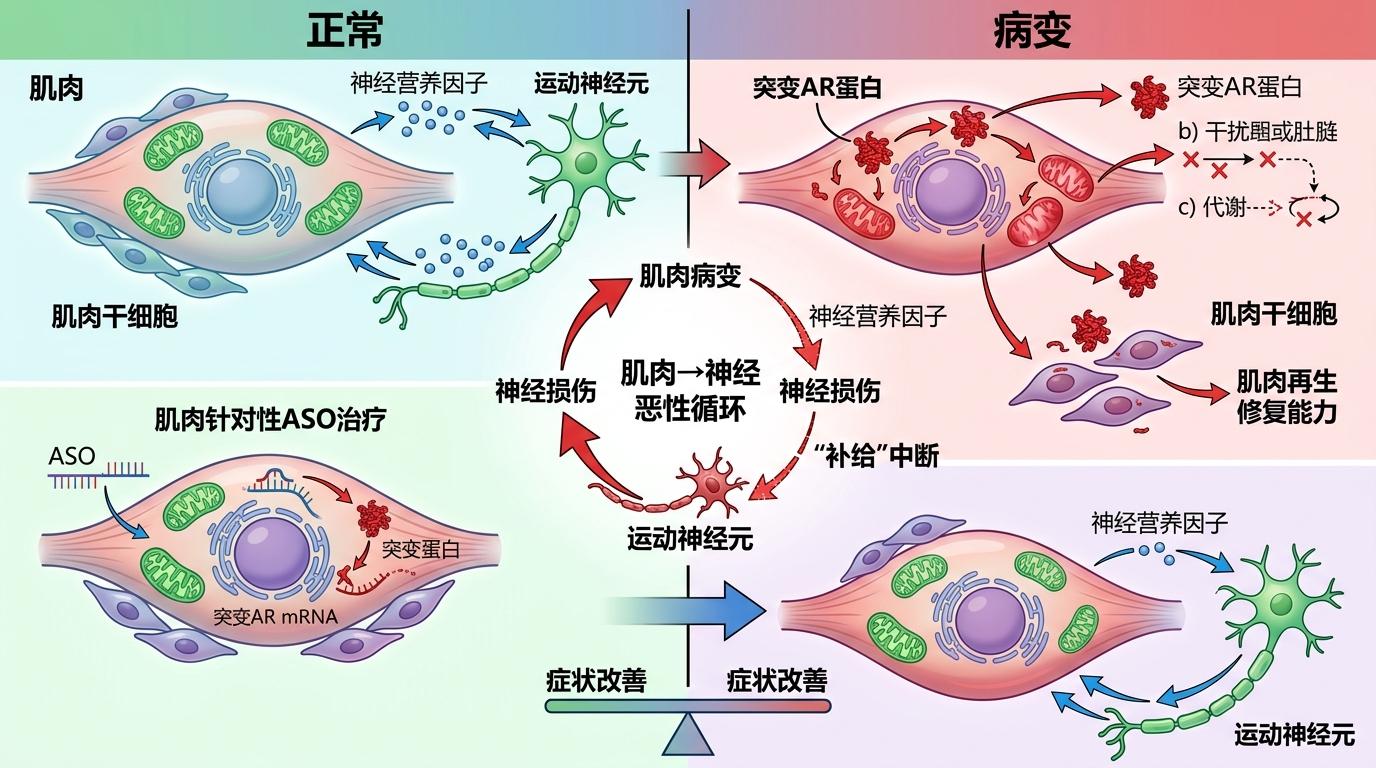
当然,这种早期干预的临床转化还面临重重挑战:ASO需要脑室内注射的侵入性操作、新生儿基因筛查的伦理争议、长期安全性的验证……但至少,我们终于跳出了‘中年发病就从中年治疗’的惯性思维。
我们总以为疾病是‘突然发生’的——四十岁的肌肉萎缩、六十岁的认知下降,都是某一天突然找上门的麻烦。但SBMA的研究撕开了这个假象:很多慢性病的种子,早在生命最初的几天、几个月就已经埋下,只是被身体的代偿机制暂时掩盖了。
早期干预的意义,从来不是‘治愈’,而是在疾病还处于‘可逆阶段’时,把它的轨迹掰回正轨。就像给刚发芽的歪树苗轻轻扶一把,它就能长成直挺的大树。
早干预一步,晚发病十年。 这不仅是SBMA给我们的启示,更是所有慢性遗传病未来的治疗方向。当我们学会在症状出现前几十年就瞄准病根,那些曾经无解的‘中年病’,或许会变得不再可怕。