对抗知识焦虑,从看懂这条开始
App 下载
冠心病用药的暗线:防血栓也要护肠胃
用药风险|消化道出血|阿司匹林|抗血小板药|冠心病患者|心脑血管疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
用药风险|消化道出血|阿司匹林|抗血小板药|冠心病患者|心脑血管疾病|医学健康
上海的一位冠心病患者拿到处方时,可能没意识到这张纸背后藏着一场精准的「风险博弈」:他要吃的抗血小板药能堵住血管里的血栓,却可能在肠胃上凿出漏洞——数据显示,双联抗血小板治疗会让消化道出血风险翻2到3倍。医生开的药里,有没有为这场博弈补上关键的「防护盾」?这不仅是一张处方的问题,更是每一位冠心病患者都要面对的「用药选择题」。
我们可以把血管里的血小板想象成一群随时准备抱团的「抢修工人」:当冠状动脉的粥样斑块破裂,它们会立刻聚集形成血栓,堵住血管引发心梗——抗血小板药就是给这些「工人」踩刹车。
阿司匹林是最经典的「刹车踏板」,它不可逆地锁住血小板里的环氧合酶,让血小板失去聚集的信号;氯吡格雷、替格瑞洛这类P2Y12抑制剂则是「拆走了抱团的工具」,阻断血小板之间的连接信号。对于急性冠脉综合征或做过支架的患者,医生通常会开两种药联合的「双重抗血小板治疗」,把血栓风险降到最低。
但这副「刹车」会误伤肠胃。阿司匹林会直接抑制胃黏膜分泌保护性的前列腺素,让胃酸像没了防护罩的子弹,直接侵蚀黏膜;氯吡格雷虽不直接伤黏膜,却会抑制血小板释放修复因子,让肠胃的小伤口迟迟无法愈合。数据显示,双重抗血小板治疗的患者中,30天内消化道出血的概率可达1.3%,而有溃疡病史的高危患者,这个风险会飙升到12%。
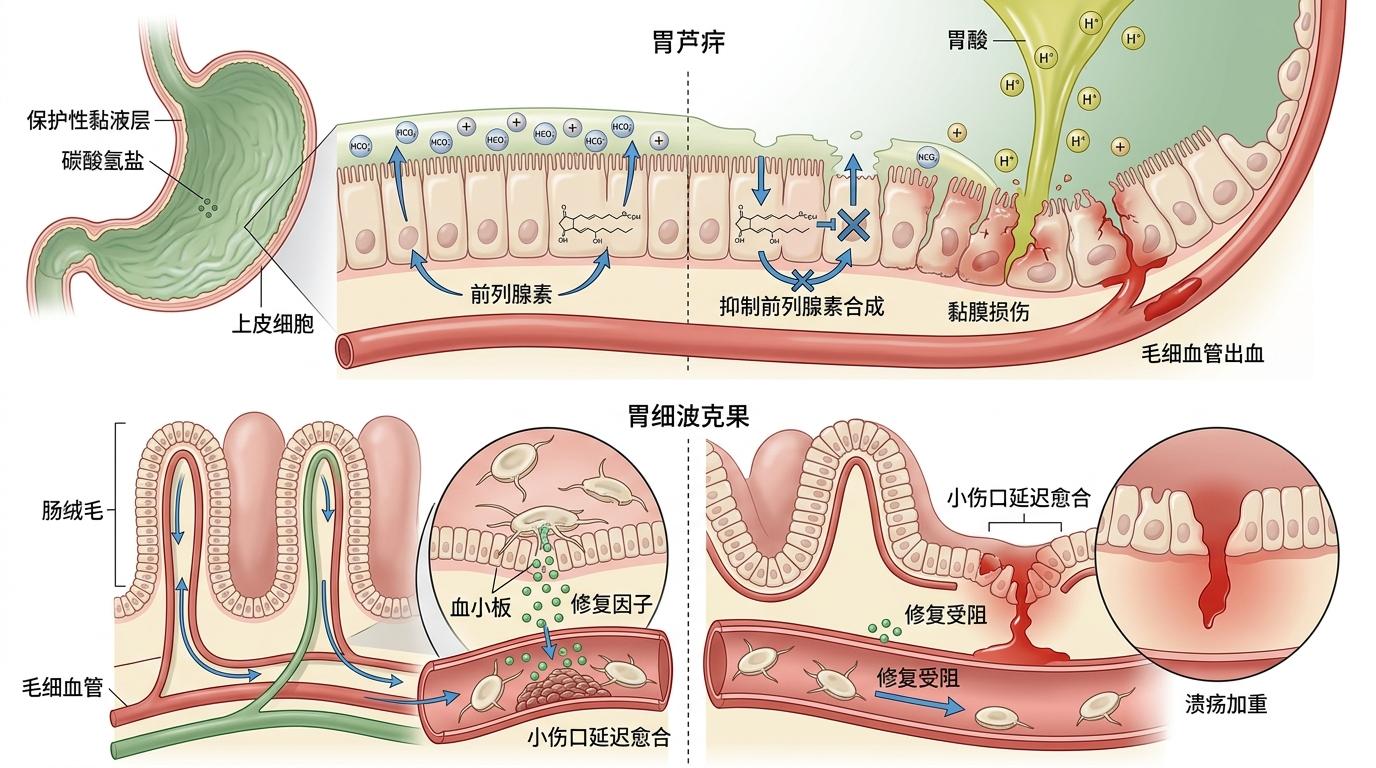
当抗血小板药的「双刃剑」挥向肠胃时,质子泵抑制剂(PPI)就是最有效的「防护盾」——它能直接关掉胃壁上的「胃酸开关」,让胃内酸度大幅降低,给受损的黏膜争取愈合时间。
但选「盾」的学问不小。早年有研究担心,奥美拉唑这类PPI会和氯吡格雷竞争肝脏里的CYP2C19酶,影响氯吡格雷的活化效果,削弱抗血栓作用。但后续大规模临床试验(如COGENT)证实,这种影响在临床上几乎可以忽略,PPI带来的出血风险降低收益远大于潜在的血栓风险。
更值得关注的是,不同PPI对酶的影响差异很大:奥美拉唑、埃索美拉唑对CYP2C19的抑制作用较强,而泮托拉唑、雷贝拉唑的影响几乎可以忽略。因此临床指南明确建议,需要联合氯吡格雷的患者,优先选择泮托拉唑这类「低干扰型」PPI。
但PPI也不是万能的。它对上消化道出血的防护效果明确,但对小肠出血的作用有限;长期滥用还可能带来肠道感染、骨质疏松等风险——临床原则是「按需使用」:有溃疡史、高龄、联用抗凝药的高危患者必须用,低风险患者则无需常规服用。
过去医生开抗血小板药,多是「按指南套方案」:支架术后双联治疗12个月,然后阿司匹林单药维持。但现在的临床思维已经转向「个体化权衡」——每一位患者的血栓风险和出血风险都需要单独计算。
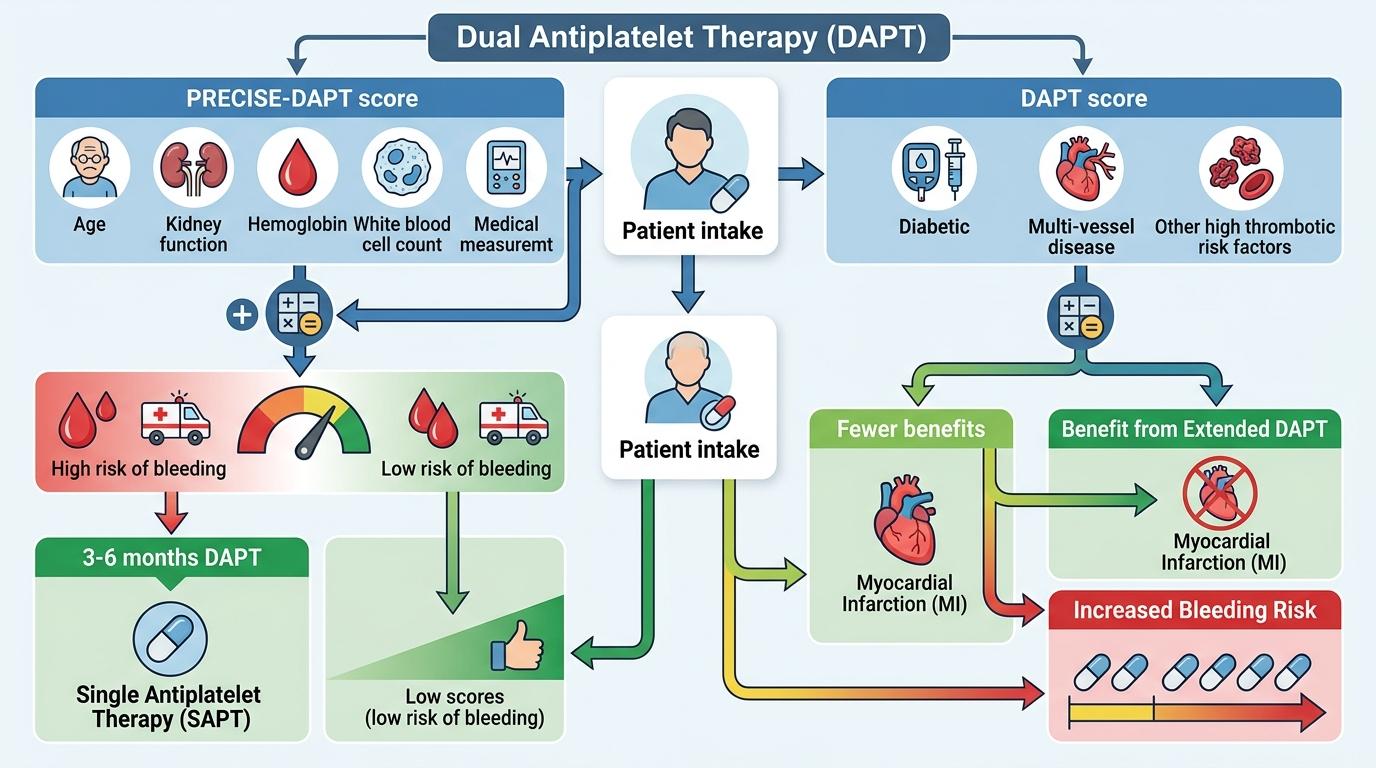
比如PRECISE-DAPT评分,会根据患者的年龄、肾功能、血红蛋白等5项指标打分,分数越高出血风险越大,这类患者可能只需3到6个月的双联治疗,就可以换成单药;而DAPT评分则会判断患者是否能从延长双联治疗中获益——糖尿病、多支血管病变的高血栓风险患者,延长治疗能减少心梗,但出血风险也会上升。
基因检测也开始进入临床:亚洲人群中约30%携带CYP2C19功能缺失基因,这类患者吃氯吡格雷的活化效果会大打折扣,血栓风险更高,医生会直接换成无需肝脏活化的替格瑞洛;而对于出血风险极高的患者,甚至可以考虑跳过阿司匹林,只用替格瑞洛单药治疗——最新的STOPDAPT-2研究证实,这种方案在减少出血的同时,血栓预防效果并不逊色。
当我们把视线从药物机制拉回患者本身,会发现冠心病的用药从来不是「选最好的药」,而是「选最适合的平衡」。那些印在处方上的药名,背后是医生对血栓与出血、疗效与安全的反复权衡。
更重要的是,患者自己也是这场平衡的参与者:不要自行停药,也不要隐瞒肠胃病史;如果出现黑便、胃痛等症状,要第一时间告知医生——毕竟,真正的合理用药,从来不是医生单方面的决策,而是医患之间共同的「风险共担」。
金句:用药的本质,是在获益与风险间找平衡。