
4 个月前

4 个月前
对于一位缺血性卒中的幸存者而言,最漫长的战斗或许并非发生在急救室,而是在那之后无数个寂静的日夜里。当生命的警报解除,身体却仿佛成了一座被遗弃的城市,曾经熟悉的指令无法传达,记忆的片段变得模糊,简单的抬手、行走也成为艰巨的挑战。这背后,是一场发生在脑内“沉默的战场”上的持续破坏——大脑白质的损伤。
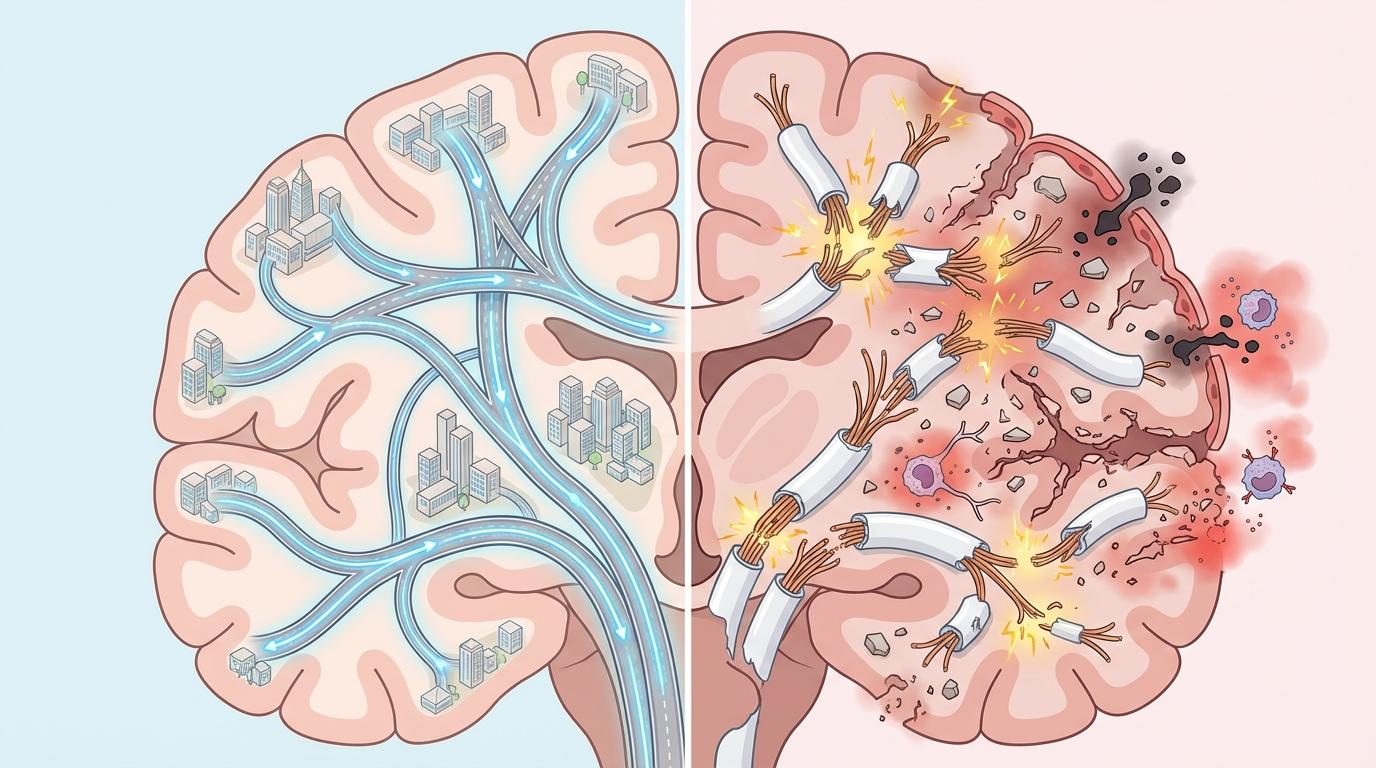
大脑白质,如同连接城市各个角落的庞大高速公路网络,由无数被髓鞘包裹的神经轴突构成,负责在不同脑区之间高速传递信息。缺血性卒中,就像一场突如其来的大地震,不仅摧毁了“城市中心”(灰质神经元),更导致了约占梗死体积一半的“交通干线”(白质)的崩塌。髓鞘剥落,轴突裸露,神经信号的传输就此中断或“短路”。这场破坏引发了连锁反应:免疫细胞被激活,释放大量炎症因子,形成一片不利于修复的“焦土”;血脑屏障这一“城墙”也被攻破,有害物质涌入,进一步加剧损伤。多年来,如何在这片废墟之上重建交通,修复白质,一直是神经科学领域面临的核心瓶颈,也是无数患者重返正常生活的最大障碍。
转机,来自一群肉眼无法看见的“微小信使”——外泌体。如果说干细胞是强大的“工程母舰”,那么外泌体就是它释放出的、装载着修复指令和关键物资的“纳米级无人机”。这些直径仅有30-150纳米的囊泡,由干细胞分泌,内部包裹着蛋白质、核酸等生物活性分子。它们是细胞间通讯的天然邮差,而它们的出现,为“无细胞治疗”带来了革命性的希望。
与直接移植干细胞相比,外泌体拥有无可比拟的优势:
科学家们猜想,这些微小的信使,或许就是那支能够精准空投到大脑战场,并启动重建程序的特种部队。
近日,国际权威期刊《脑血流与代谢杂志》(J Cereb Blood Flow Metab)上发表的一项研究,将这一猜想变成了确凿的证据。研究团队利用牙髓干细胞来源的外泌体(DPSCs-Exos),在模拟缺血性卒中的小鼠模型上,上演了一场精彩的“逆转之战”。
研究人员在小鼠大脑缺血后的关键时间点,通过脑室内注射这些外泌体。结果令人振奋:
**功能上,奇迹正在发生。**接受治疗的小鼠,其神经功能得到了显著改善。在精细的运动测试中,它们在平衡木上保持平衡的时间显著延长,行走时的失误步数大幅减少。在认知测试中,它们的工作记忆和识别记忆能力也明显提升,有效缓解了由缺血引发的学习记忆障碍。这表明,外泌体不仅修复了运动控制,也重建了认知功能。
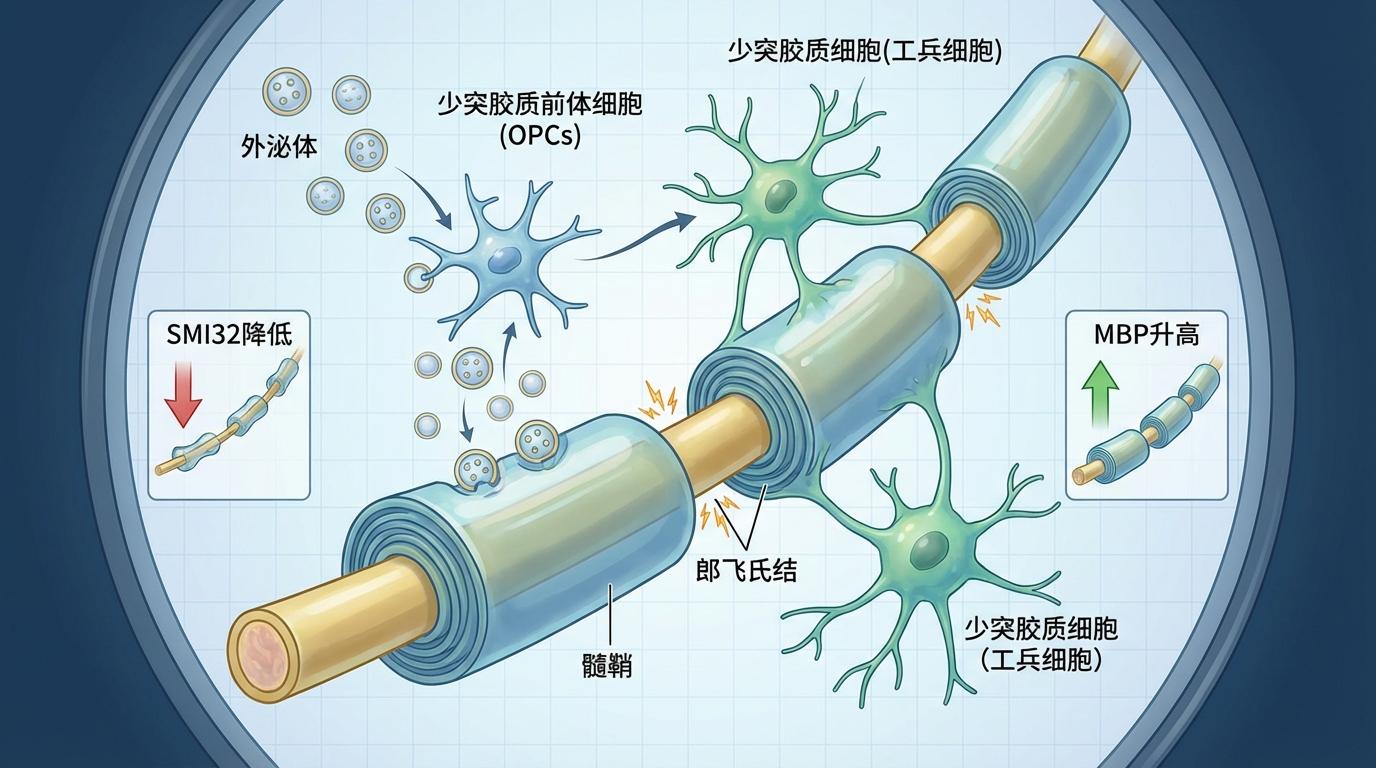
**形态上,证据坚实有力。**通过高倍显微镜和分子检测,科学家们得以窥见大脑内部的微观变化。在治疗组小鼠的受损脑区,代表髓鞘健康的标志物“髓鞘碱性蛋白”(MBP)水平显著升高,而代表白质损伤的标志物SMI32则明显降低。更令人惊叹的是,透射电镜下的图像显示,神经轴突重新被厚实的髓鞘包裹,髓鞘化轴突的比例大幅增加,神经信号传导的关键结构“郎飞氏结”数量也增多了。这一切都指向一个结论:外泌体成功唤醒了大脑内源性的修复力量,促使负责制造髓鞘的“工兵细胞”——少突胶质前体细胞(OPCs)——分化成熟,并高效地投入到修复工作中。
这次研究最核心的突破,在于它没有停留在“有效”的层面,而是像一位侦探,层层深入,最终揪出了外泌体发挥作用的完整分子通路——一个被命名为 Myl9-PRMT5-ID2 的信号轴。
整个过程如同一场精密的特工行动:
研究团队通过基因敲除实验进一步证实,一旦拿掉PRMT5这个“将军”,外泌体的所有修复效果便荡然无存。这无可辩驳地证明了,Myl9-PRMT5-ID2轴正是牙髓干细胞外泌体重启大脑白质修复程序的核心密码。
这项研究的意义远不止于一篇高水平论文。它首次清晰地描绘出牙髓干细胞外泌体修复白质的完整分子蓝图,为开发针对性的卒中后遗症治疗药物提供了全新的、精准的靶点。它证实了外泌体作为一种“无细胞”生物制剂,在安全性、有效性和临床转化潜力上,都展现出超越传统干细胞疗法的巨大前景。
然而,将这份希望转化为惠及全球数千万卒中患者的现实,依然道阻且长。横亘在面前的挑战是真实存在的:
大脑白质的损伤,曾是卒中幸存者面前一道难以逾越的鸿沟。而今,源自牙髓干细胞的微小外泌体,正以其精准而强大的力量,在这道鸿沟上架起一座通往康复的桥梁。这项开创性的研究,让我们得以窥见细胞内部那令人惊叹的精密调控网络,也让我们触摸到了未来神经修复疗法的曙光。
从一颗废弃的智齿,到一个受损大脑的重生,科学的探索正在将看似不可能的想象变为现实。这条从实验室通往临床的道路或许充满挑战,但每一步坚实的进展,都在为那些在寂静中挣扎的患者,带去重获新生的希望——希望有一天,他们大脑中沉寂的高速公路能够再次贯通,让思想与指令自由驰骋。
点击充电,成为大圆镜下一个视频选题!