对抗知识焦虑,从看懂这条开始
App 下载
受精即破对称:蛋白质揭示胚胎命运起源
全能性|卵裂球|对称性破缺|细胞命运决定|受精卵|发育生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
全能性|卵裂球|对称性破缺|细胞命运决定|受精卵|发育生物学|生命科学
在发育生物学的经典教科书中,哺乳动物生命的开端常被描绘成一幅完美对称的画卷:一个受精卵,经过第一次分裂,形成两个完全等效的细胞,即卵裂球。它们如同两个拥有相同潜能的双胞胎,共享着一张通往完整生命的蓝图,似乎机会均等,命运未定。几十年来,这种“全能性”和“等效性”的观念一直是理解我们自身起源的基石。然而,如果这幅看似完美的对称画卷,从一开始就是一种精妙的错觉呢?如果决定细胞“天资”高低的第一张牌,在受精那一瞬间就已经发出,我们对生命起点的理解又将发生怎样的颠覆?
2025年12月3日,加州理工学院的Magdalena Zernicka-Goetz团队在顶级期刊《Cell》上投下了一枚重磅炸弹。他们的研究论文Fertilization triggers early proteomic symmetry breaking in mammalian embryos,以前所未有的精度揭示了一个惊人事实:哺乳动物胚胎的对称性,在受精那一刻便已被打破。
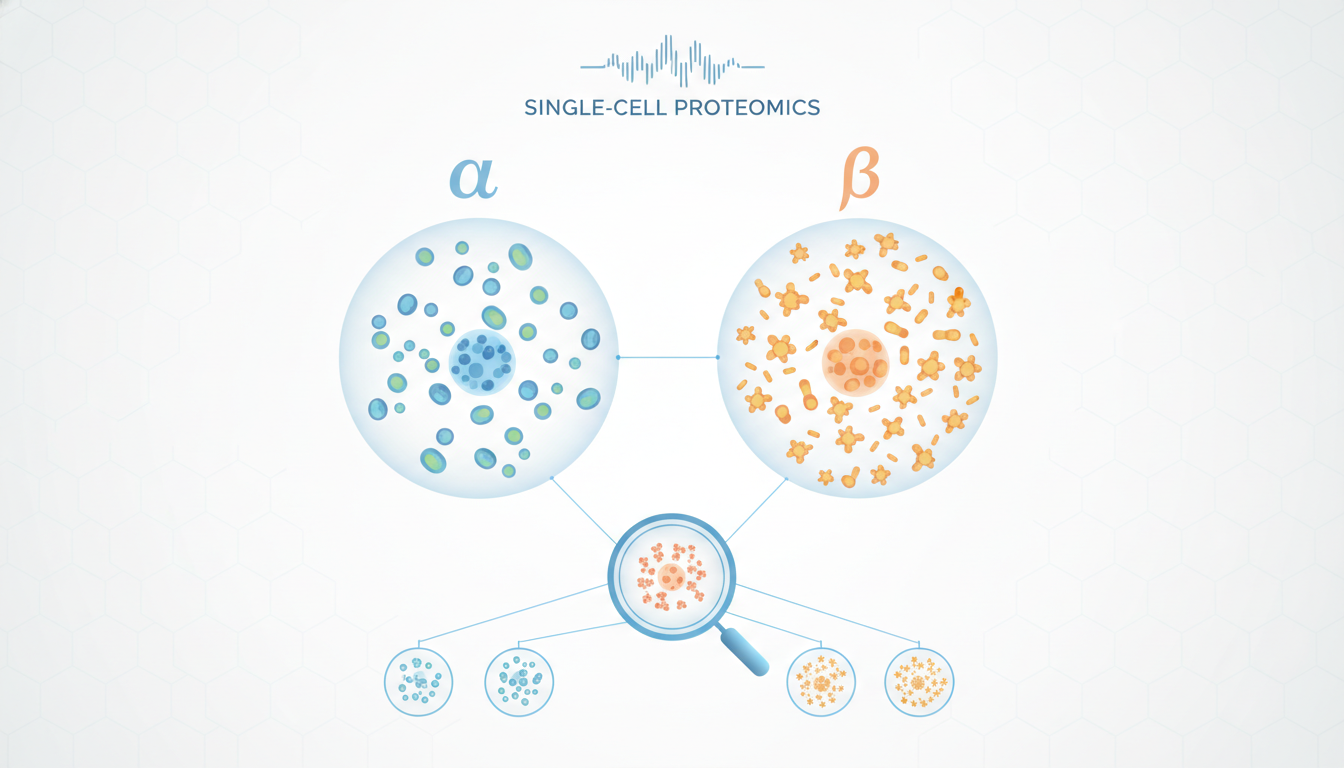
借助尖端的单细胞蛋白质组学技术,研究团队得以窥探小鼠和人类单个卵裂球内部的分子世界。他们发现,2细胞阶段的两个姐妹细胞远非完全相同,而是可以被清晰地分为两种截然不同的蛋白质组状态,他们将其命名为 α 和 β。
这一里程碑式的发现,离不开技术的革命性进步。过去,蛋白质组学研究依赖于将成百上千个胚胎混合在一起的“批量分析”,这种方法虽然能提供整体信息,却也无情地抹平了细胞间的个体差异。这就好比试图通过分析整个城市所有居民的平均身高,来理解每个人的高矮胖瘦,重要的个体信息消失在了平均值之中。
Zernicka-Goetz团队采用的 SCoPE2(单细胞蛋白质组学) 等前沿技术,则像一台超高分辨率的显微镜,首次让科学家能够逐一审视每个细胞的蛋白质构成。这项技术克服了单个细胞内蛋白质含量极其微弱的巨大挑战,使我们得以捕捉到早期胚胎中微妙而关键的异质性。正是这“看见”的能力,才让隐藏在对称表象之下的生命“预设程序”得以曝光。这一突破不仅是发育生物学的胜利,也是分析化学和生物工程学协同创新的典范。
α和β细胞内不同的蛋白质组合,并非仅仅是标示身份的“旗帜”,更是实实在在调控细胞命运的“方向盘”。为了证明这一点,研究团队进行了一系列功能性实验,通过敲低特定蛋白质的表达,观察细胞命运的变化:
这些实验有力地证明,受精瞬间建立的蛋白质组不对称,通过一系列精确的分子调控网络,直接驱动了哺乳动物生命中第一次细胞命运的偏离,为全能性的逐步、不平等丧失提供了坚实的分子起源证据。
这项发现的意义远远超出了实验室的范畴,它深刻地改变了我们对生命开端的理解,并为现实世界带来了新的启示。
对科学界的影响:它颠覆了哺乳动物发育始于“等效细胞”的传统教条,将决定论的时刻大大提前。生命的发育并非完全随机和可塑,而是在一开始就存在着由物理事件(受精)引发的分子层面的偏好。这一新范式将激发对早期胚胎发育、细胞竞争和全能性调控机制的全新研究浪潮。
对社会的影响:这一发现对辅助生殖技术(ART),尤其是体外受精(IVF),具有巨大的潜在价值。目前,IVF中胚胎的选择主要依赖于形态学评估,主观性较强且预测成功率有限。未来,通过检测早期胚胎中的α/β细胞特异性蛋白质标志物,或许能开发出一种更精准、更客观的胚胎筛选方法,从而挑选出最具发育潜力的胚胎进行移植,显著提高IVF的成功率,为无数不孕不育家庭带来新的希望。
尽管Zernicka-Goetz团队的研究打开了一扇全新的窗户,但窗外的风景依然广阔而神秘。一系列关键问题仍等待着科学家们去解答:
回答这些问题,需要更先进的单细胞多组学技术、更高分辨率的活细胞成像,以及跨学科的紧密合作。我们正站在理解生命起源新纪元的门槛上。这项研究告诉我们,生命的序曲并非一首和谐的齐唱,而是一段从受精瞬间就开始的、充满微妙差异的二重奏。正是这种最初的不对称,孕育了后续发育过程中所有的复杂性与可能性,谱写出独一无二的生命乐章。