对抗知识焦虑,从看懂这条开始
App 下载
心脏瓣膜老化的元凶找到了:NAD+代谢的双重背叛
华中科技大学|内皮细胞|心脏瓣膜老化|NAD+分子|钙化性主动脉瓣疾病|心脑血管疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
华中科技大学|内皮细胞|心脏瓣膜老化|NAD+分子|钙化性主动脉瓣疾病|心脑血管疾病|医学健康
你可能没听过钙化性主动脉瓣疾病,但它正悄悄盯上每三个65岁以上老人中的一个。这种病从心脏瓣膜悄悄变硬开始,到出现胸闷、晕厥时,两年内死亡率就会飙升到50%——比很多癌症还凶险。过去我们总以为这是心脏用久了的「正常磨损」,直到华中科技大学等团队的新研究撕开了真相:不是瓣膜老了,是一种叫NAD+的关键分子,在心脏里发生了「双重背叛」。这背后的机制,藏着逆转这种老年病的第一个可能。
我们可以把心脏瓣膜想象成一个精密的「单向门」,内皮细胞就是门的「密封条」,负责维持瓣膜的光滑和稳定。而NAD+就是给这个密封条供能的「电池」——它是细胞里管能量、抗炎症的核心分子,会随着年纪增长自然下降。
研究人员发现,老年瓣膜的内皮细胞里,负责合成NAD+的关键酶NAMPT活性骤降,相当于「电池工厂」停工了。没有足够的NAD+,内皮细胞的「抗炎开关」SIRT1就会失灵,核因子NF-κB开始疯狂释放炎症信号,就像密封条先破了个洞,引来一堆「维修工」。
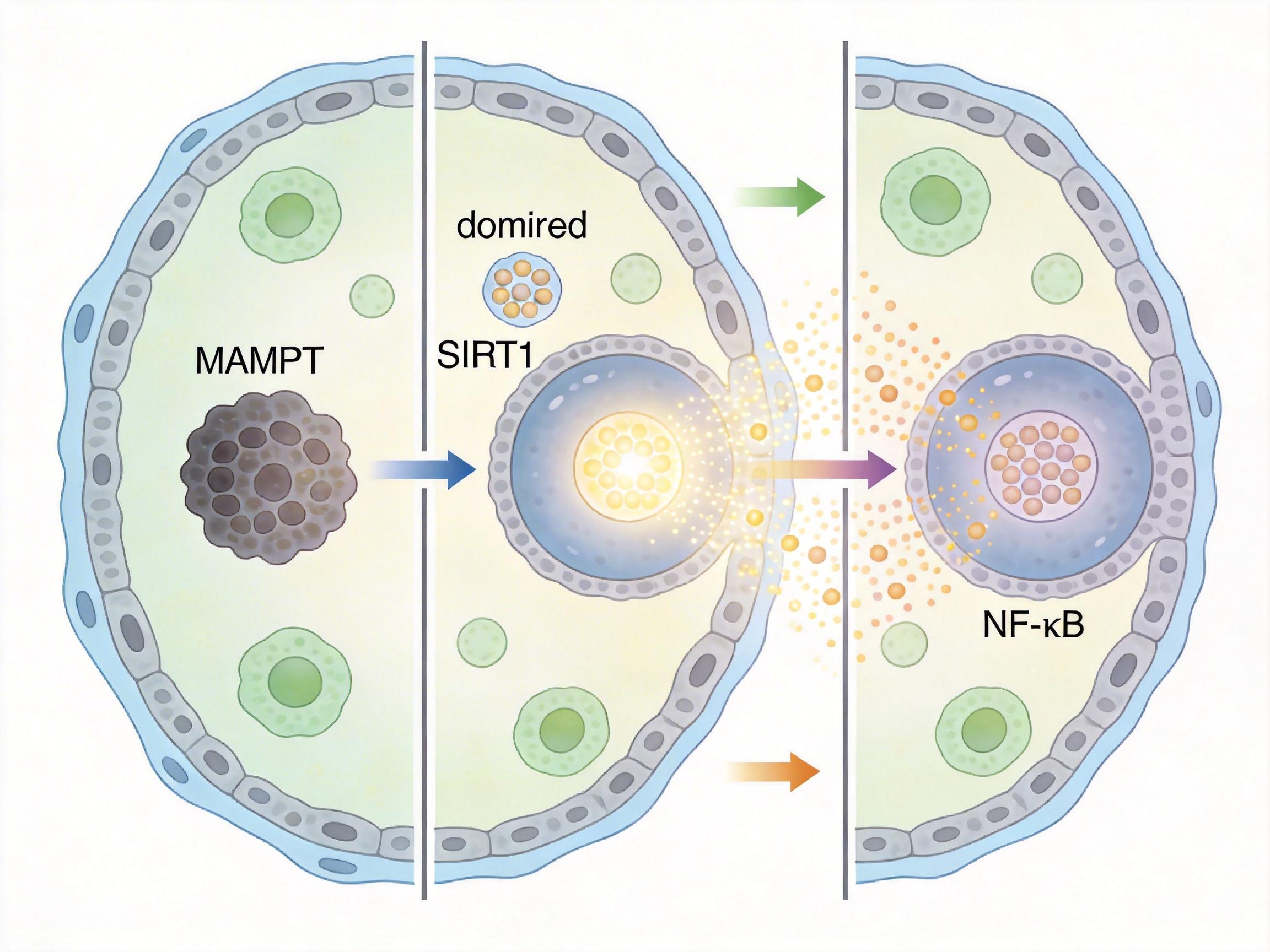
但这些叫巨噬细胞的「维修工」,才是真正的麻烦制造者。它们的NAMPT活性反而异常升高,不仅自己分泌大量促炎因子,还会释放胞外NAMPT——一种能激活炎症通路的「信号弹」,把局部炎症越烧越旺,同时还会啃食瓣膜的胶原蛋白基质,让瓣膜从「磨损」变成「主动崩溃」。
这不是两个独立的问题,而是一套精密又致命的「恶性循环」:内皮细胞缺NAD+引发炎症,巨噬细胞靠高NAMPT放大炎症,两者形成了「分隔的NAD+回路」——一个细胞缺能,一个细胞过度产炎,把瓣膜的炎症和基质破坏牢牢绑在了一起。
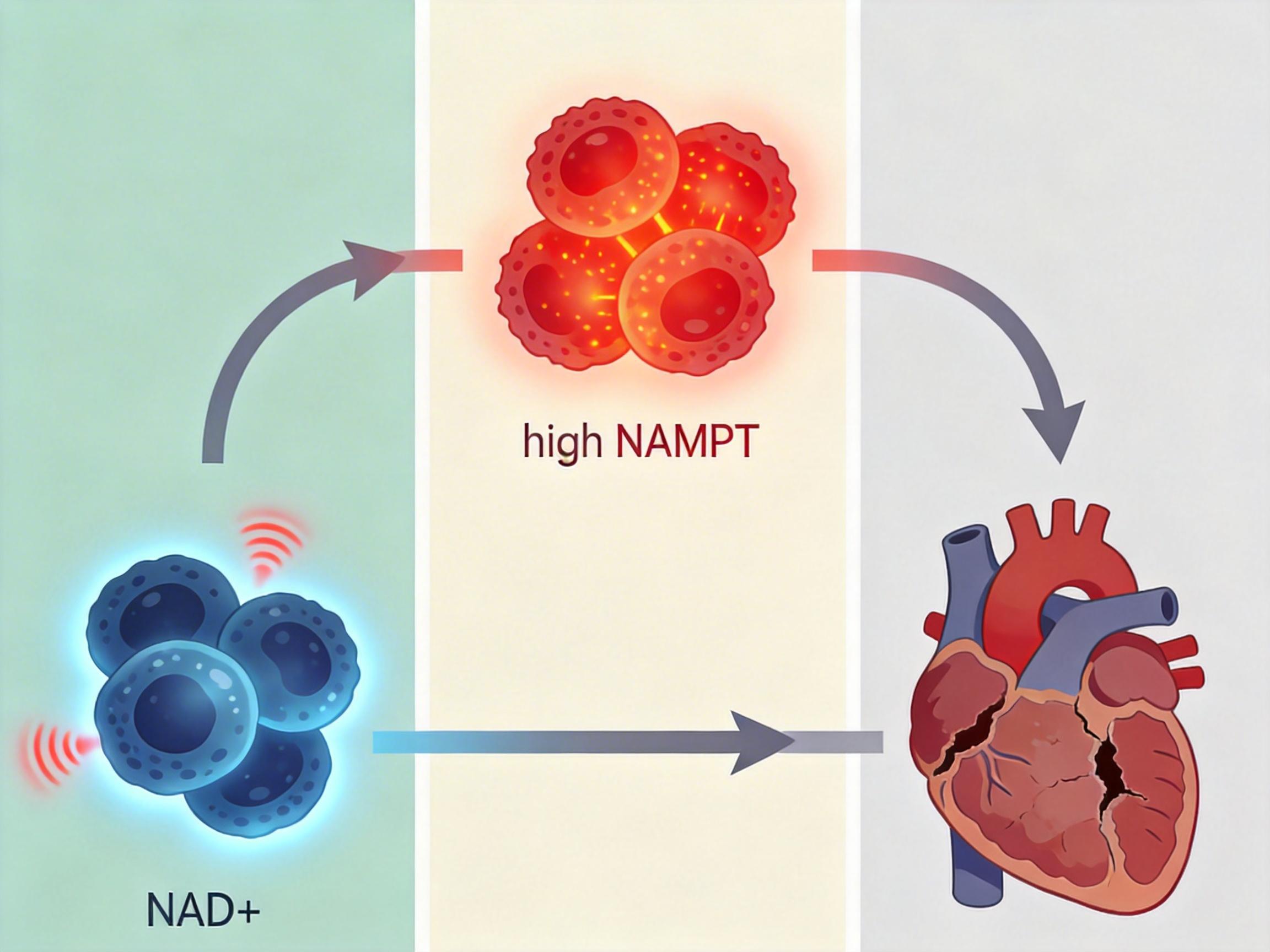
研究团队用单细胞测序技术,精准描绘了两种细胞的NAD+代谢差异:内皮细胞的NAMPT表达量比年轻人低了近40%,而巨噬细胞的NAMPT水平却高出3倍。更关键的是,巨噬细胞还会分泌胞外NAMPT,通过TLR4受体再次激活内皮细胞的炎症反应,相当于「维修工」一边补洞一边在洞旁边凿新坑。
他们在小鼠模型里验证了这个逻辑:给年轻小鼠抑制内皮NAMPT,很快就出现了瓣膜钙化;而给老年小鼠补充NAD+前体NMN,能让瓣膜的NAD+水平恢复60%,炎症反应减少45%,钙化进程被显著延缓。但如果等到瓣膜已经硬化再补,效果就微乎其微——这个治疗有严格的「时间窗」。
这也是研究最值得警惕的地方:NAD+不是万能的补剂,它的作用完全取决于细胞类型。如果不分青红皂白地给全身补NAD+,反而可能让巨噬细胞的炎症反应更剧烈,相当于给「凿坑的维修工」递了一把更锋利的锤子。
目前的思路是「双向调控」:给内皮细胞补NAD+前体,比如早期口服NMN;同时抑制巨噬细胞的胞外NAMPT信号,比如用中和抗体阻断TLR4通路。但这还停留在动物实验阶段,人体临床试验需要解决两个关键问题:一是如何让NMN精准到达心脏瓣膜,而不是被肝脏、肌肉等组织抢着吸收;二是如何避免抑制NAMPT影响巨噬细胞的正常免疫功能——毕竟它们还是身体里重要的「免疫卫士」。
更现实的是,NAD+补充剂的市场已经炒得火热,但这项研究给了我们一个冷静的提醒:没有任何一种抗衰老补剂是「通用神药」,它的效果取决于你补的时机、剂量,以及身体的具体状态。
当我们终于把「心脏磨损」这个模糊的概念,拆解成两种细胞的NAD+代谢失衡时,才发现衰老从来不是一个笼统的「整体老化」,而是身体里无数个细胞「各自为政」的结果。有的细胞缺能罢工,有的细胞过度工作添乱,最后凑成了一场看似「自然」的疾病。
「衰老不是均匀的,治疗也该精准。」这句话不仅适用于心脏瓣膜病,也适用于所有和年龄相关的疾病。未来的抗衰老研究,不会是找到一种「万能补剂」,而是像拆钟表一样,精准修复每个出问题的齿轮——而这项研究,就是给心脏这个精密钟表,找到了第一个可以撬动的齿轮。