对抗知识焦虑,从看懂这条开始
App 下载
小脑惊天秘密:FOXP基因如何塑造人类认知与自闭症风险?
神经元分布|自闭症风险|认知功能|FOXP基因|小脑|神经生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
神经元分布|自闭症风险|认知功能|FOXP基因|小脑|神经生物学|生命科学
在颅腔的后下方,静卧着一个常被误解的脑区——小脑。它的体积仅占大脑的10%,神经元数量却超过了整个大脑皮层,占据了全脑神经元总数的一半以上。长久以来,我们将其功能主要限定在运动协调与平衡控制的“幕后功臣”。然而,这个看似结构均一、功能单一的“小脑”,正逐渐揭示其在语言、社交、情感乃至高级认知功能中的核心作用。一个深刻的谜题随之浮现:一个在显微镜下呈现出高度重复、近乎“晶体”般规整结构的脑区,如何能支撑如此复杂多样的功能?答案,或许就隐藏在细胞诞生之初的遗传密码里。
近日,一项发表于《自然·神经科学》的突破性研究,为我们揭开了这个谜题的关键一角。由美国康涅狄格大学James Y. H. Li研究团队领导的工作,首次系统性地阐明了**FOXP基因家族(Foxp1, Foxp2, Foxp4)**如何像一支精密的“指挥团队”,通过调控小脑中唯一的输出神经元——**浦肯野细胞(Purkinje cells, PCs)**的多样性,从而驱动小脑的发育与进化。这项研究不仅为理解哺乳动物(尤其是人类)显著扩张的小脑半球提供了细胞层面的基础,更对自闭症等神经发育疾病的病理机制提出了颠覆性的新见解。
研究团队利用前沿的单细胞RNA测序技术,深入探索了小鼠胚胎期的小脑。他们发现,在小脑还处于“建设初期”时,本应被视为标准化“砖块”的浦肯野细胞,实际上早已分化为至少11种分子特征迥异的亚型。每一种亚型,都由FOXP基因家族的不同成员以独特的组合方式进行“标记”,如同拥有了独一无二的“基因身份证”。
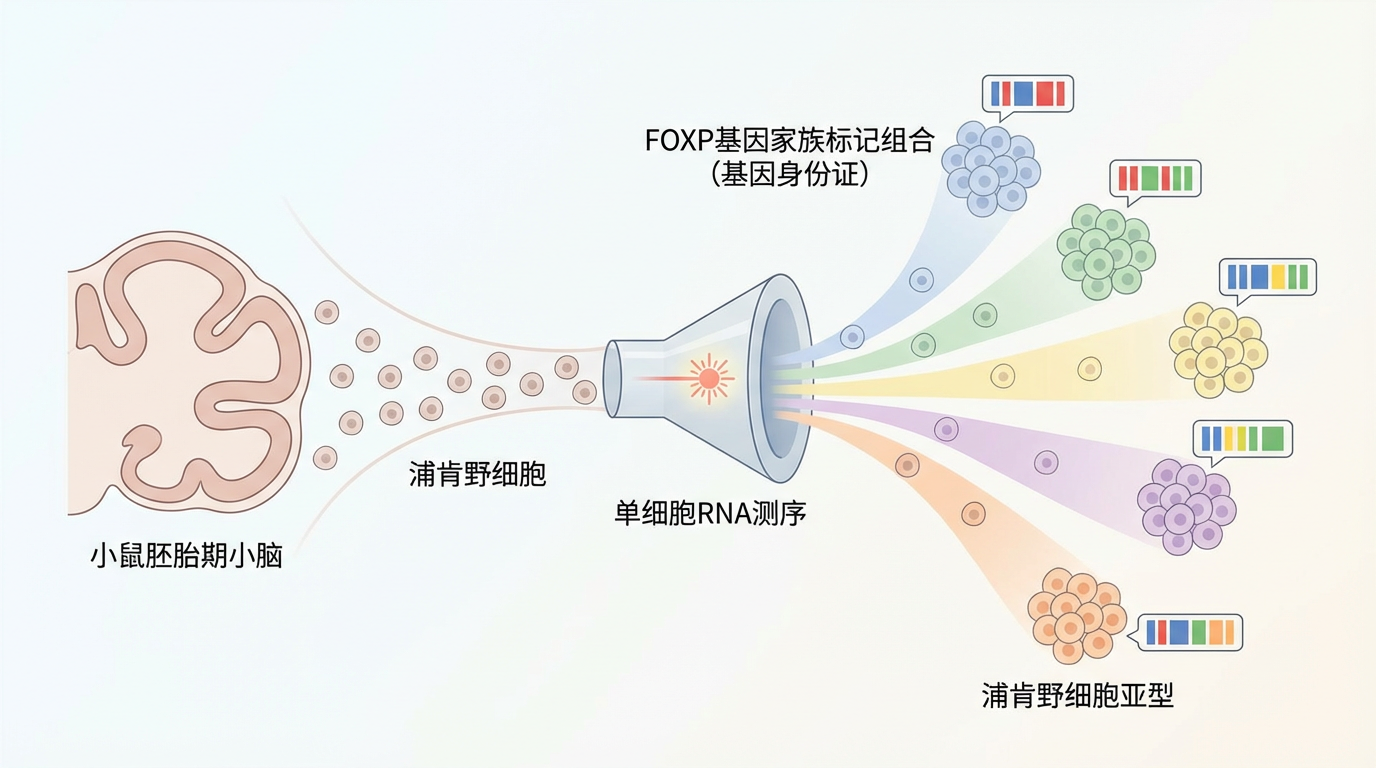
这11种细胞亚型并非随机散落,而是遵循着一张精密的“建筑蓝图”。研究者们开发了一种名为scANKRS的新型三维空间映射技术,成功地将这些细胞亚型“放回”它们在胚胎小脑中的原始位置。结果令人震撼:这些细胞亚型在胚胎期就已经形成了特定的空间格局,有的聚集在表层,有的位于深处,被清晰的“细胞稀疏边界”隔开。这个早期的空间排布,竟能精准地预测成年后小脑功能模块(如纵向条纹和横向脑叶)的最终形态。
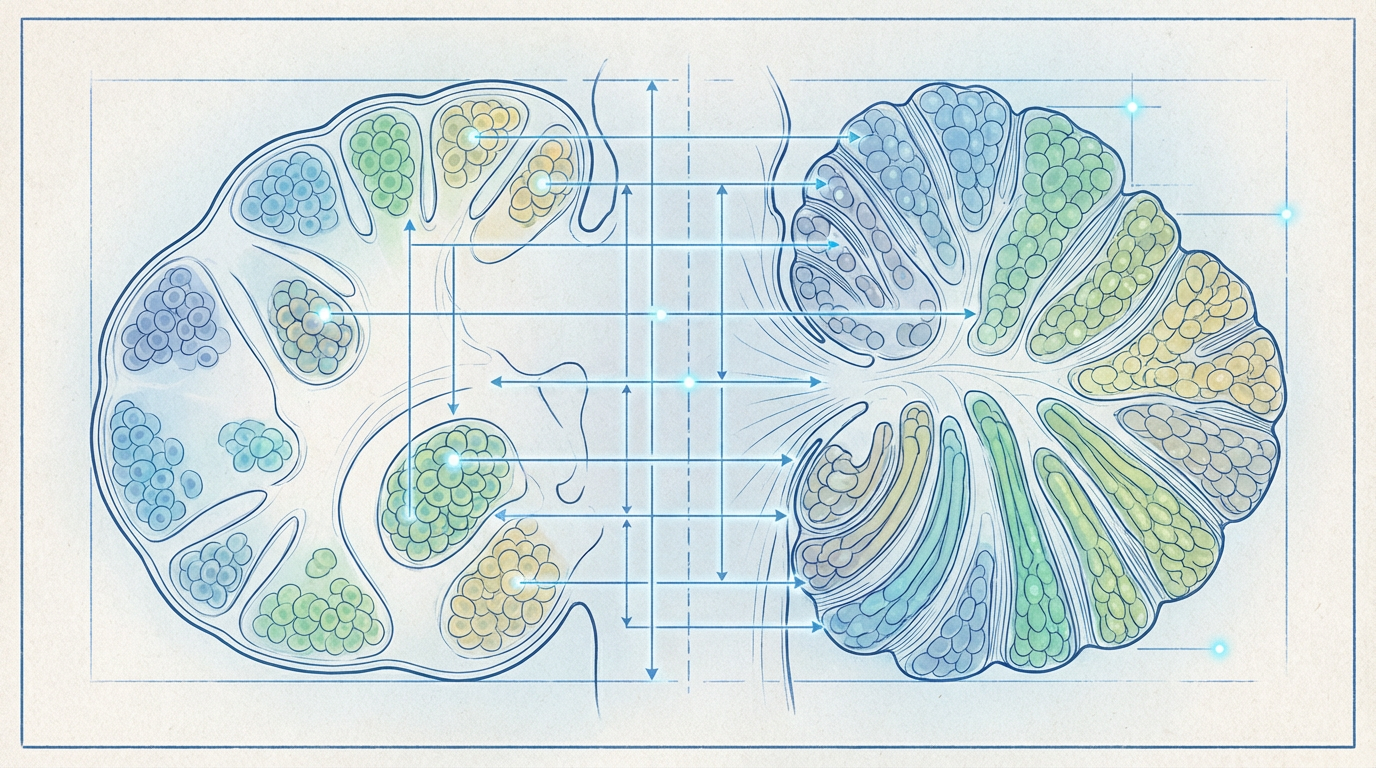
这就像一场宏大的细胞交响乐。FOXP基因是乐谱,它为每一种浦肯野细胞(演奏者)指定了独特的乐器和声部。这些细胞各就其位,共同奏响了小脑复杂结构形成的序曲。而细胞表面的钙粘蛋白等粘附分子,则像是确保演奏者们能找到并固定在正确位置的“舞台标记”。
为了验证FOXP基因这位“总指挥”的关键作用,研究团队构建了基因敲除小鼠模型。当Foxp1或Foxp2基因被特异性敲除后,这场发育的交响乐瞬间陷入混乱。
更深层次的证据来自神经环路。当小脑半球因Foxp2缺失而发育失败时,其上游专门向该区域投射信息的“下橄榄核”神经元,也因失去目标而发生大规模凋亡。这从环路层面证实,FOXP基因的指令,决定了整个小脑模块的生死存亡。
这项研究最激动人心的发现,在于它连接了发育与进化。研究团队将目光从老鼠扩展到人类和小鸡,进行了一场跨物种的比较。
他们发现,在小鼠小脑半球发育中扮演关键角色的PC1亚型细胞(其身份由高表达的Foxp1基因定义),在高度演化、拥有巨大认知能力的人类胎儿小脑中高度富集;而在几乎没有小脑半球、认知能力相对简单的鸡的小脑中则极为罕见。
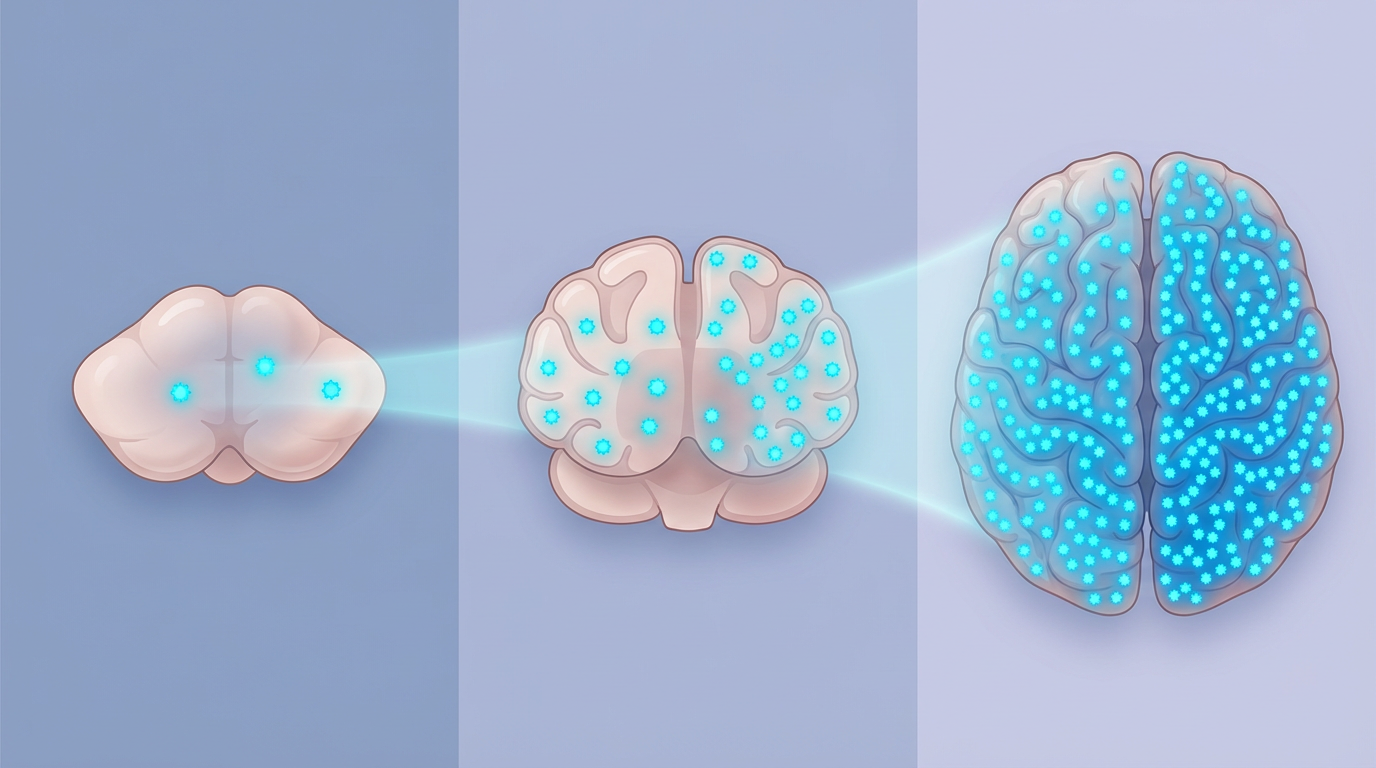
这一发现提出了一个影响深远的假说:由Foxp1基因调控的PC1细胞亚型的扩增,可能是驱动哺乳动物小脑半球在进化中不断扩张,并最终促成人类高级认知能力(如语言、工具使用和复杂社交)出现的关键细胞学基础。
这项基础研究的现实意义直指一类困扰全球数百万家庭的疾病——自闭症谱系障碍(ASD)。临床上早已发现,许多自闭症患者存在小脑结构的异常,而FOXP1和FOXP2基因的突变也是已知的自闭症高风险遗传因素。
过去,我们知道基因与疾病相关,却不清楚中间的“黑箱”。这项研究则打开了这个黑箱,它提供了一个清晰的生物学机制:FOXP基因突变 → 浦肯野细胞多样性受损 → 特定小脑功能模块(尤其是半球)发育缺陷 → 社交、语言等高级认知功能障碍。
这为我们理解自闭症的病因提供了一个全新的、基于小脑发育的细胞分子视角,也为未来开发更具针对性的干预和治疗策略指明了方向。
当然,大脑的奥秘远未被完全揭开。FOXP基因家族无疑是小脑发育这本复杂乐谱中的关键章节,但它并非全部。未来的研究将需要进一步探索:
从曾被认为是“语言基因”的FOXP2,到如今揭示整个FOXP家族在构建“智能中枢”小脑中的宏大作用,科学的认知在不断深化。通过解码这份由基因书写的古老发育蓝图,我们不仅在理解大脑如何构建,更是在探寻人类智慧与意识的起源,并为那些因这幅蓝图出现些许偏差而备受困扰的灵魂,点亮一盏希望之灯。