对抗知识焦虑,从看懂这条开始
App 下载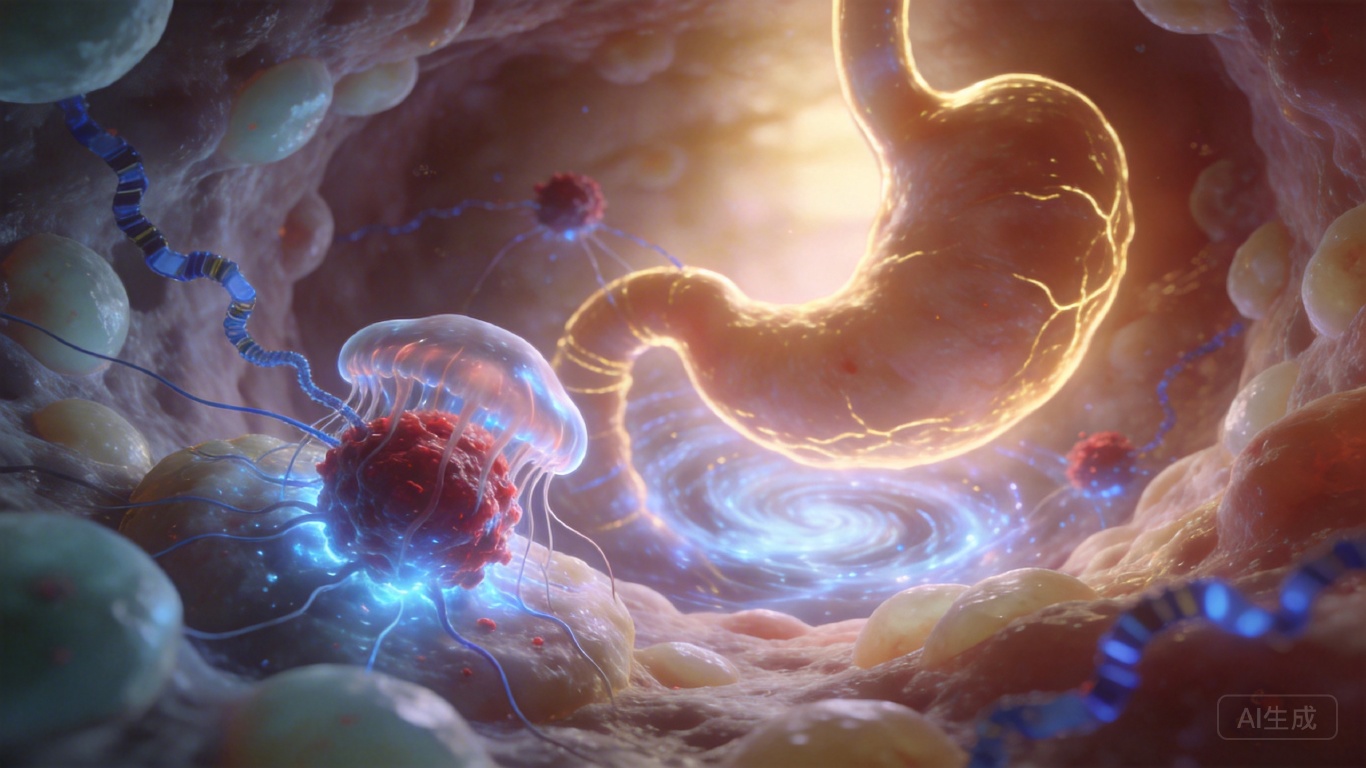
胃癌转移的隐秘通路:成纤维细胞操控癌细胞的表观密码
上海交通大学|肿瘤微环境|组蛋白硫酸化修饰|胃癌转移|癌症相关成纤维细胞|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
上海交通大学|肿瘤微环境|组蛋白硫酸化修饰|胃癌转移|癌症相关成纤维细胞|肿瘤学|医学健康
你可能听过癌细胞会自己“跑”到身体其他部位,但很少有人知道,真正帮它们“越狱”的,可能是肿瘤身边一群看似无害的“帮凶”——癌症相关成纤维细胞(CAFs),就是肿瘤微环境里的“包工头”,专门给癌细胞铺路、递信号。
全球每年有近百万胃癌新患者,其中超过一半会走向转移,中位生存期只剩1年。上海交通大学的研究团队,最近揪出了这群“帮凶”操控癌细胞的核心密码:一条藏在组蛋白上的硫酸化修饰通路,能让乖乖待在胃里的癌细胞,瞬间变成会“穿墙”的侵袭者。
为什么成纤维细胞能远程操控癌细胞的命运?这条隐秘通路到底是怎么运作的?
我们可以把癌细胞的转移过程,比作一场有预谋的“越狱”——首先得有人给它递“越狱指南”,然后它得自己改造身体,最后才能突破防线。
CAFs就是递指南的那个“内鬼”。它们会分泌一种叫信号素7A(SEMA7A)的分子,像个藏在信封里的指令,精准贴到胃癌细胞表面的整合素β1(ITGB1)上——这就好比癌细胞的“接收天线”收到了信号。接下来,胃癌细胞内部的ERK1/2-CEBPB信号通路被激活,就像按下了启动键,直接上调了半乳糖-3-O-磺基转移酶1(GAL3ST1)的表达。
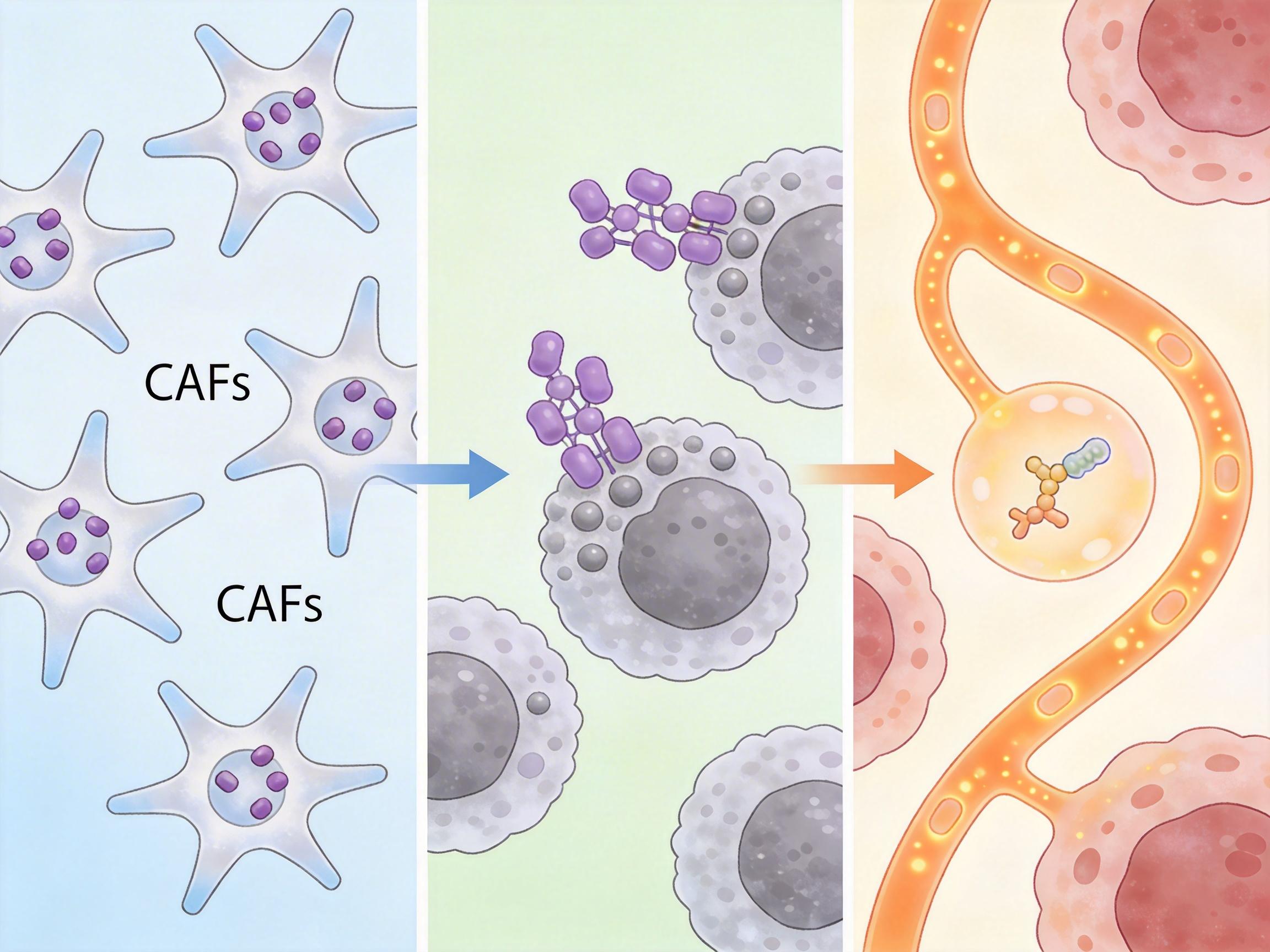
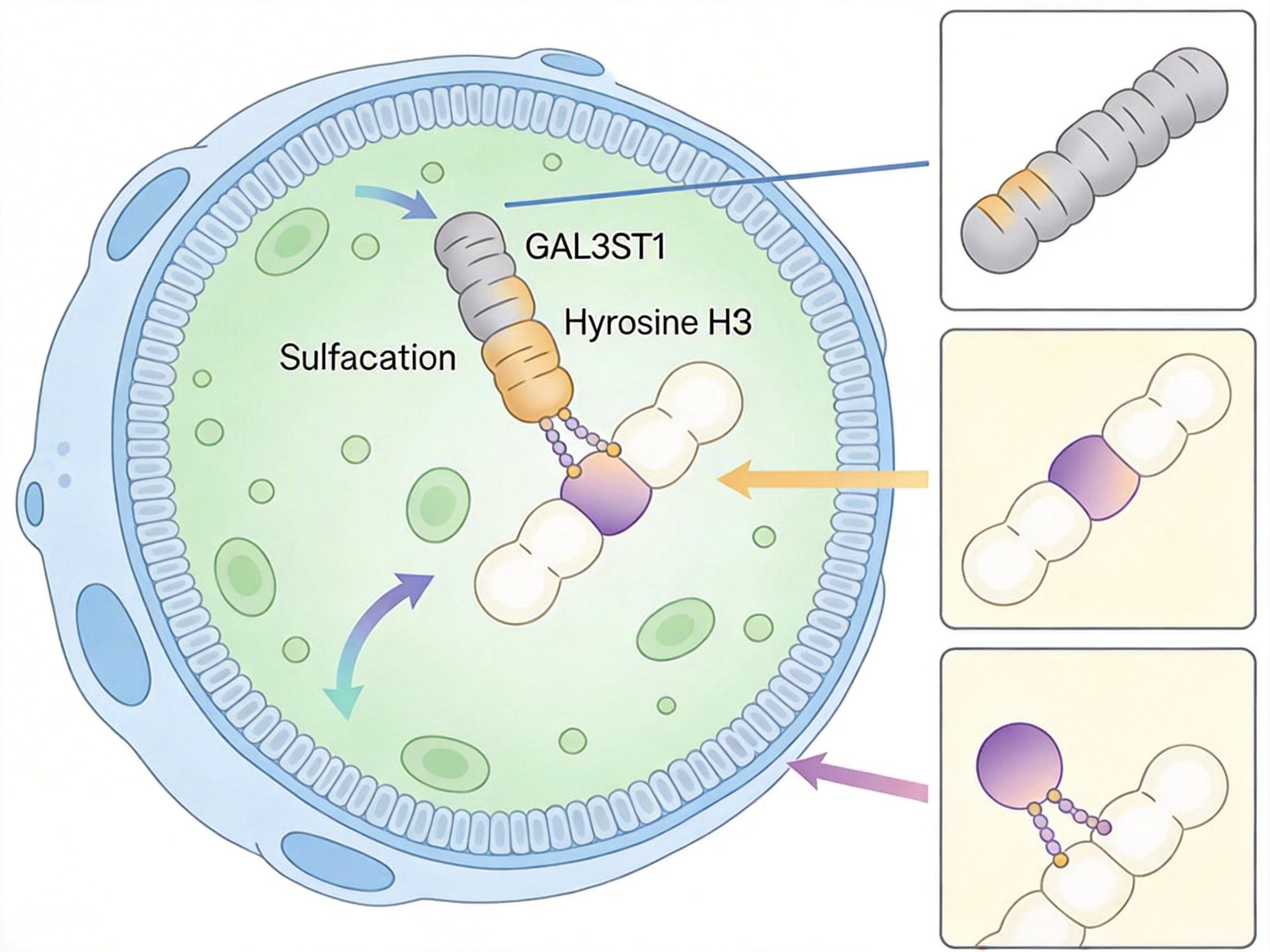
GAL3ST1是这场越狱的“技术总监”。它不是直接指挥癌细胞跑路,而是在细胞里给一种叫组蛋白H3的蛋白质“做标记”:在细胞质里,它会给新生组蛋白H3的酪氨酸99位点(H3Y99)加上一个硫酸基团——这就像给文件盖了个“允许通行”的章。
这些盖了章的组蛋白,会通过AP2B1这个“快递员”被运进细胞核,在那里招募KAT2A这个“装修工”,给组蛋白H3的第56位赖氨酸加上乙酰化修饰(H3K56ac)。这个修饰会直接激活β-连环蛋白的转录,而β-连环蛋白就是癌细胞“变身”的开关——它一激活,癌细胞就会启动上皮-间质转化(EMT),从原本黏在一起的“上皮细胞”,变成能自由移动的“间质细胞”,也就是完成了“越狱”的最后一步。
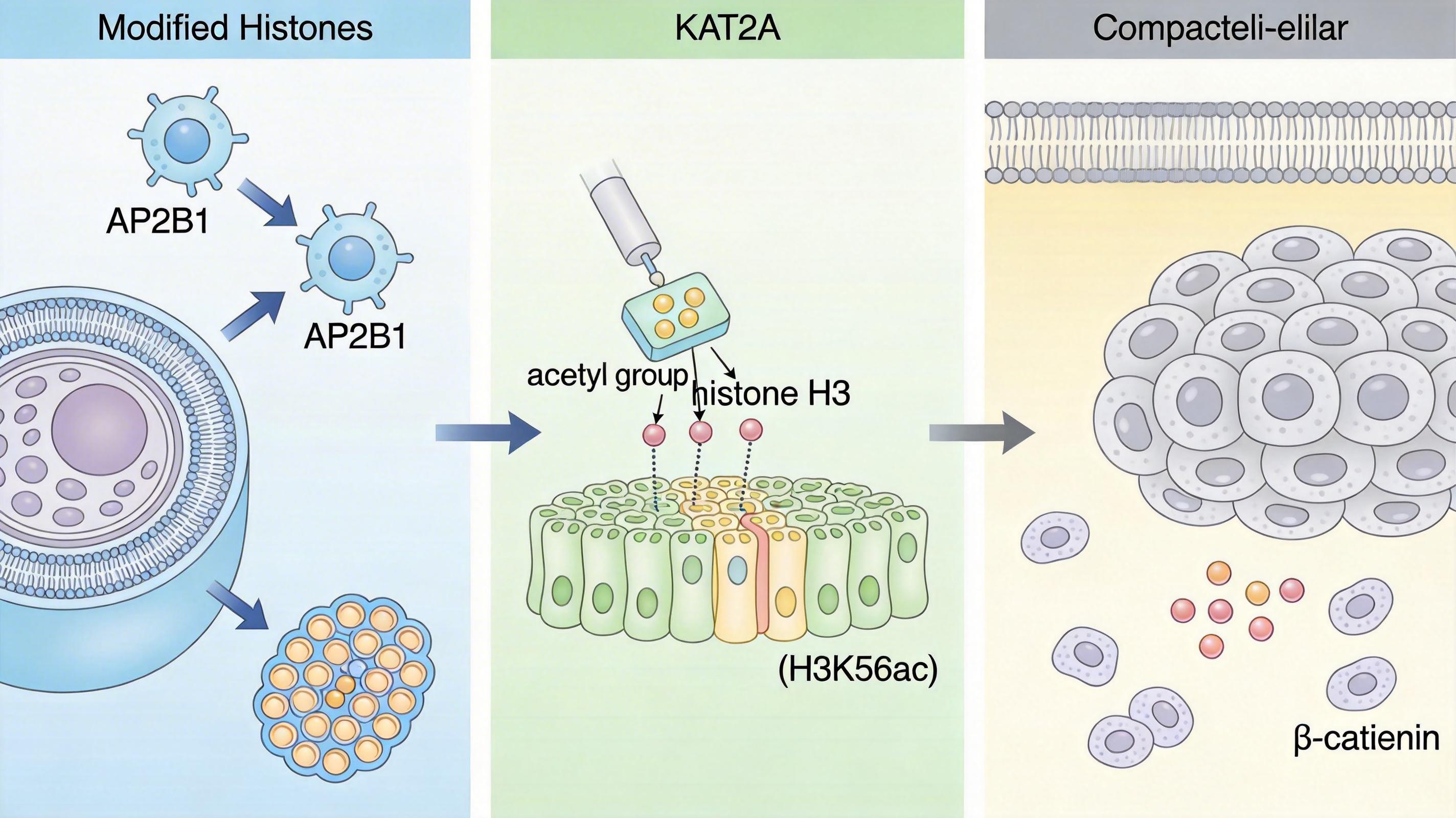
简单说,整个通路就是:CAFs发信号→胃癌细胞激活GAL3ST1→组蛋白被硫酸化修饰→核内激活转移相关基因→癌细胞获得侵袭能力。
在这场分子操控里,最关键的突破,是发现了GAL3ST1作为组蛋白磺基转移酶的功能——这打破了我们对组蛋白修饰的传统认知。
过去我们知道的组蛋白修饰,主要是甲基化、乙酰化、磷酸化这些,硫酸化修饰是近几年才被发现的新型表观遗传标记。它和其他修饰的不同在于,它发生在细胞质里的新生组蛋白上,而不是细胞核内的成熟组蛋白。而且,这个修饰的位点H3Y99,正好位于核小体的内部,平时被包裹得严严实实,只有在组蛋白新生、尚未组装成核小体的时候,才会暴露出来,给GAL3ST1留下“盖章”的机会。
更重要的是,这个硫酸化修饰不是孤立存在的。它会和组蛋白H4的第3位精氨酸二甲基化(H4R3me2a)形成“双重标记”,共同招募转录因子TDRD3,调控下游基因的表达。在胃癌里,这个通路最终激活的是β-连环蛋白,而在肝癌里,它还能调控癌细胞对缺氧环境的适应——这说明,组蛋白硫酸化可能是多种癌症共有的表观遗传调控机制。
不过,我认为目前这个研究还有一个容易被忽略的点:组蛋白硫酸化的调控是动态的,它不仅受CAFs的信号影响,还可能受细胞代谢状态的调控——因为硫酸化修饰需要的硫酸基供体PAPS,是细胞代谢的产物。也就是说,癌细胞的代谢状态,可能会反过来影响这个通路的活性,这给未来的治疗留下了更多想象空间。
这条SEMA7A/GAL3ST1/H3Y99sulf通路的发现,给胃癌转移的治疗带来了新的靶点,但从实验室到临床,还有不少坎要跨。
首先是CAFs的异质性。CAFs不是单一的细胞群体,它有很多亚型,有的促肿瘤,有的甚至有抑瘤作用。这次研究里的CAFs分泌SEMA7A,但不是所有CAFs都会分泌这个分子——如果我们盲目靶向所有CAFs,可能会误伤那些有抑瘤作用的亚型,反而得不偿失。
其次是GAL3ST1的特异性。GAL3ST1不仅在胃癌里表达,在其他癌症甚至正常组织里也有分布,只是表达水平不同。要开发针对它的抑制剂,必须保证只抑制胃癌细胞里的GAL3ST1,而不影响正常细胞的功能,否则会带来严重的副作用。
不过,也有值得期待的地方。目前已经有研究发现,GAL3ST1在胆管癌、肝癌里也扮演着促转移的角色,这说明针对这个靶点的药物,可能对多种癌症有效。而且,这个通路涉及的多个环节,从SEMA7A到ITGB1,再到GAL3ST1,都可以作为治疗靶点——我们可以选择其中最特异性的环节入手,比如开发针对SEMA7A和ITGB1结合的抗体,阻断CAFs给癌细胞发信号。
另外,这条通路和免疫治疗的结合也值得探索。CAFs本身就是肿瘤免疫抑制微环境的重要组成部分,靶向这个通路不仅能抑制癌细胞转移,还可能重塑肿瘤微环境,增强免疫治疗的效果。比如,抑制GAL3ST1可能会减少β-连环蛋白的激活,而β-连环蛋白正好是免疫抑制的关键调控因子之一。
当我们把目光从癌细胞本身,转向它身边的微环境,就会发现肿瘤的发生发展,从来不是单一细胞的“独角戏”,而是一场复杂的“群体博弈”。CAFs和癌细胞的这场操控与被操控,只是肿瘤微环境里无数故事中的一个。
GAL3ST1介导的组蛋白硫酸化通路的发现,不仅让我们对胃癌转移的机制有了更深入的理解,更重要的是,它给我们打开了一扇新的门——原来表观遗传修饰,也可以成为肿瘤-基质相互作用的关键节点。
微观的分子标记,决定着宏观的生命走向。 未来,随着我们对肿瘤微环境的理解越来越深入,或许我们能找到更多这样的“隐秘通路”,给那些被癌症判了“死刑”的患者,带来新的希望。