13 天前

13 天前
一位62岁的非吸烟女性,确诊晚期肺腺癌时带着EGFR敏感突变——这曾是个“好消息”,意味着她能用上第三代靶向药,预期无进展生存期能到18-20个月。可仅仅12个月后,她的肿瘤就开始进展。基因测序结果揭开谜底:她的肿瘤细胞里,还藏着一个TP53突变——这个被称为“基因组守护者”的抑癌基因失效了,让靶向药的效果打了对折。
在中国,每两个EGFR突变肺癌患者里,就有一个带着这类抑癌基因共突变。他们曾是靶向治疗时代的“隐形掉队者”,直到2026年3月,一项针对这类人群的三期临床研究,终于给他们找到了新的出路。
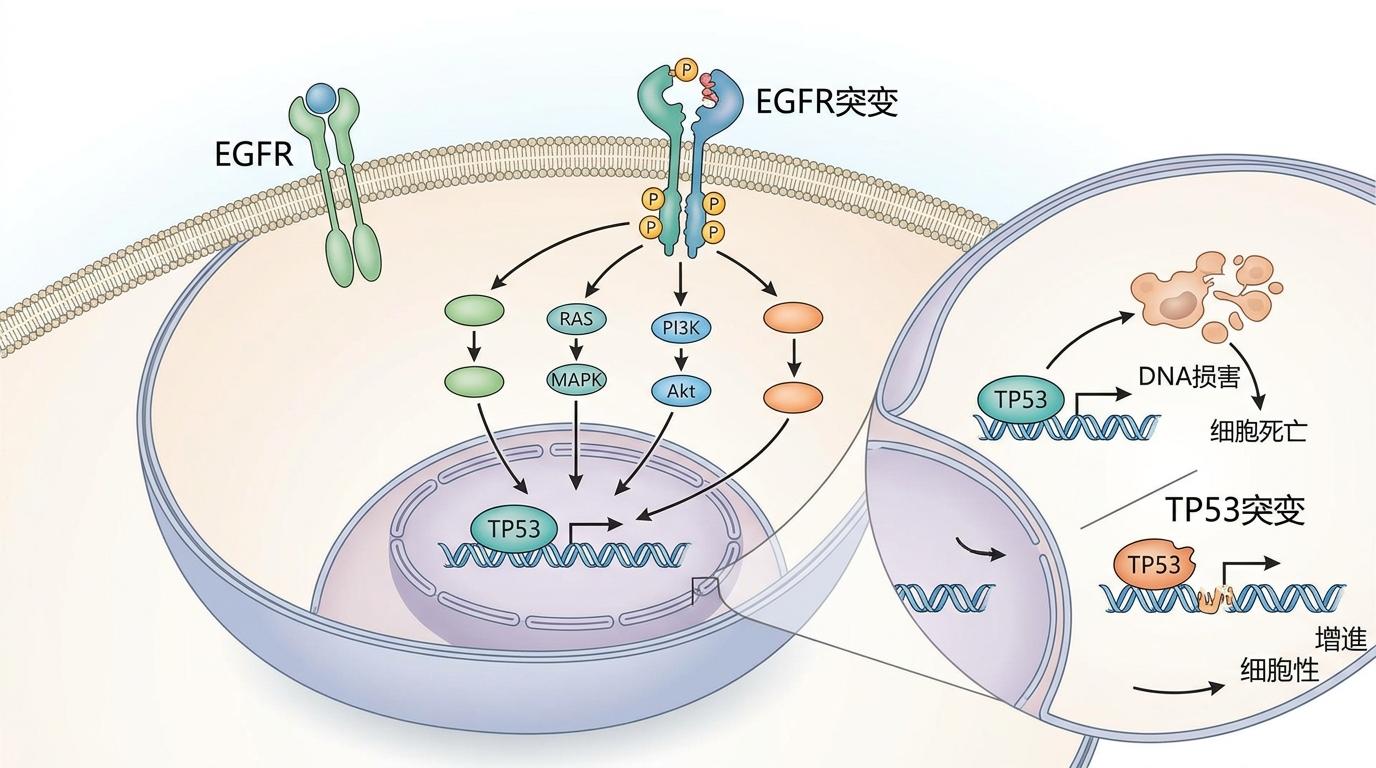
要理解这个问题,得先搞懂EGFR突变和抑癌基因的关系。EGFR就像肿瘤细胞上的“油门”,一旦发生突变,就会被死死卡住,让细胞疯狂增殖;而以TP53为代表的抑癌基因,是细胞里的“刹车”,负责监控DNA损伤,及时让异常细胞凋亡。
你可以把肿瘤细胞想象成一辆失控的汽车:EGFR突变踩下了油门,而抑癌基因突变,相当于刹车也失灵了。第三代靶向药能精准松开油门,但对失灵的刹车无能为力——这就是为什么单纯用靶向药,对带着抑癌基因共突变的患者效果有限。
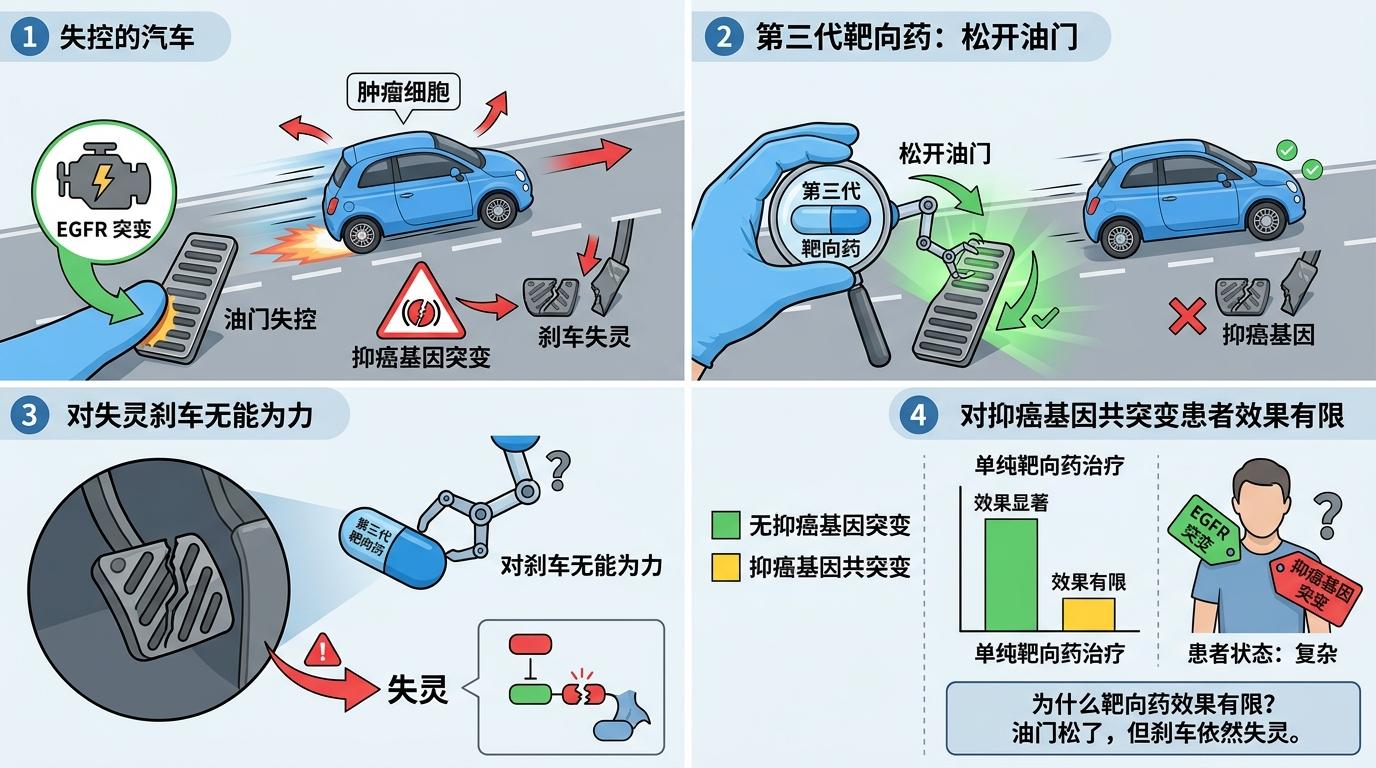
之前的研究数据显示,这类患者用靶向药的中位无进展生存期,比单纯EGFR突变患者短了近三分之一。更棘手的是,随着基因测序技术的普及,医生发现90%以上的EGFR突变肺癌患者,都带着至少一个共突变基因,其中抑癌基因的突变占了一半以上。
2026年发布的这项三期临床研究,首次专门瞄准了EGFR突变合并抑癌基因共突变的患者。研究把126名患者分成两组:一组单用第三代靶向药,另一组用靶向药联合卡铂-培美曲塞化疗。
结果超出预期:联合治疗组的中位无进展生存期达到了19.78个月,比单药组的16.53个月足足延长了3个多月;尤其是带着TP53突变的亚组患者,联合治疗让他们的无进展生存期从16.3个月提升到了18.69个月。
这个方案的逻辑很直接:既然刹车失灵了,那就给车装个“减速带”——化疗能杀伤那些躲过靶向药的耐药细胞,弥补抑癌基因失效带来的漏洞。当然,代价是化疗的副作用:联合治疗组3级以上不良反应发生率是25.9%,比单药组的17.2%略高,但没有出现药物相关的死亡病例,大多数副作用都能通过支持治疗控制。
更重要的是,这项研究首次用循证医学证据证明:通过基因分层筛选出高风险患者,再用强化治疗方案,能真正缩小不同患者之间的疗效差距。
这项研究的另一个意义,是把基因检测从“可选项目”推到了“一线标准”。过去,很多患者只做单基因EGFR检测,就直接用上了靶向药,直到耐药后才想起做全基因测序——但这时往往已经错过了最佳治疗时机。
现在,医生可以通过下一代测序(NGS)技术,一次性检测几十甚至上百个基因,不仅能找到驱动突变,还能发现那些会影响疗效的共突变基因。比如TP53、RB1这些抑癌基因的突变,就像给医生提了个醒:这个患者单纯用靶向药可能不够,需要更强化的治疗方案。
当然,基因分层也面临挑战。目前NGS检测的费用还比较高,部分地区的医保覆盖有限;而且不同基因检测公司的结果解读标准不统一,也可能影响治疗决策。但不可否认的是,随着技术的进步和成本的下降,基因分层会越来越普及——毕竟,对患者来说,最精准的治疗,才是最有效的治疗。
从“一把钥匙开所有锁”的广谱治疗,到“精准匹配”的靶向治疗,再到“基因分层指导”的个体化治疗,肺癌治疗的每一步,都在朝着“让每个患者都得到最合适的治疗”这个目标靠近。
那位带着TP53突变的患者,如果能在确诊时就做全基因测序,就能直接用上靶向药联合化疗的方案,或许就能多争取几个月的无进展生存期。而这项研究的意义,就是让更多这样的“隐形掉队者”,不再被靶向药的“平均疗效”所掩盖。
基因分层,让肺癌治疗不再“一刀切”。未来,随着更多基因靶点被发现,更多联合治疗方案被验证,我们离“治愈肺癌”的目标,又近了一步。
点击催更,成为大圆镜下一个视频选题!