对抗知识焦虑,从看懂这条开始
App 下载
心脏靠跳动抗癌,这个蛋白是关键
里雅斯特大学|塞雷娜·扎奇尼亚|物理抑癌机制|原发性心脏肿瘤|心脏跳动|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
里雅斯特大学|塞雷娜·扎奇尼亚|物理抑癌机制|原发性心脏肿瘤|心脏跳动|肿瘤学|医学健康
人体有超过200种细胞,几乎每种都可能叛变长成癌细胞——肺、肝、肠、乳腺,甚至指甲盖下面都能长出恶性肿瘤。但有一个器官是例外:心脏。
尸检数据显示,原发性心脏肿瘤的检出率不足1%,连其他器官癌细胞转移到心脏的概率,也只有不到两成。这个“癌症绝缘体”的秘密,困扰了医学界几十年。直到2026年4月,发表在《科学》杂志上的一项研究给出了答案:不是心脏的位置特殊,也不是它的细胞有什么“免死金牌”——而是它一辈子没停过的跳动,在物理层面死死摁住了癌细胞。
意大利的里雅斯特大学的科学家塞雷娜·扎奇尼亚团队,做了一个听起来有点疯狂的实验:他们把小鼠的心脏完整移植到了小鼠的颈部。这些“脖子上的心脏”能得到正常血液供应,维持基本代谢,但因为没有连接血管泵血的需求,它们不会跳动。
研究团队同时给小鼠原生的跳动心脏,和颈部的“静止心脏”注射了同一种癌细胞。两周后结果出来时,连研究者都吃了一惊:静止的移植心脏里,癌细胞已经疯长到取代了大部分健康组织;而跳动的原生心脏里,癌变区域只占了不到20%。
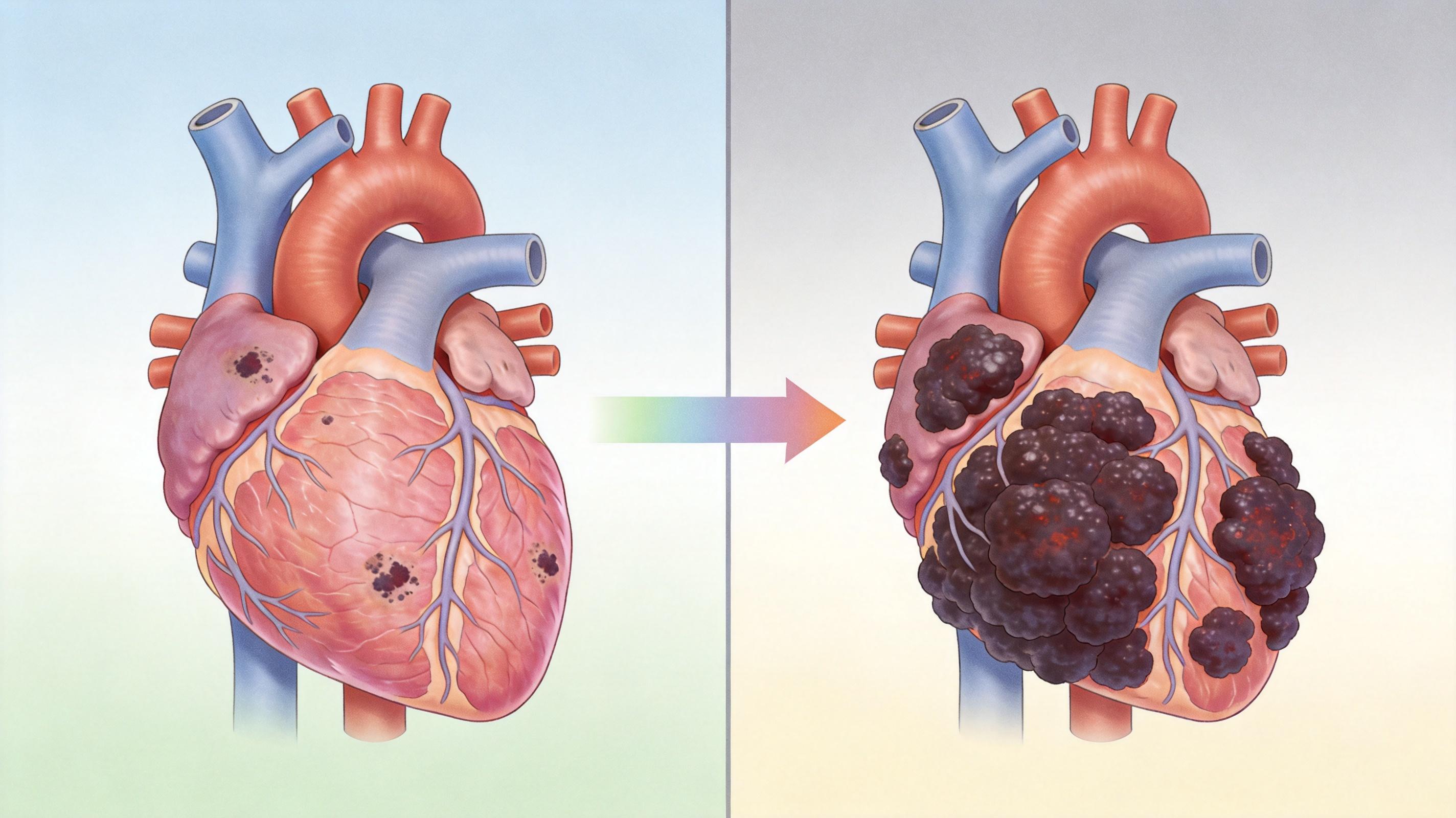
为了排除“位置差异”的干扰,他们又在实验室里用大鼠细胞培养了“工程化心脏组织”——这种组织只有接触钙离子时才会收缩跳动。实验结果和动物模型完全一致:在跳动的组织里,癌细胞只敢零星聚集在外层;而在静止的组织里,癌细胞像泼在宣纸上的墨汁一样,毫无阻碍地弥漫扩散。
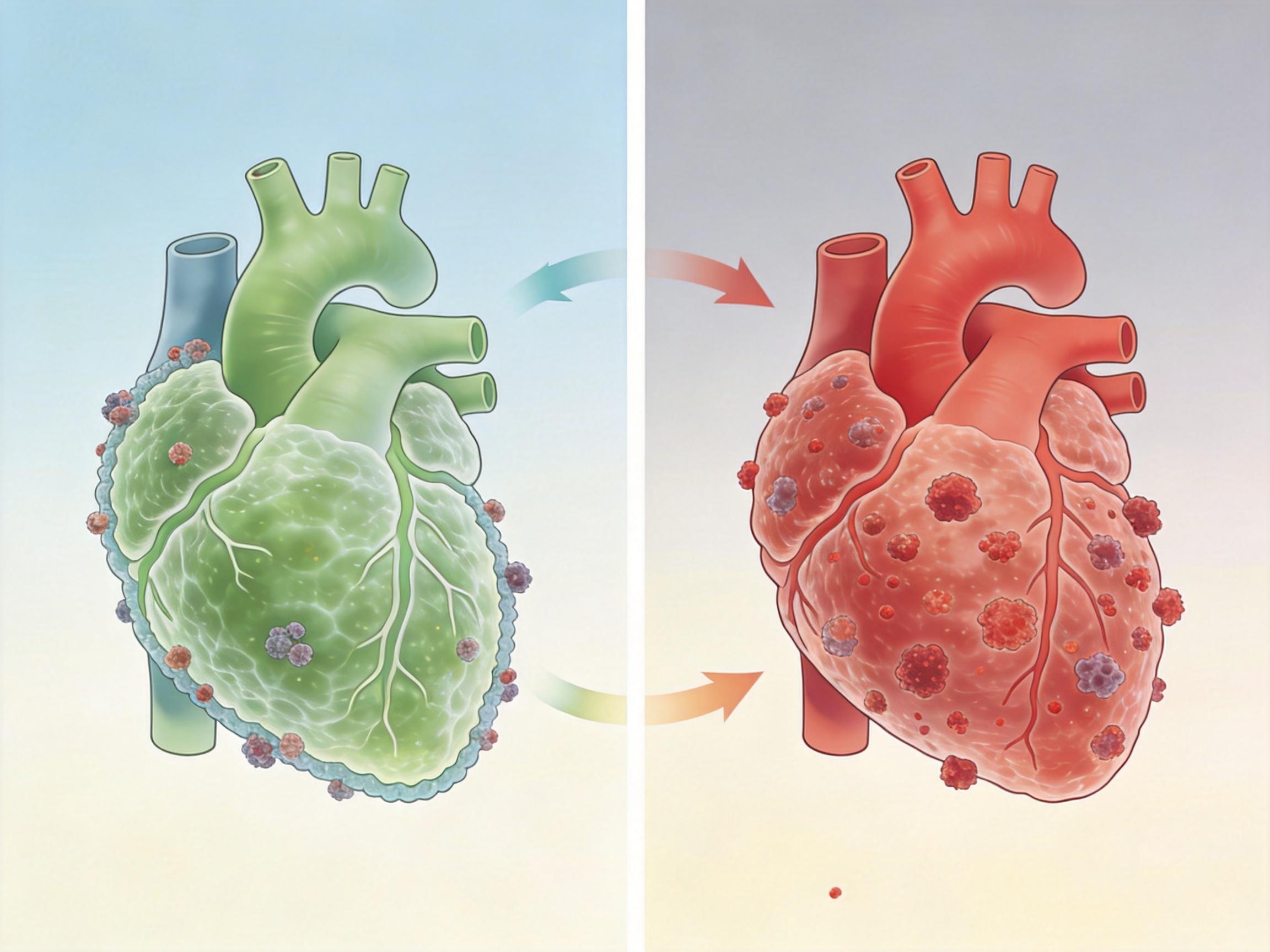
这不是某种神秘的化学物质在起作用,纯粹是物理力量的胜利。心脏每天跳动10万次,每一次收缩舒张都会产生持续的机械拉伸和压力——这种被称为“机械应变”的物理刺激,成了癌细胞无法突破的牢笼。
那么,看不见摸不着的机械力,是怎么变成抑制癌细胞生长的信号的?研究团队通过空间转录组学分析人类心脏转移癌样本,找到了关键的“传令兵”——Nesprin-2蛋白。
你可以把这个蛋白想象成一根贯穿细胞的“电话线”:它的一端连在细胞膜上的细胞骨架上,另一端直接扎进细胞核里。当心脏跳动产生的机械力拉扯细胞时,这根“电话线”会把物理信号直接传递到细胞核内部,而不是像普通信号那样要经过层层生化反应的“翻译”。
具体的过程是这样的:机械力通过Nesprin-2传递到细胞核后,会激活一种“组蛋白去甲基化酶”,这种酶会把包裹DNA的组蛋白上的某个“标记”——组蛋白H3第9位赖氨酸的三甲基化——给去掉。这个标记的作用是让DNA紧密缠绕成一团,就像把文件塞进加密的档案柜;而去掉标记后,染色质会变得松散,相当于把档案柜的门打开了。
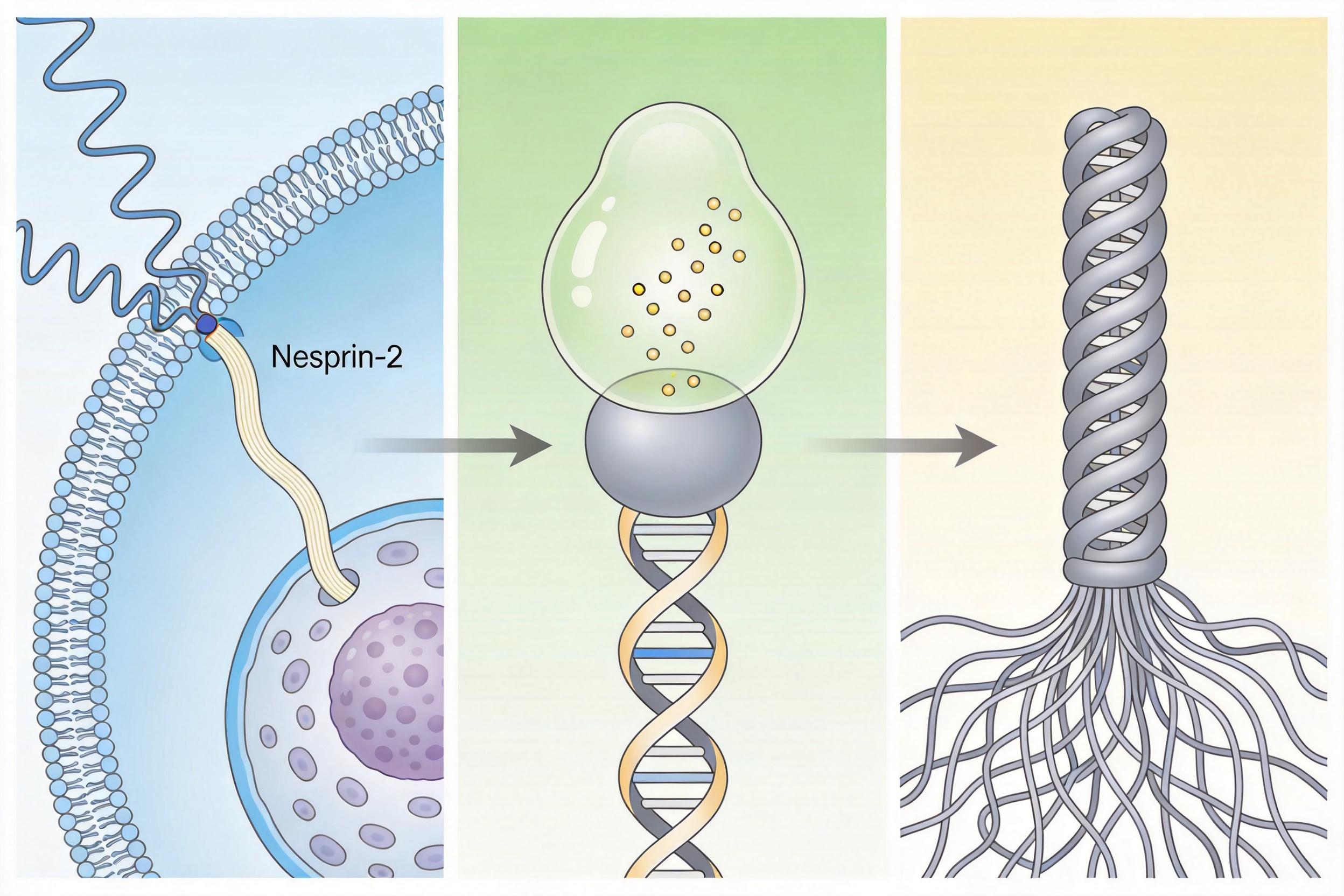
别以为松散的染色质是给癌细胞开了绿灯——恰恰相反,癌细胞的快速增殖需要精准调控特定基因的开关,松散的染色质会打乱它们的增殖程序,让它们无法顺利分裂。当研究者在癌细胞里敲低Nesprin-2的表达后,哪怕把这些细胞放回跳动的心脏里,它们也能立刻恢复疯长的能力,形成和静止环境里一样大的肿瘤。
更有意思的是,Nesprin-2还兼职调控细胞的“死亡开关”:它能和Bcl-2家族蛋白结合,直接启动癌细胞的凋亡程序。也就是说,它不仅能“叫停”癌细胞的生长,还能主动“下令”让癌细胞死亡。
这个发现不止解决了“心脏为什么不得癌”的老问题,还打开了一扇全新的大门:既然机械力能抑制癌细胞,那能不能把这种机制复制到其他器官上?
研究团队已经开始探索,能不能用模拟心脏跳动的机械刺激,来治疗皮肤、乳腺这些表浅部位的肿瘤。比如给患者戴上一个能产生规律拉伸力的装置,通过物理刺激来抑制肿瘤生长,或者增强化疗和免疫治疗的效果。
还有一个更反常识的猜想:高血压患者的心脏承受着比常人更大的压力,这种额外的机械负荷,会不会意外地给他们带来一点抗癌的保护?目前这个猜想还没有临床数据支持,但从机制上看并非完全没有可能。
甚至这个发现还能解释心脏的另一个特点:为什么成年人心肌细胞几乎不会再生。原来,抑制心肌细胞增殖的机械信号通路,和抑制癌细胞生长的是同一条——大自然用同一个机制,既让心脏保持了终身稳定的泵血功能,又顺便给它装上了抗癌的“防护罩”。
当然,这个机制还有很多未解之谜:比如为什么有些癌细胞还是能突破机械屏障转移到心脏?不同频率、强度的机械力,对癌细胞的影响会不会有差异?这些问题都需要更多研究来回答。
我们总以为抗癌的关键是找到某种神奇的分子,或者设计出精准的靶向药物,却常常忽略了最朴素的物理力量。心脏用一辈子的跳动告诉我们:生命的运作,从来都不是单一的化学或生物过程,而是物理、化学、生物信号交织成的复杂网络。
机械力不仅是维持器官功能的“动力”,更是调控细胞命运的“信号”。当我们开始用“力学视角”重新审视生命,说不定能发现更多藏在身体里的“天然防护机制”。
机械即信号,跳动即守护。