
5 天前

5 天前
当你盯着体检报告上的“脂肪肝”字样不以为意时,你的肝脏里可能正在发生一场沉默的灾难。每五个脂肪肝患者里,就有一个会进展为代谢相关脂肪性肝炎(MASH),而其中近四分之一会走向肝纤维化——这个阶段的患者,每加重一个纤维化等级,预期寿命就缩短10年。过去我们以为,肝纤维化只是炎症后的被动修复,直到复旦大学的研究团队,揪出了藏在代谢通路里的“幕后黑手”。他们用基因敲除小鼠证实,阻断一条由代谢物琥珀酸启动的信号通路,就能让已经启动的肝纤维化显著逆转。这背后的逻辑,颠覆了我们对肝纤维化的传统认知。
你可以把肝脏想象成一个繁忙的食品加工厂,肝细胞负责生产和代谢,而肝星状细胞(HSCs)原本是仓库管理员,负责储存维生素A。但当肝细胞因为脂肪堆积受损时,会意外泄漏一种叫琥珀酸的代谢物——它本该是细胞能量循环里的“中间产物”,却在此时变成了“警报信号”。
琥珀酸会精准找到肝星状细胞表面的GPR91受体,就像一把钥匙插进锁孔。一旦结合,两个关键通路就会被激活:一条通路让“仓库管理员”瞬间变身“纤维工人”,开始疯狂合成胶原蛋白;另一条通路则给这些“工人”打上“免死金牌”,阻止它们自然凋亡。
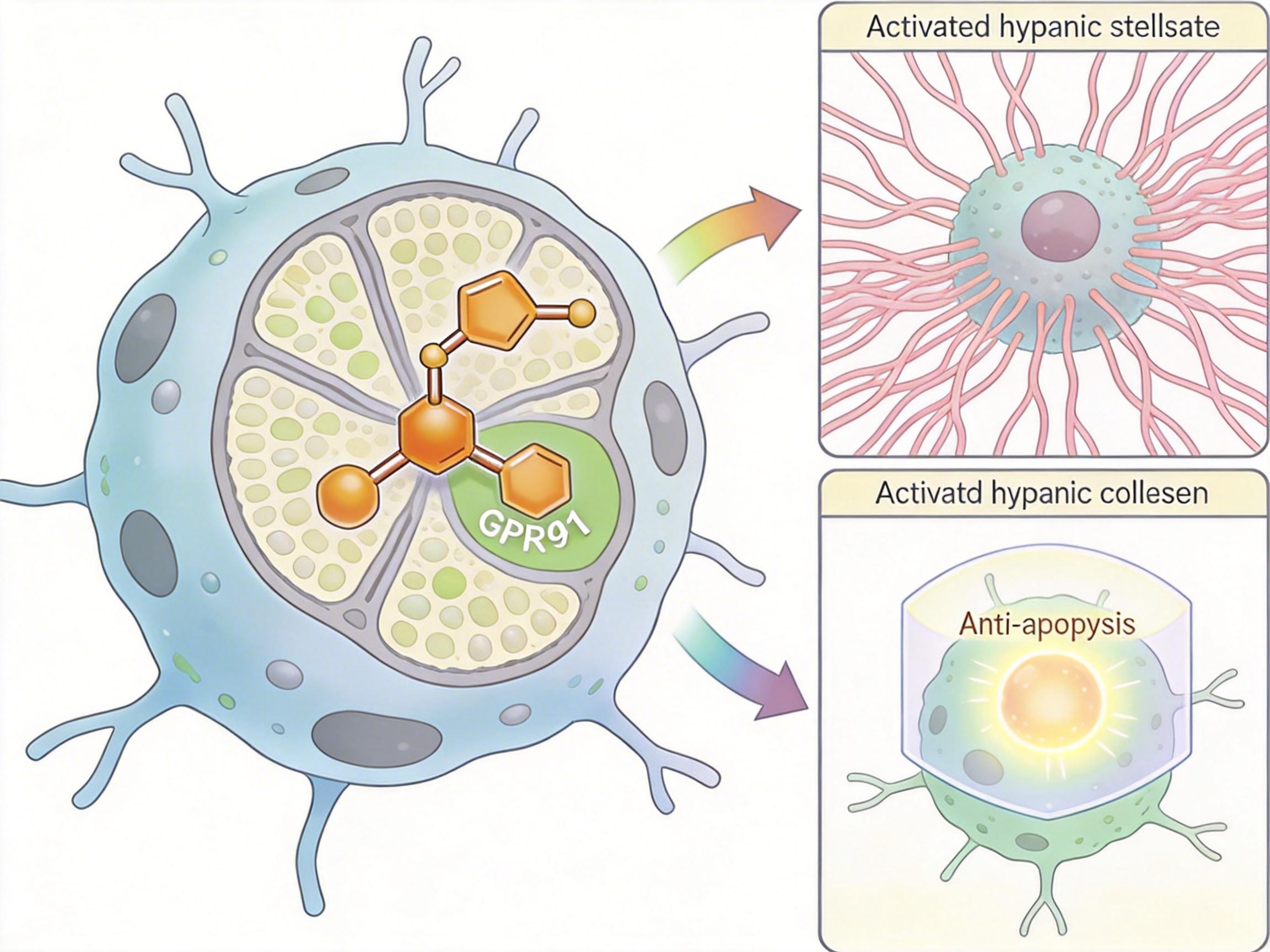
研究团队在小鼠身上做了两组对照实验:给野生型小鼠注射琥珀酸,原本的肝纤维化程度直接翻倍;而给肝星状细胞特异性敲除GPR91的小鼠喂同样的高脂高糖饮食,它们的肝脏胶原蛋白沉积量比野生型小鼠低了40%,纤维化标志物水平直接腰斩。
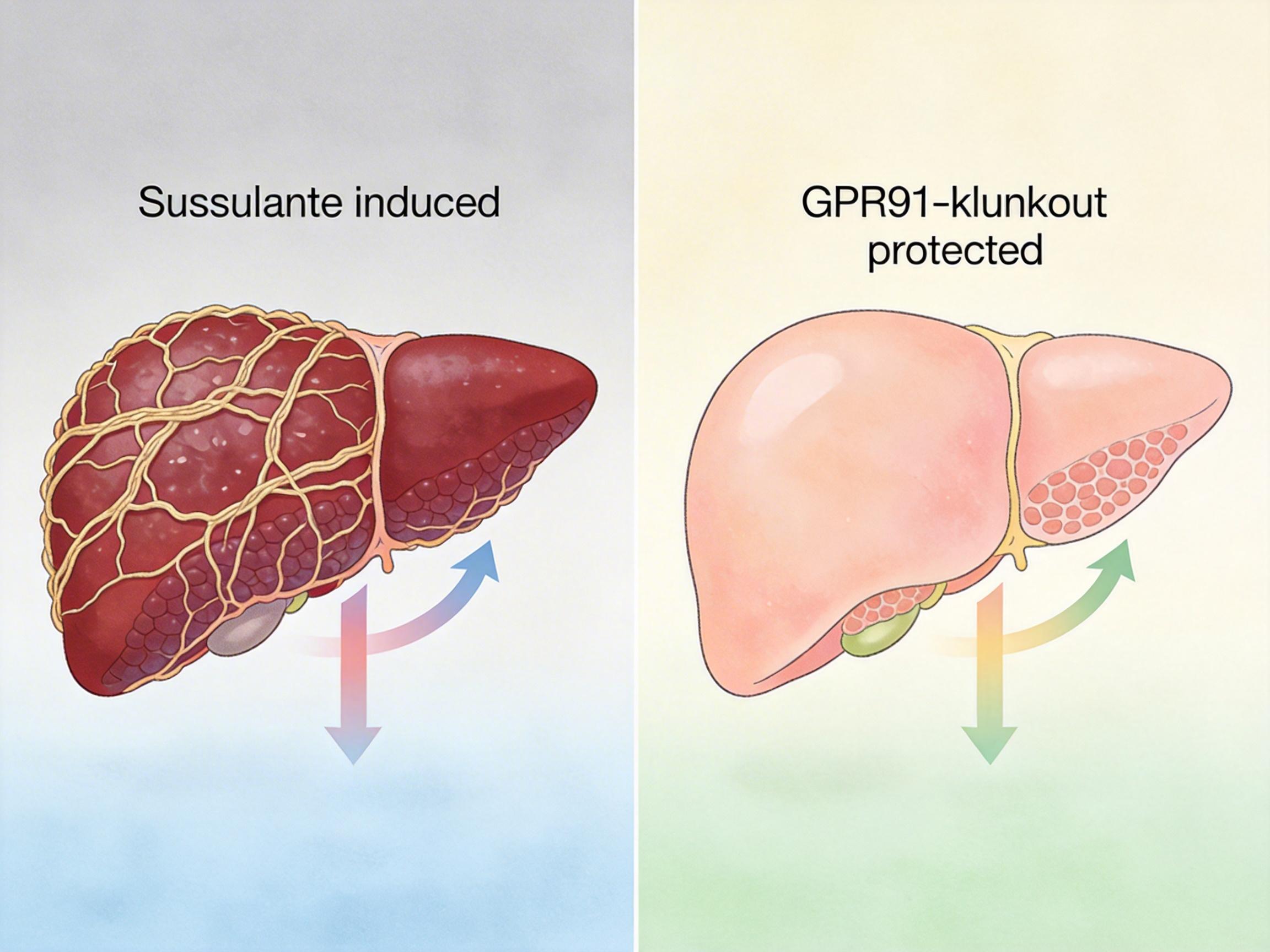
更有意思的是,这个琥珀酸-GPR91信号轴不是肝脏的“专属问题”。研究人员发现,在特发性肺纤维化、肾纤维化患者的病变组织里,琥珀酸浓度同样显著升高,GPR91受体的表达量也远超健康组织。这意味着,这个信号轴可能是多器官纤维化的“通用密码”。
在肺纤维化模型里,给小鼠补充琥珀酸会让肺组织的胶原沉积量增加60%,而用药物阻断GPR91后,小鼠的肺功能下降速度减缓了一半。甚至在克罗恩病的肠道纤维化病变中,也能找到这条通路激活的痕迹。
当然,现在就谈临床应用还为时尚早。GPR91受体不仅存在于纤维化相关细胞,还在心脏、肾脏等健康组织中表达,直接用药物全身阻断可能会引发副作用。研究团队的下一步,是开发能精准靶向肝星状细胞的递送系统——就像给药物装个“导航”,只在肝脏的“纤维工厂”里发挥作用。
这场研究最颠覆的地方,是重新定义了代谢物的角色。过去我们以为,琥珀酸这类三羧酸循环中间产物,只是细胞能量生产线上的“过客”,没想到它们还能变身“信号指挥官”,直接调控细胞的命运。
在MASH患者的肝脏里,受损肝细胞的线粒体功能紊乱,导致琥珀酸无法正常进入能量循环,只能大量泄漏到细胞外。这些“逃逸”的琥珀酸就像失控的信号弹,在肝脏里掀起纤维化的连锁反应。而研究中用到的二甲基马来酸盐,能通过抑制琥珀酸脱氢酶的活性,减少琥珀酸的积累,在小鼠模型里成功减轻了肝纤维化程度。
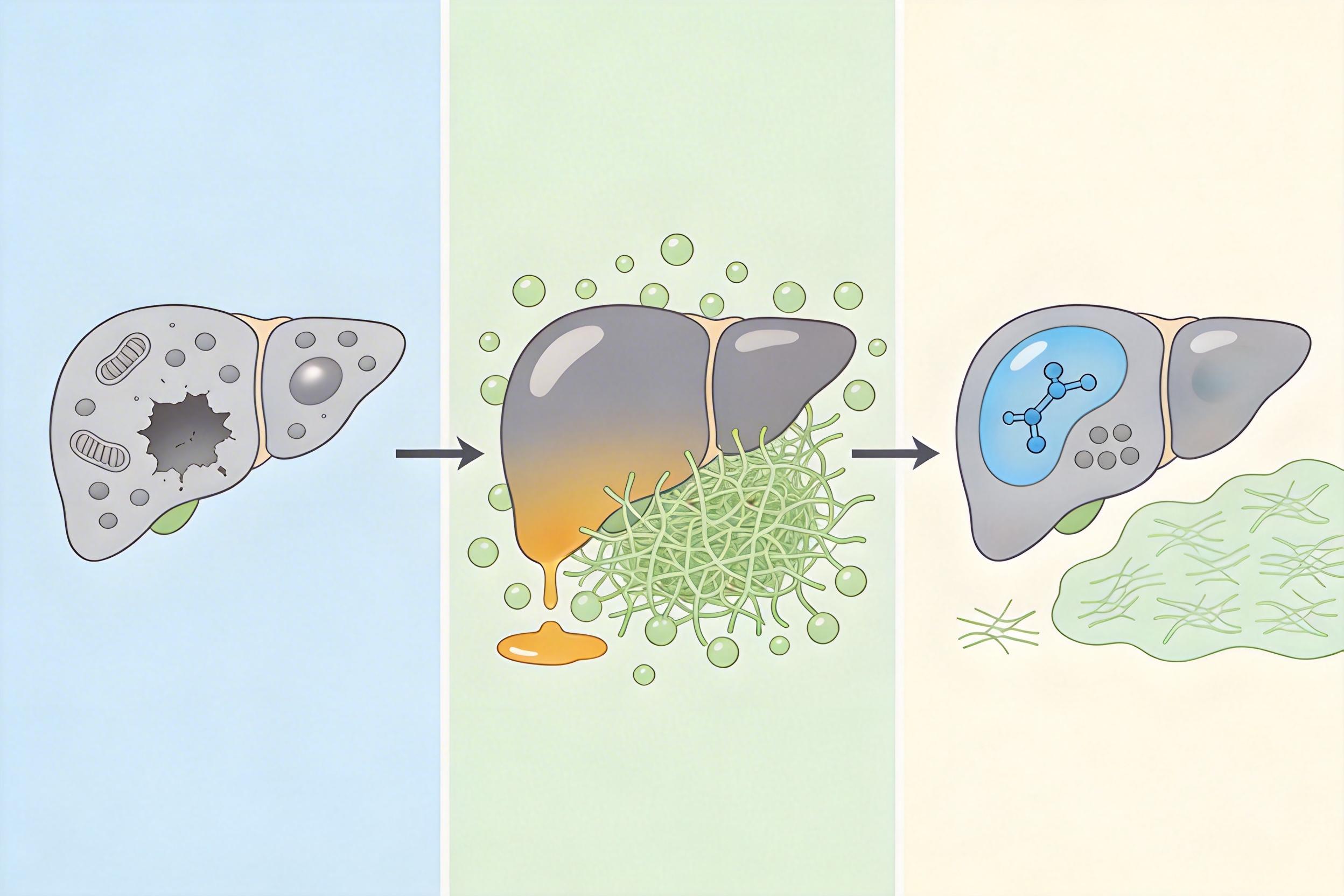
不过这种代谢调控的思路也有局限:它可能会影响正常细胞的能量代谢,长期使用的安全性还需要更多验证。相比之下,精准阻断GPR91受体的策略,更像是“掐断信号源”,对正常细胞的影响更小。
当我们还在把脂肪肝当成“小毛病”时,肝脏里的代谢信号已经在悄悄改写疾病的走向。复旦大学的研究不仅找到了肝纤维化的关键靶点,更让我们意识到:代谢物从来不是细胞里的“背景板”,它们是调控疾病的“隐形开关”。
未来的抗纤维化治疗,或许不再是单纯的“抗炎”或“抑制胶原合成”,而是精准切断代谢信号的传导通路。就像关掉一个失控的工厂,让肝脏的“仓库管理员”重新回到岗位上。
代谢信号,才是纤维化的隐秘指挥棒。
点击催更,成为大圆镜下一个视频选题!