对抗知识焦虑,从看懂这条开始
App 下载
胃癌免疫抑制的幕后推手被找到了
调节性T细胞|CD44受体|丝甘蛋白|南京医科大学|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
调节性T细胞|CD44受体|丝甘蛋白|南京医科大学|肿瘤学|医学健康
你或许听说过,胃癌患者的免疫系统常常像被按下了暂停键——本该攻击肿瘤的免疫细胞,要么缩在一旁不动,要么干脆帮着肿瘤生长。南京医科大学的研究团队,在分析了23对胃癌组织样本后,揪出了这个藏在肿瘤微环境里的“内奸”:一种叫丝甘蛋白的蛋白聚糖,它正通过一套精密的分子逻辑,把免疫细胞改造成肿瘤的“保护伞”。这背后的机制,比我们想象的更狡猾,也为打破胃癌免疫僵局提供了新的突破口。
丝甘蛋白(Serglycin)是肿瘤细胞大量分泌的一种蛋白聚糖,它的目标是免疫细胞表面的CD44受体——这种受体在调节性T细胞(Tregs)上尤其多。Tregs本来是免疫系统的“刹车”,用来防止免疫反应过度攻击自身组织,但在肿瘤微环境里,它们成了帮凶:分泌抑制因子、阻止效应T细胞活化,让肿瘤得以“逍遥法外”。
研究发现,丝甘蛋白和CD44结合后,会启动一条连锁反应:先激活TGFβRI/Smad3信号通路,直接推动Tregs向更具抑制性的LAG3+亚群分化;同时触发Tregs的代谢重编程——增强糖酵解,加速清除细胞内的活性氧(ROS)。
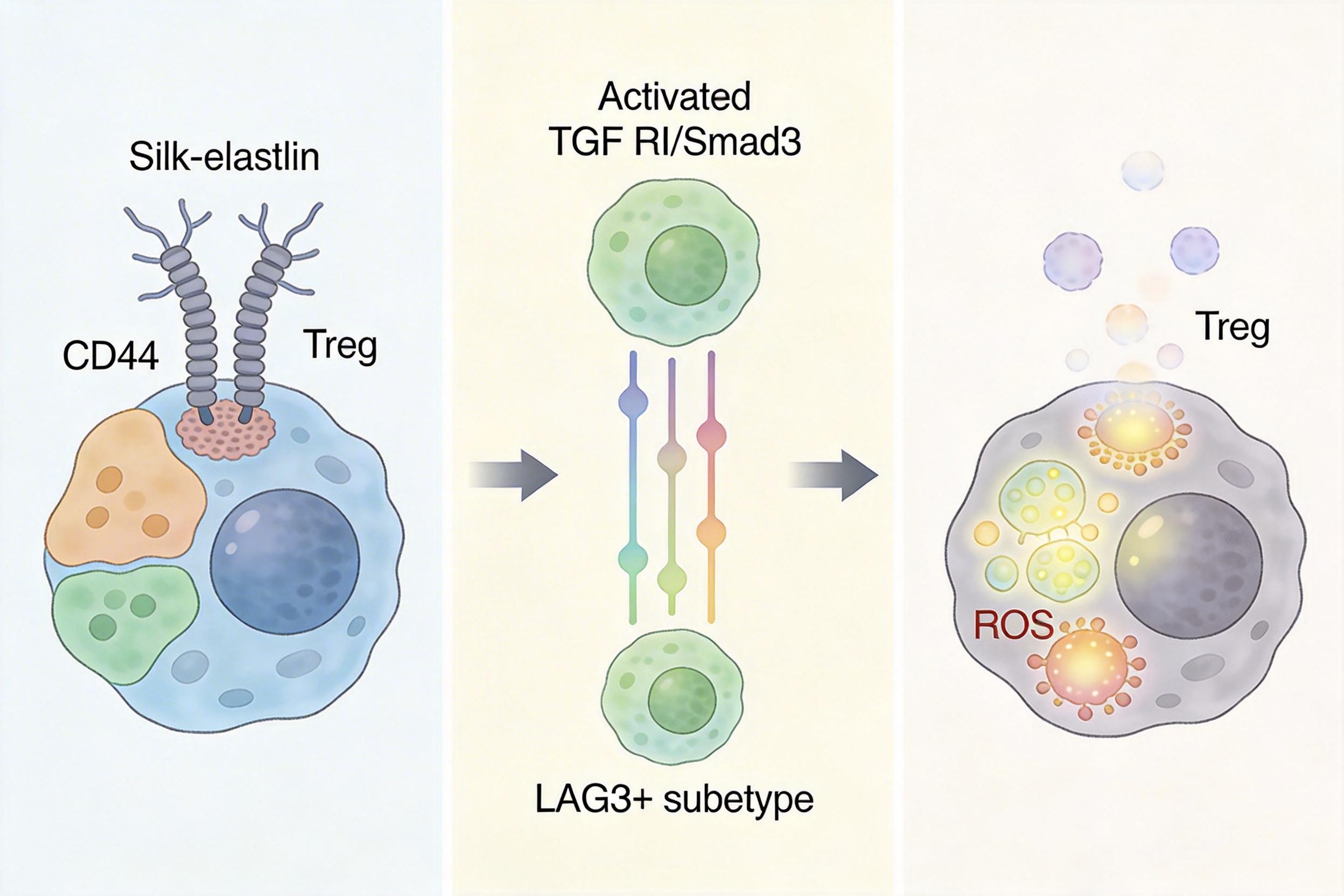
你可以把这个过程想象成:丝甘蛋白给Tregs递了一张“通行证”,不仅让它们在肿瘤里站稳脚跟,还升级了它们的“刹车装置”,让免疫系统彻底失灵。
真正的“诡计”藏在更细微的分子层面。
丝甘蛋白-CD44信号激活的糖酵解,会让Tregs内的ROS水平骤降。而ROS本来负责给LAG3蛋白的M171位点做“氧化标记”——这个标记一旦减少,LAG3就会发生两个关键变化:一是更容易形成二聚体,增强它的抑制功能;二是会躲开一种叫PELI1的泛素连接酶,避免被打上“K48连接型泛素标签”——这种标签是蛋白降解的“死刑令”。
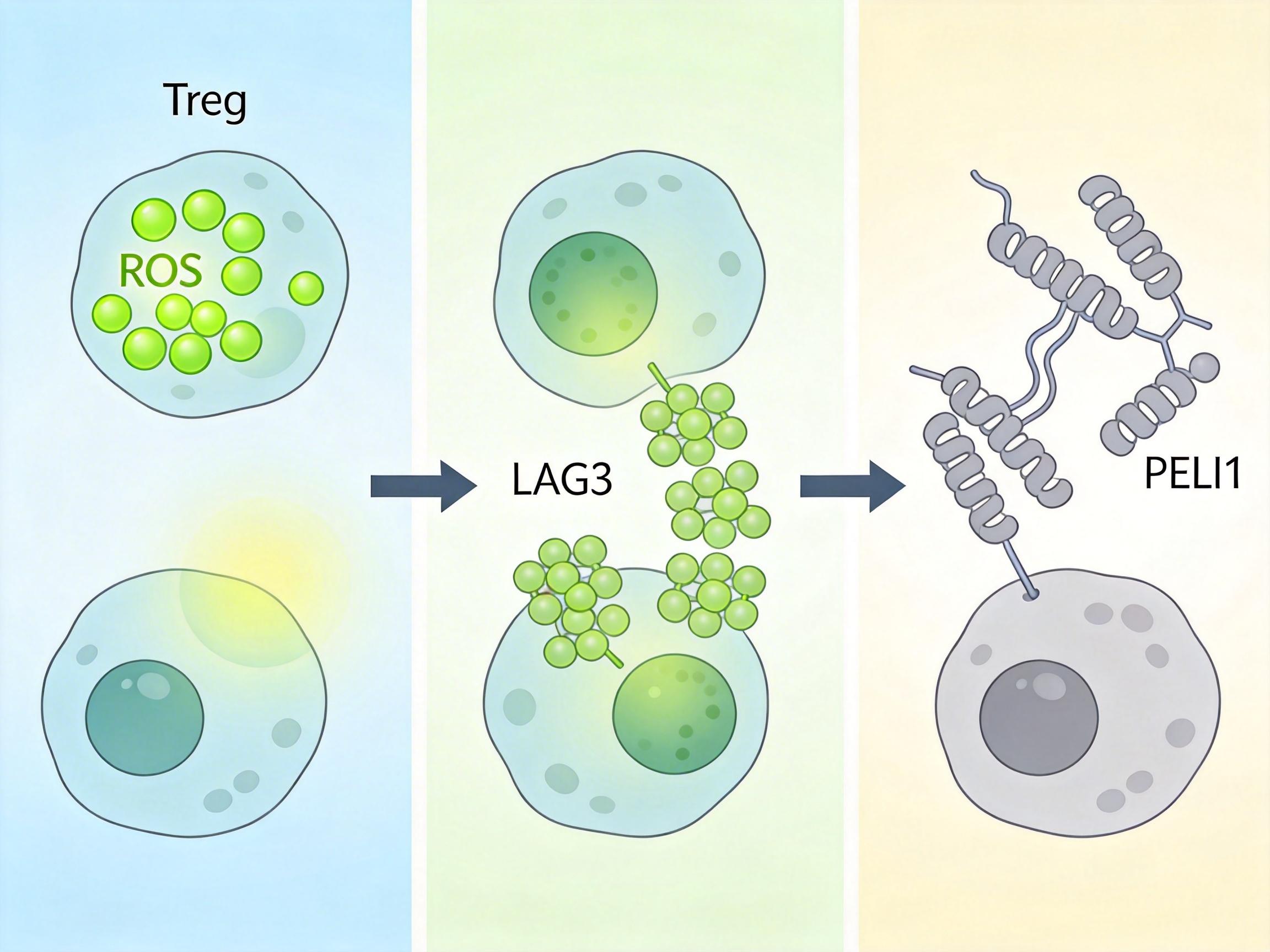
直白点说:丝甘蛋白通过调控代谢,保住了LAG3蛋白的“小命”,让它能持续在Tregs表面发挥作用,死死按住免疫系统的“启动键”。当研究人员用抗CD44抗体阻断这条通路时,LAG3+ Tregs的数量明显减少,效应T细胞重新恢复了攻击肿瘤的能力,小鼠体内的肿瘤生长也被显著抑制。
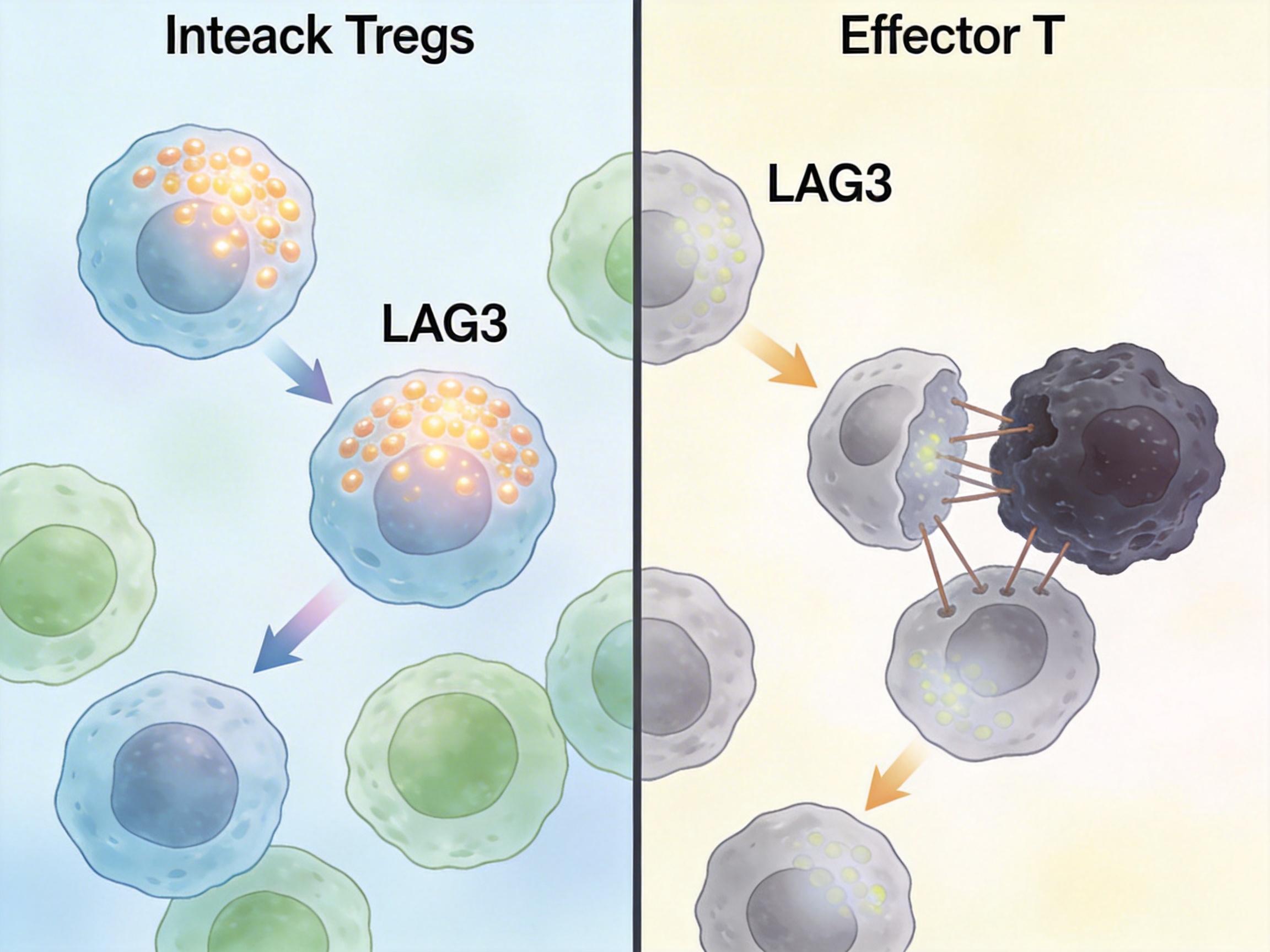
过去,胃癌免疫治疗的主要靶点是PD-1/PD-L1这类免疫检查点,但不少患者会出现耐药,核心原因就是肿瘤微环境里的免疫抑制网络太复杂——LAG3+ Tregs就是其中一个被忽略的“节点”。
这项研究的价值在于,它不仅找到了丝甘蛋白-CD44这条驱动LAG3+ Tregs分化的核心通路,还明确了从代谢调控到蛋白修饰的完整逻辑链。这意味着,未来我们可以联合靶向丝甘蛋白-CD44通路和LAG3,甚至结合现有的PD-1抑制剂,从多个角度打破免疫抑制。
更重要的是,研究团队通过单细胞测序和临床样本验证,确认了胃癌组织中丝甘蛋白水平与LAG3+ Tregs的富集程度正相关,这为开发相关的预后生物标志物提供了依据——未来或许能通过检测丝甘蛋白水平,提前判断患者的免疫治疗潜力。
长久以来,我们对抗肿瘤的思路,大多是直接“攻击”肿瘤细胞,却常常忽略了肿瘤微环境里那些被策反的“自己人”。丝甘蛋白-CD44通路的发现,让我们看到了肿瘤“驯化”免疫系统的精密逻辑——它不是简单地压制免疫,而是从代谢、蛋白修饰等底层逻辑入手,把免疫细胞改造成自己的“盟友”。
破解代谢陷阱,才能重启免疫防线。这条通路的发现,不仅为胃癌免疫治疗打开了新的窗口,也提醒我们:对抗肿瘤,或许需要先读懂肿瘤和免疫系统之间的“暗战”,才能找到精准破局的钥匙。