
1 个月前

1 个月前
当你盯着手机屏幕刷到深夜时,眼球深处那层薄如蝉翼的视网膜色素上皮细胞(RPE)正在默默加班——它要吞噬老化的感光细胞碎片,要维持视网膜的营养供应,还要扛住光照和氧化的双重攻击。到2040年,全球将有2.88亿人因为这层细胞的崩溃,陷入不可逆的失明,这就是干性年龄相关性黄斑变性(AMD)。过去我们只知道RPE细胞会死,但没人说清它是怎么“被炎症拖进死亡陷阱”的。温州医科大学的团队最近揪出了这个陷阱的总开关——一个叫DAPL1的基因,它的缺席会触发一场细胞死亡的连锁反应。
你可以把细胞想象成一个分工明确的工厂:内质网是仓库,负责储存钙离子;线粒体是发电厂,给整个工厂供能。正常情况下,仓库和发电厂之间有一条精准的“货运专线”——线粒体相关内质网膜(MAMs),它只输送刚好够发电厂运转的钙离子。但当DAPL1基因缺失时,这条专线会变成无节制的“超载高速”。
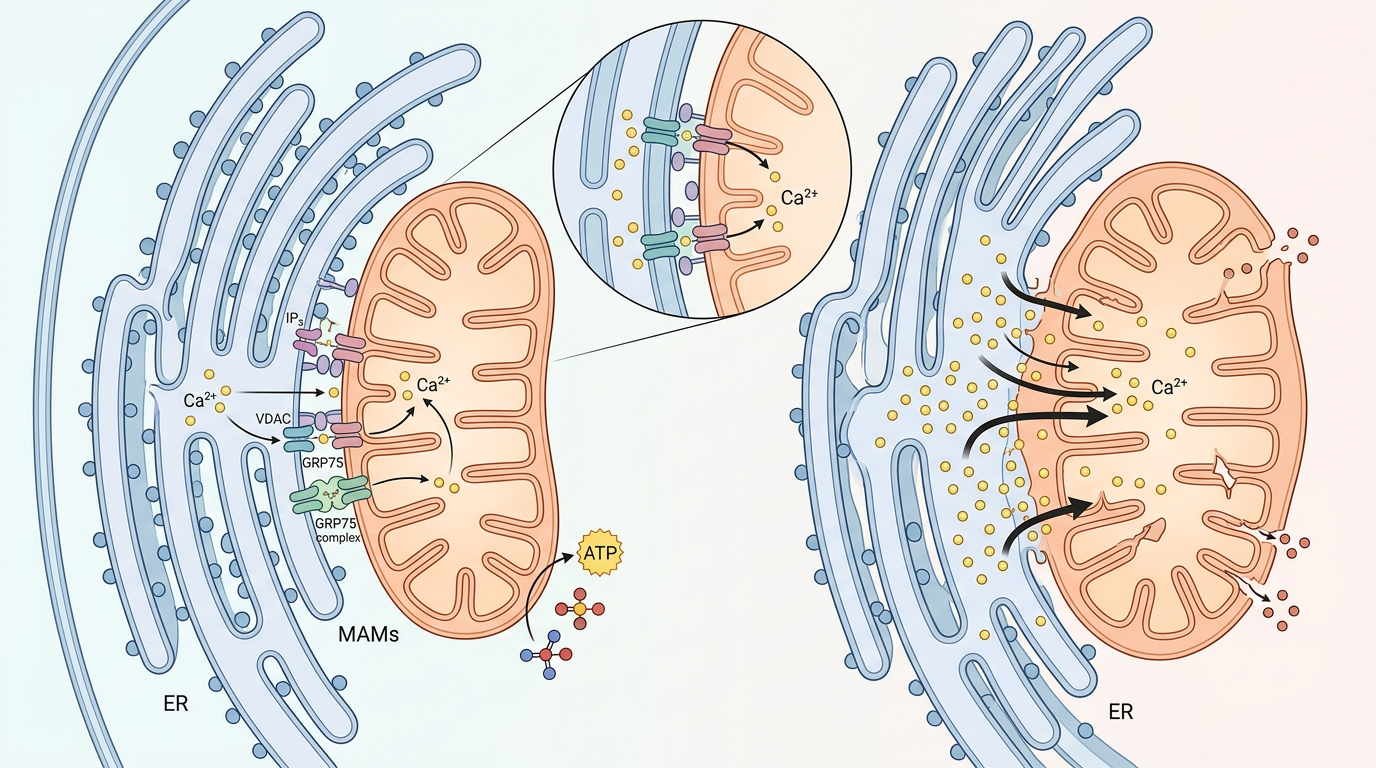
研究人员发现,DAPL1会盯着一个叫GRP75的蛋白,一旦DAPL1缺席,GRP75就会疯狂累积,像过量的胶水一样,把内质网和线粒体粘得死死的,硬生生造出更多的MAMs。这些额外的MAMs会把内质网里的钙离子一股脑倒进线粒体,导致“发电厂”被钙离子撑到过载:线粒体膜电位崩溃,DNA被挤到细胞质里,连最基本的能量都产不出来。
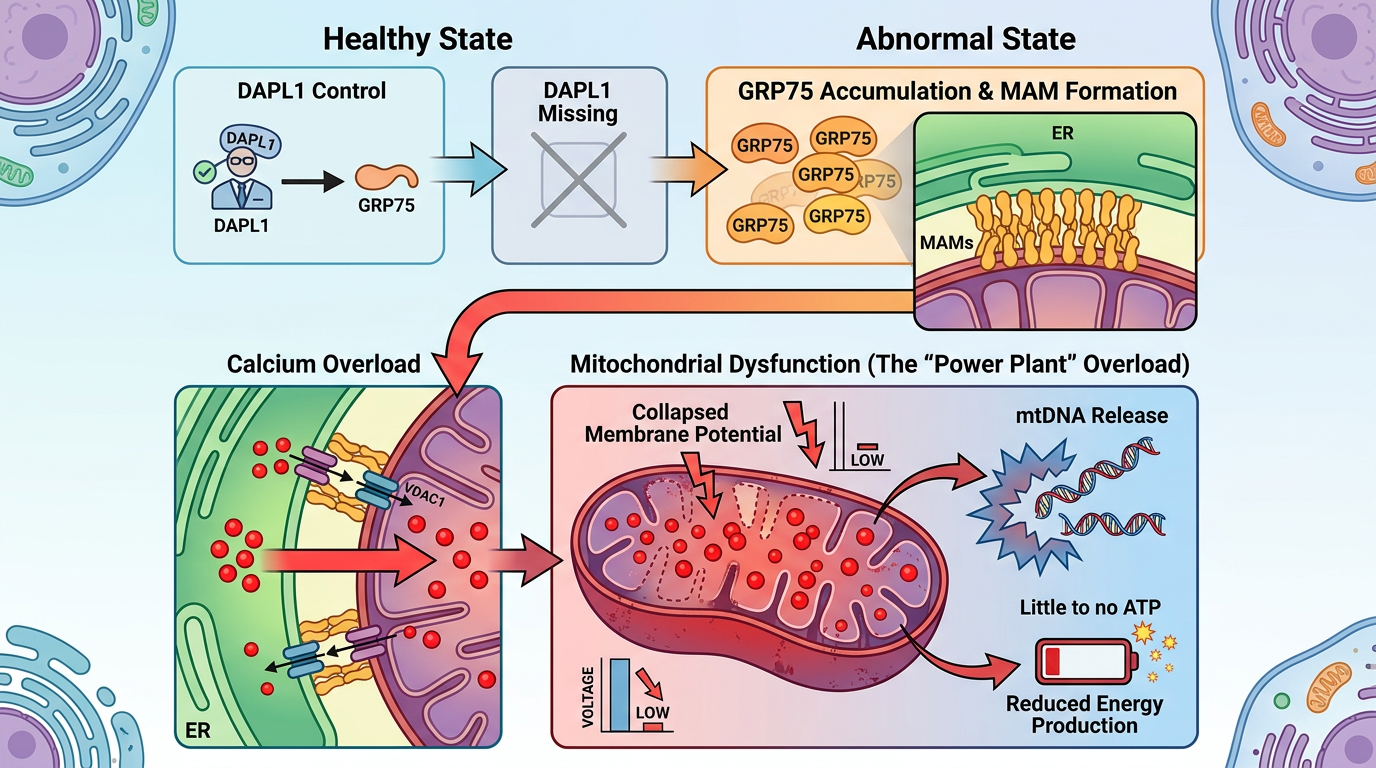
更糟的是,跑出来的线粒体DNA会激活细胞里的“炎症警报器”ZBP1,这个警报器一启动,就会召集起凋亡、坏死、焦亡三种死亡程序,形成一种叫PANoptosis的“混合死亡风暴”——RPE细胞不仅会自我溶解,还会释放炎症因子,把周围的健康细胞也拖进死亡循环。
为了确认这条死亡链条的真实性,团队在小鼠身上做了两组对照实验:一组敲除DAPL1基因,另一组同时敲除DAPL1和RIPK1——后者是PANoptosis的核心执行者。结果一目了然:只缺DAPL1的小鼠,视网膜上出现了干性AMD特有的地图样萎缩,RPE细胞成片死亡;而同时敲除RIPK1的小鼠,视网膜萎缩明显减轻,RPE细胞的存活率提高了30%。
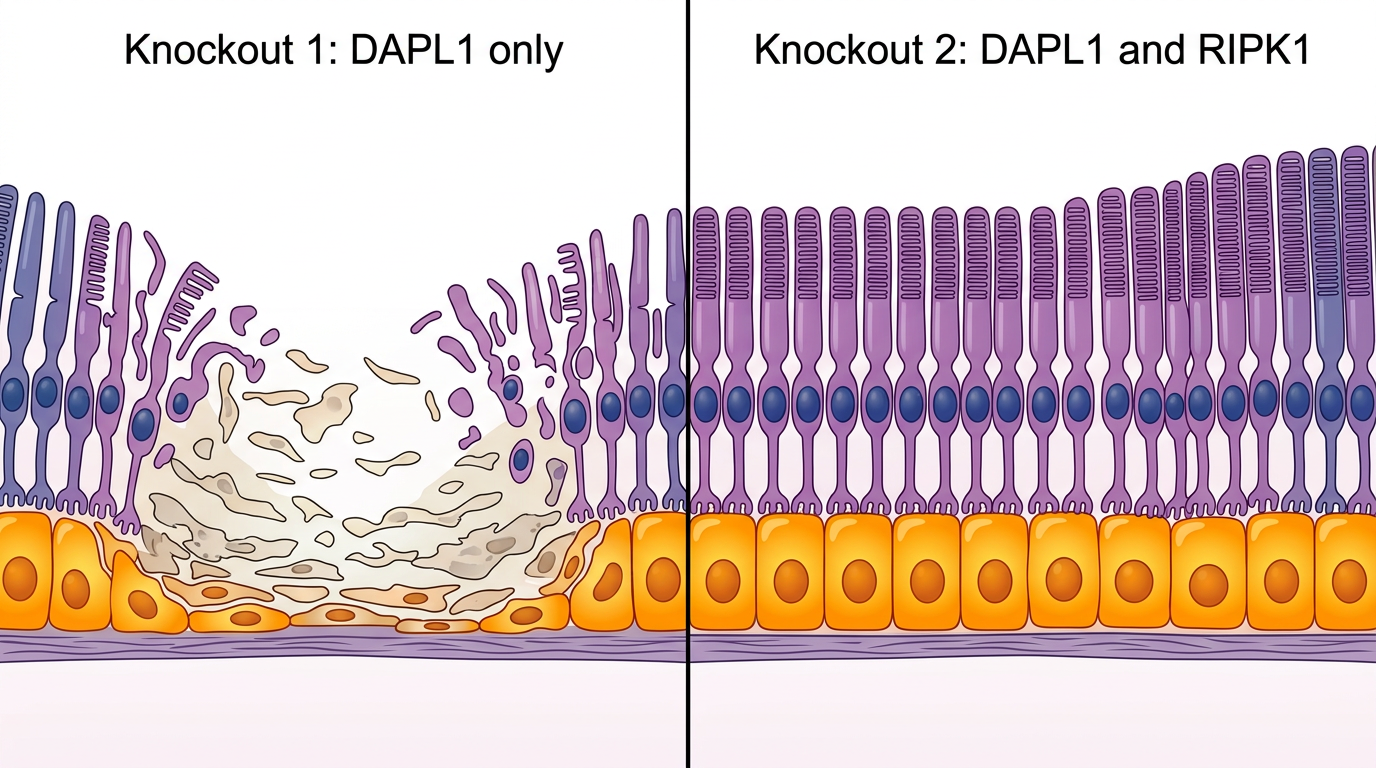
反过来,如果给小鼠的RPE细胞额外补充DAPL1,情况会完全逆转:GRP75的水平被压了下去,MAMs的数量回到正常,线粒体里的钙离子不再超载,PANoptosis也被彻底阻断。团队还在细胞实验里验证了关键数据:DAPL1缺失的RPE细胞,线粒体钙离子浓度是正常细胞的2-3倍,GRP75的蛋白量增加了近2倍,而敲低GRP75后,线粒体钙离子水平下降了60%,细胞存活率明显回升。
这里藏着一个很有意思的细节:GRP75的疯狂累积,不是因为它的基因被过度激活,而是因为DAPL1缺席后,GRP75的“保质期”被延长了——一种叫O-GlcNAc的糖基化修饰会粘在GRP75上,阻止它被细胞的“垃圾处理系统”降解。这也意味着,我们不一定非要从DAPL1入手,只要能打断GRP75的“续命”修饰,就能拆毁MAMs这条危险连线。
我认为,这项研究最有价值的地方,不是找到了一个新的基因靶点,而是第一次把干性AMD的病理过程,从“模糊的细胞死亡”细化成了“可精准干预的连锁反应”。过去我们对付干性AMD,只能用抗氧化剂或者营养补充剂“瞎猫碰死耗子”,现在我们可以直接瞄准GRP75、MAMs或者RIPK1,像拆炸弹一样一步步剪断死亡链条。
但我们也不能高估它的短期价值:目前所有实验都还停留在小鼠和细胞层面,人体的RPE细胞环境要复杂得多——比如人类的RPE细胞会积累一种叫脂褐素的垃圾,这种垃圾会不会影响DAPL1的功能?另外,GRP75在正常细胞里也有重要作用,直接敲低它会不会影响其他器官的线粒体功能?这些都是临床转化前必须解决的问题。
还有一个被忽略的点:干性AMD是一种年龄相关性疾病,DAPL1的缺失会不会只是衰老带来的“结果”,而不是“原因”?如果是后者,我们就算补上DAPL1,也挡不住衰老本身对RPE细胞的侵蚀。不过退一步说,哪怕只是延缓RPE细胞的死亡速度,对那些即将失明的老人来说,也是能多看清几年世界的希望。
当我们把目光从基因序列拉回现实,那些因为干性AMD而失明的老人,他们的世界不是突然变黑的,而是像被橡皮擦慢慢擦掉的——先看不清报纸上的字,再认不出家人的脸,最后连窗外的阳光都只剩一片模糊。
这项研究给了我们一把擦除“死亡链条”的橡皮:从DAPL1到GRP75,从MAMs到PANoptosis,每一个环节都可能成为延缓失明的突破口。“细胞的死亡不是终点,而是炎症的起点。” 未来的某一天,也许我们只要给眼睛滴一滴能抑制GRP75的药水,就能让那层薄如蝉翼的RPE细胞,多扛几年岁月的侵蚀。
点击充电,成为大圆镜下一个视频选题!