对抗知识焦虑,从看懂这条开始
App 下载
用患者细胞建微型人体,筛耐药乳腺癌特效药
药物筛选|耐药乳腺癌|微型人体系统|诱导多能干细胞|NF1突变|肿瘤学|合成生物学|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
药物筛选|耐药乳腺癌|微型人体系统|诱导多能干细胞|NF1突变|肿瘤学|合成生物学|生命科学|医学健康
同样是晚期乳腺癌,同样的靶向药,有人肿瘤缩小一半,有人却完全无效——这种绝望的差异,就藏在基因里。比如携带NF1突变的患者,癌细胞里的增殖信号像被焊死的油门,对几乎所有常规药物都耐药,中位无进展生存期只有6.2个月,还不到普通患者的一半。
现在,一群科学家给这类患者找到了新的可能:用患者自己的皮肤细胞,在实验室里重建一套包含肠、肝、肾和肿瘤的微型人体系统,像搭了个专属的药物试炼场,精准找出能打垮肿瘤的药。这到底是怎么做到的?
要搭建这个“药物试炼场”,第一步是拿到能变成任何器官的“种子细胞”——诱导多能干细胞(iPSCs)。你可以把它理解成一种“万能细胞”:从患者身上取一小块皮肤,用特殊的“重编程”因子处理,就能让已经分化的体细胞退回“婴儿状态”,重新获得分化成小肠、肝脏、肾脏甚至肿瘤细胞的能力。
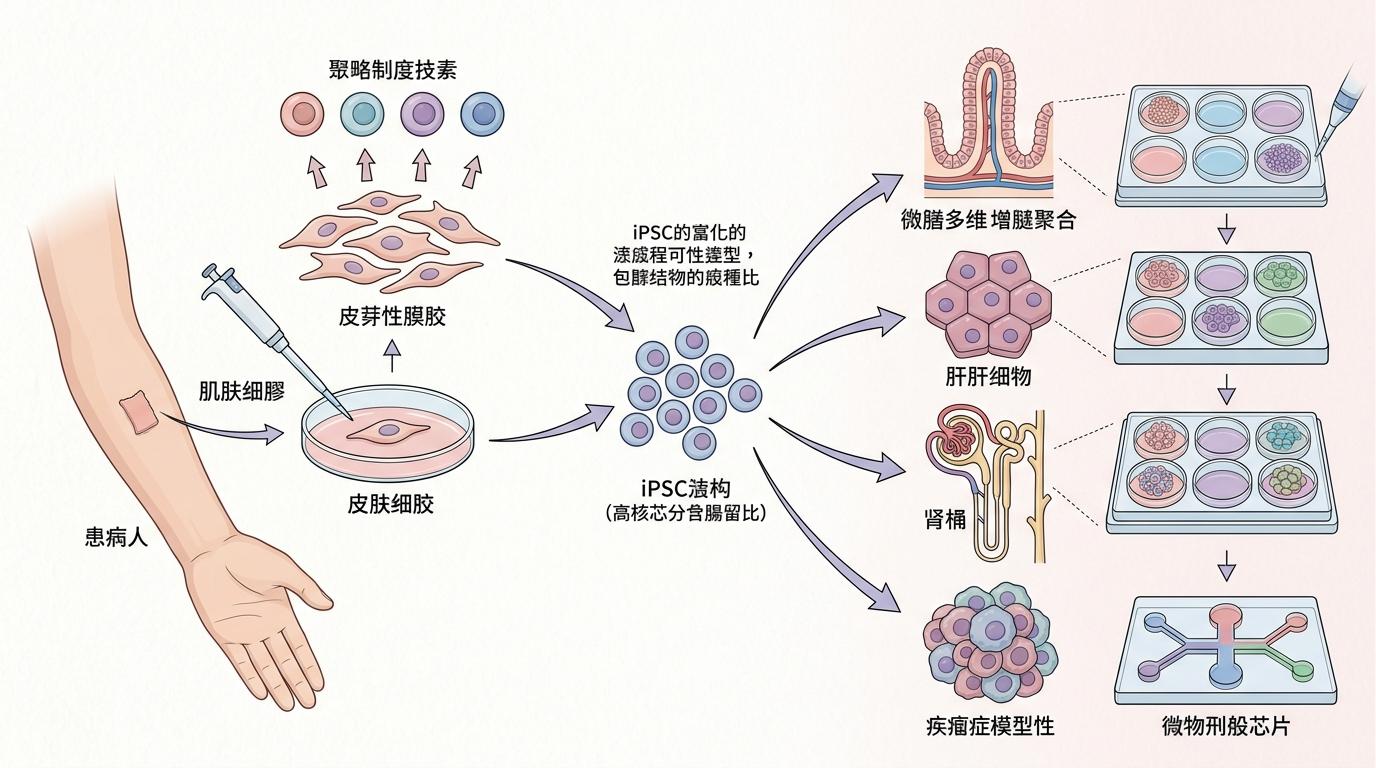
这种技术可不是近年的新发明。2006年日本科学家山中伸弥首次成功将体细胞重编程为iPSCs,还因此拿了诺贝尔奖。但过去的iPSC研究大多停留在单一器官模型,这次的突破在于,研究者把从同一患者iPSC分化来的小肠、肝脏、肾脏类器官,和患者的肿瘤细胞整合在了一起。
这套系统绝非样子货:小肠类器官长出了和人体一样的紧密连接,能模拟药物被肠道吸收的全过程;肝脏类器官能分泌代谢酶,像真肝脏一样把药物分解成活性或毒性成分;肾脏类器官则有专门的转运蛋白,负责药物的排泄。更关键的是,患者的NF1突变在这些器官模型里留下了真实痕迹——肝脏类器官的白蛋白分泌少了一半,药物代谢酶活性只有健康人的三分之一,这直接解释了为什么常规药物在他体内要么没效果,要么毒性过大。
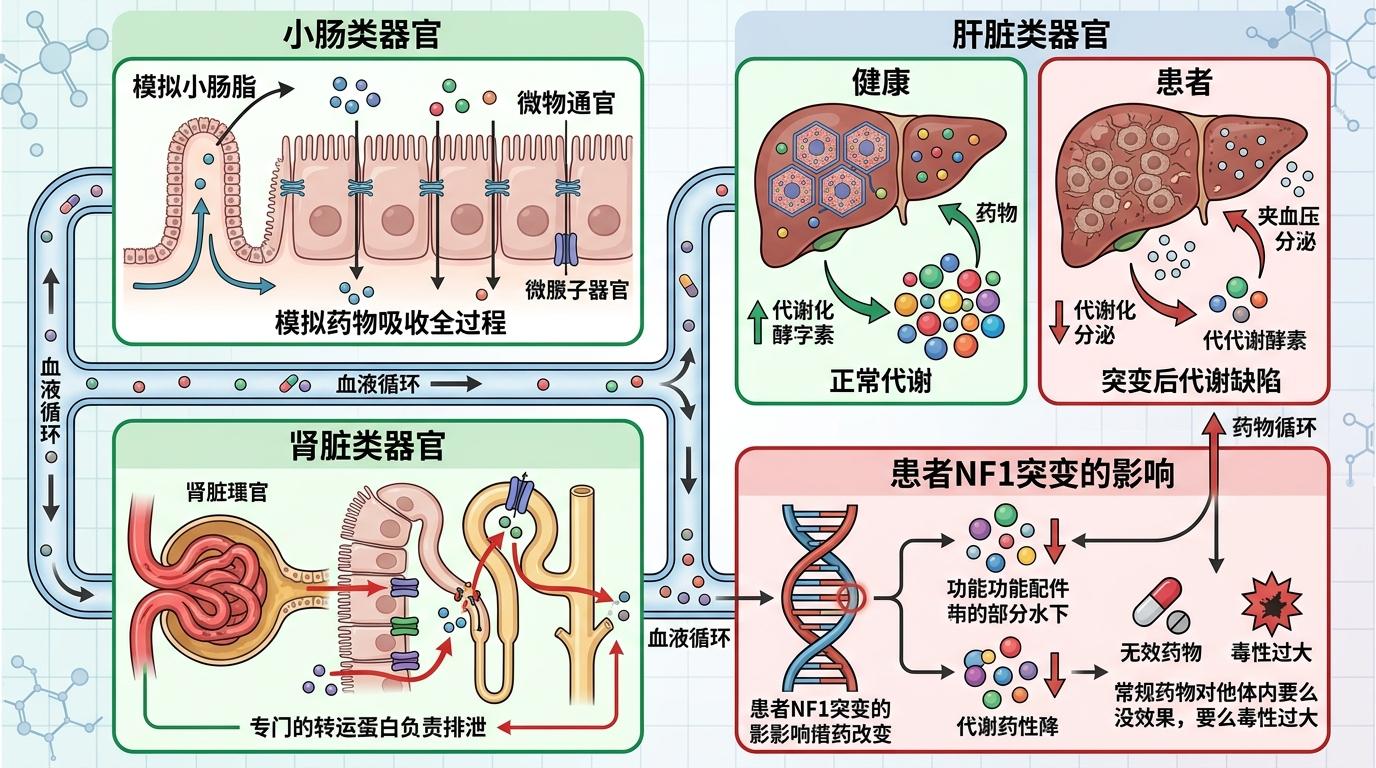
光有试炼场还不够,得先把癌细胞里那个“焊死的油门”松一松。研究者针对患者NF1基因的突变设计了“外显子跳跃”策略:用一段人工合成的反义寡核苷酸,像给错误的基因片段贴了个“跳过”标签,让细胞在合成蛋白质时自动忽略那段突变的序列,从而生成部分有功能的NF1蛋白。
简单说,这就像一本书里有几页印错了,直接把这几页粘起来,剩下的内容依然能读。为了让效果更持久,他们把这段寡核苷酸装进了慢病毒载体,让它能在细胞里持续发挥作用。处理后的肿瘤细胞里,NF1蛋白的表达量回升了40%,原本过度活跃的增殖信号通路也被踩下了刹车。
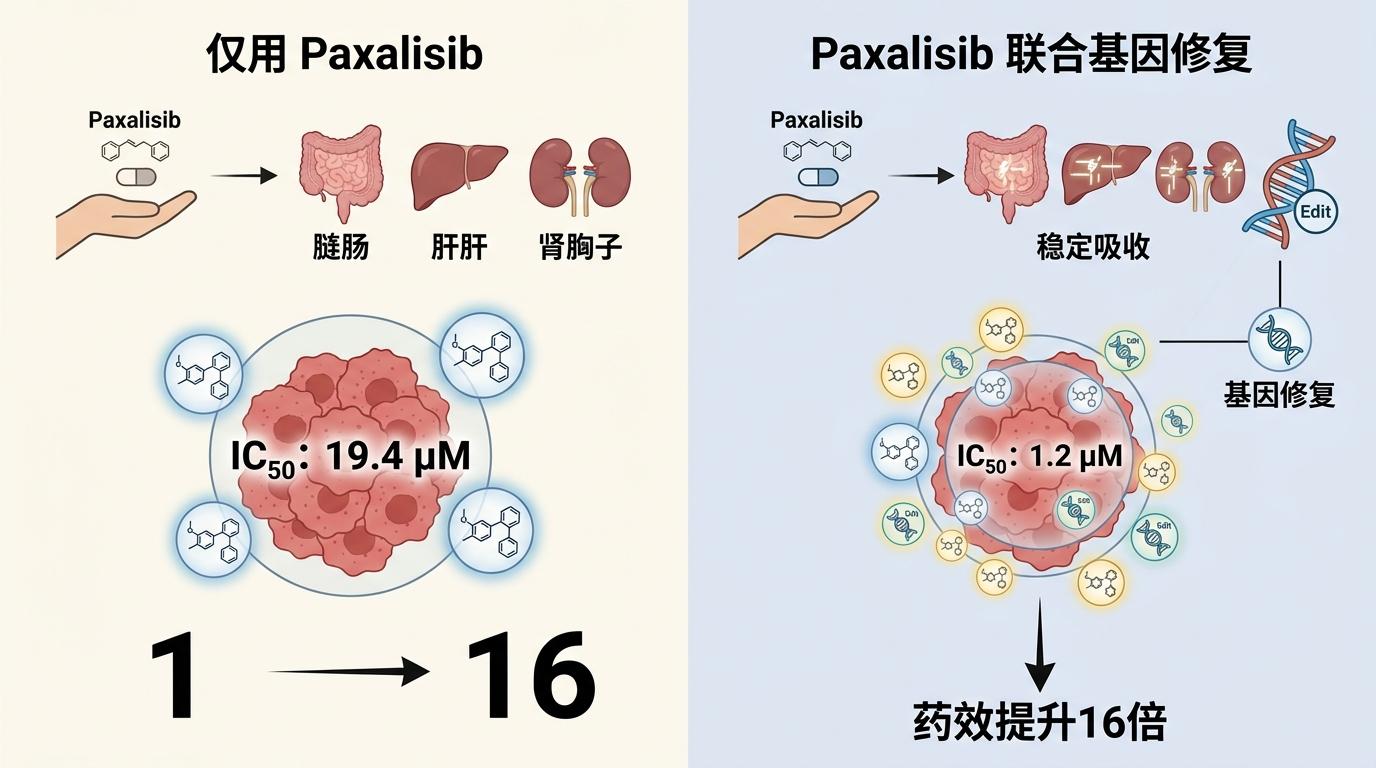
接下来就是在微型人体里试药。研究者选了8种针对PI3K-mTOR通路的双靶点抑制剂,逐一在这套多器官系统里测试。结果很明确:Paxalisib的口服吸收效果最好,在肠、肝、肾类器官里能维持稳定的有效浓度;而另一种已获批的药物口服吸收几乎为零,和它只能静脉注射的临床用法完全吻合。单独用Paxalisib时,抑制一半肿瘤细胞生长需要19.4μM的浓度,但联合基因修复后,这个浓度降到了1.2μM——药效提升了16倍。
在移植了患者肿瘤细胞的裸鼠身上,这个组合疗法同样起效:联合治疗组的肿瘤体积只有单药组的三分之一,肿瘤细胞的增殖率下降了60%,而小鼠的体重和器官功能完全没受影响。
当然,这项技术离走进医院还有不少坎要跨。首先是成本和效率问题:从患者身上取细胞,重编程为iPSC,再分化成四种器官类器官,整个过程需要4到6周,花费可能超过10万元,对于急需用药的晚期患者来说,时间和金钱都是不小的负担。
其次是标准化难题。目前的类器官培养还像“手工做菜”,不同实验室甚至同一实验室的不同批次,培养出的类器官功能都可能有差异。要让它成为临床常规检测手段,得像流水线生产一样实现标准化,还要解决类器官缺乏血管、免疫细胞等关键生理结构的问题——毕竟真实的人体里,药物还得和免疫系统、血液循环互动。
更不用说基因编辑的安全性:慢病毒载体虽然已经用了很多年,但依然存在整合到基因组随机位置的风险,可能引发意想不到的突变。而外显子跳跃策略也可能影响其他正常基因的剪接,这些都需要更长期的安全性验证。
当我们谈论精准医疗时,很多时候还停留在“根据基因选药”的阶段,但这项研究把它往前推了一大步——用患者自己的细胞建一个“替身”,先在体外把药试明白再用到人身上。
这不仅仅是技术的突破,更是一种思路的转变:不再把患者当成疾病的载体,而是把每个患者的身体当成独一无二的系统去理解和治疗。未来或许不用再纠结“为什么同样的药对我没用”,因为每个人都能拥有专属于自己的药物试炼场。
用患者的细胞,做患者的解药。这正是精准医疗最动人的地方——让医学终于跟上了生命的复杂性。