对抗知识焦虑,从看懂这条开始
App 下载
斯坦福造出双信号蛋白,精准诱导免疫耐受
器官移植|免疫耐受|调节性T细胞|双信号蛋白|斯坦福大学|自身免疫疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
器官移植|免疫耐受|调节性T细胞|双信号蛋白|斯坦福大学|自身免疫疾病|医学健康
想象一下:过敏发作时不用躲着花粉,得了类风湿不用靠激素止疼,甚至器官移植后能摆脱终身吃免疫抑制剂的日子——这些场景,正在从科幻靠近现实。2026年3月,斯坦福大学的科学家造出了一种「双信号蛋白」,它能像精准开关一样,在体内唤醒一群专门管「免疫刹车」的细胞,让免疫系统学会「认亲」,不再乱攻击自身组织或无害物质。为什么这个蛋白能做到之前疗法做不到的事?答案藏在免疫系统最核心的信号密码里。
要理解这个蛋白的厉害,得先搞懂免疫系统的「刹车失灵」问题:我们体内有一种叫调节性T细胞(Treg)的免疫细胞,它像免疫系统的交警,专门叫停过度的免疫攻击——比如阻止免疫系统误杀自身细胞,或是对花粉、牛奶这类无害物质反应过度。
但Treg的激活有个苛刻条件:必须同时收到两个信号——IL-2的「启动信号」和TGF-β的「分化信号」。就像你开保险箱,得同时输对密码和刷指纹,少一个都不行。过去的疗法要么只给IL-2,要么只补TGF-β,最多就是把两者混合注射,结果要么激活了不该激活的免疫细胞,要么信号太弱,Treg根本醒不来。
斯坦福团队的解决办法,是把IL-2和一种线虫来源的低亲和力TGF-β模拟物,用一条蛋白链「焊」在一起,做成了一个「双信号蛋白」。它就像个自带双验证的钥匙,只会去找那些表达IL-2受体的T细胞,然后同时激活STAT5和SMAD2/3两条信号通路,精准把普通T细胞改造成专职「交警」的Treg。
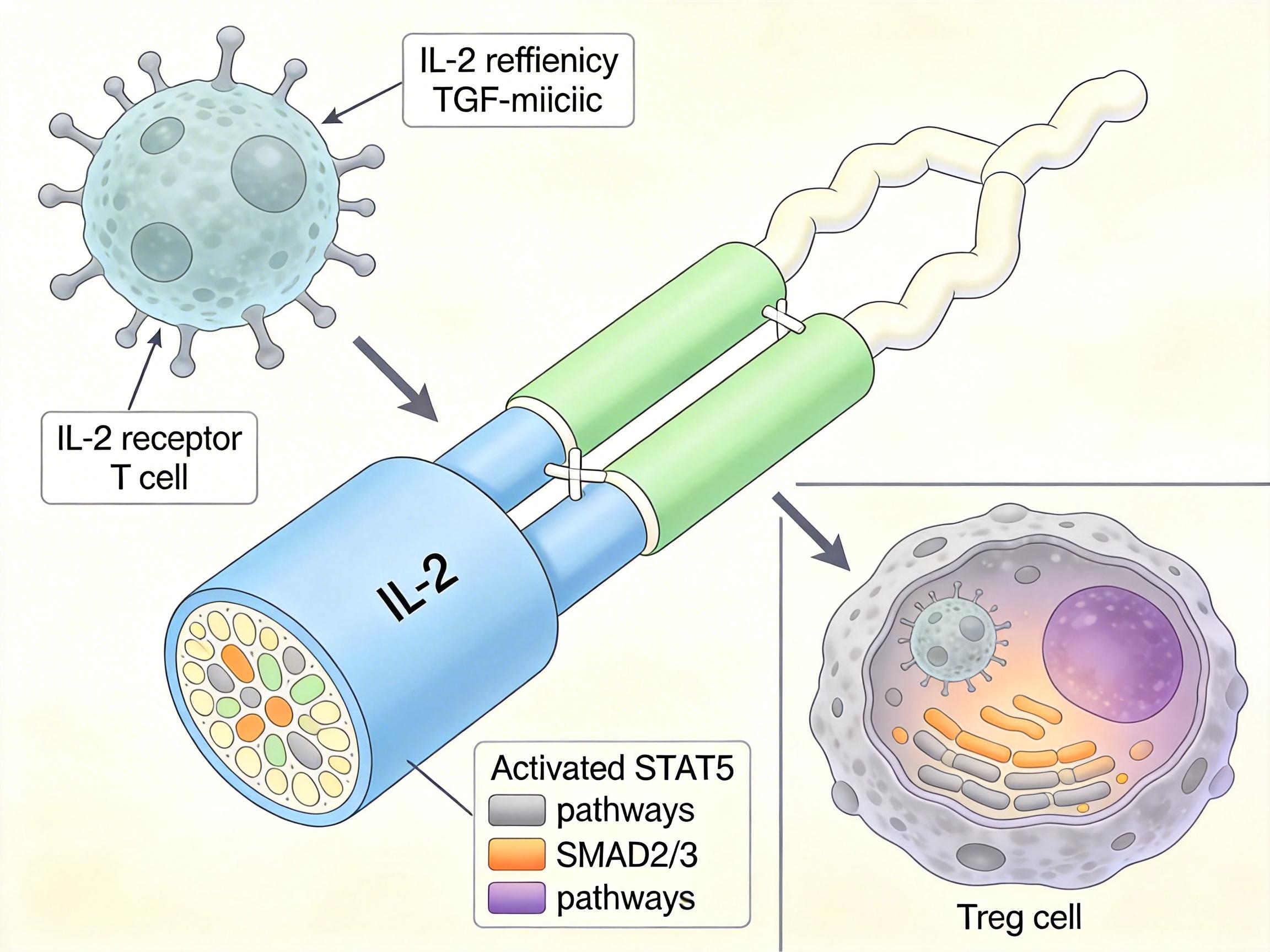
直给的技术逻辑是:
在实验室的培养皿里,这个双信号蛋白展现出了惊人的效率:它诱导Treg分化的能力,比单独混合IL-2和TGF-β强了100倍。但真正的考验是在活体内——毕竟培养皿里的细胞和复杂的体内环境完全是两回事。
科学家给小鼠注射了卵白蛋白(一种常见过敏原)和髓鞘蛋白(引发自身免疫性脑脊髓炎的关键抗原),然后用双信号蛋白处理。结果让人兴奋:小鼠体内高达80%的抗原特异性T细胞,都被改造成了Treg。这些Treg不是「躺平」的假交警,它们高表达RORγt,能像特种兵一样精准迁移到炎症部位,还能分泌多种抑制因子,把过度的免疫攻击掐灭在源头。
在过敏性哮喘模型里,注射双信号蛋白的小鼠,肺部炎症细胞浸润减少了70%,IgE抗体水平直接降到接近正常;在自身免疫性脑脊髓炎模型里,小鼠的瘫痪症状明显减轻,中枢神经系统的炎症几乎消失。更重要的是,这些Treg能长期稳定存在,不会轻易「叛变」回攻击性T细胞——它们的FOXP3基因调控区保持着去甲基化状态,相当于拿到了终身交警执照。
我认为,这项研究最被低估的一点,是它解决了过去免疫耐受疗法的核心痛点:特异性。传统的免疫抑制剂是「一刀切」,把整个免疫系统的活性都压下去,患者容易感染、得癌症;而这个双信号蛋白只针对特定抗原激活的T细胞,相当于只叫停针对「自己人」或「无害物」的攻击,不影响免疫系统对抗真正的病原体。

当然,这个双信号蛋白离真正走进医院,还有几道坎要跨。
首先是安全性:虽然小鼠实验里没发现明显副作用,但人体的免疫系统比小鼠复杂得多。比如,双信号蛋白会不会意外激活某些隐藏的攻击性T细胞?会不会影响NK细胞的功能?这些都需要大规模的临床试验来验证。
其次是生产成本:这种融合蛋白需要用哺乳动物细胞表达系统生产,目前的成本还很高。如果要用于长期治疗,必须优化生产工艺,把成本降下来,才能让更多患者用得起。
最后是个性化问题:不同患者的免疫系统状态不一样,过敏原或自身抗原也千差万别。未来可能需要根据患者的具体情况,定制不同的双信号蛋白,或是结合抗原递呈技术,实现更精准的免疫耐受诱导。
不过,这些问题都是技术层面的,而非原理上的障碍。目前已经有几家生物科技公司盯上了这项技术,预计最快2028年就能进入一期临床试验。
从1995年FOXP3基因被发现,到今天双信号蛋白精准诱导Treg,人类对免疫耐受的理解,终于从「摸着石头过河」走到了「精准调控」的阶段。
我们一直在和免疫系统的「错误攻击」做斗争:从最早的激素疗法,到后来的免疫抑制剂,再到现在的Treg疗法,每一步都是在寻找「精准刹车」的开关。而这个双信号蛋白,就是我们找到的最接近完美的开关之一。
精准调控免疫,才是未来的方向。它不仅能治疗过敏、自身免疫病,还可能为器官移植、甚至某些癌症的治疗打开新的大门。毕竟,有时候让免疫系统停下来,比让它发动攻击更重要。