
1 个月前

1 个月前
中国每两个胃癌患者里,就有一个会在放化疗中逐渐“失效”——肿瘤细胞像练就了金刚不坏之身,能快速修复治疗造成的DNA损伤。复旦大学的研究团队最近揪出了这个“修复外挂”的核心:一个原本管细胞“快递”的蛋白EXOC4,竟会偷偷溜进细胞核,给癌细胞的DNA修复系统“开加速”。更关键的是,他们找到了能把这个蛋白“锁”在细胞质里的办法,让耐药的肿瘤重新对治疗敏感。这到底是怎么做到的?
EXOC4原本是细胞里的“资深快递员”——它是胞外分泌体复合物的核心成员,专门负责把细胞生产的蛋白、囊泡精准运送到细胞膜上。但在胃癌细胞里,它被一个叫p300的“化妆师”盯上了:p300会给EXOC4的第433位赖氨酸“刷”上一个乙酰化标记,就像给它贴了张“核内通行证”。
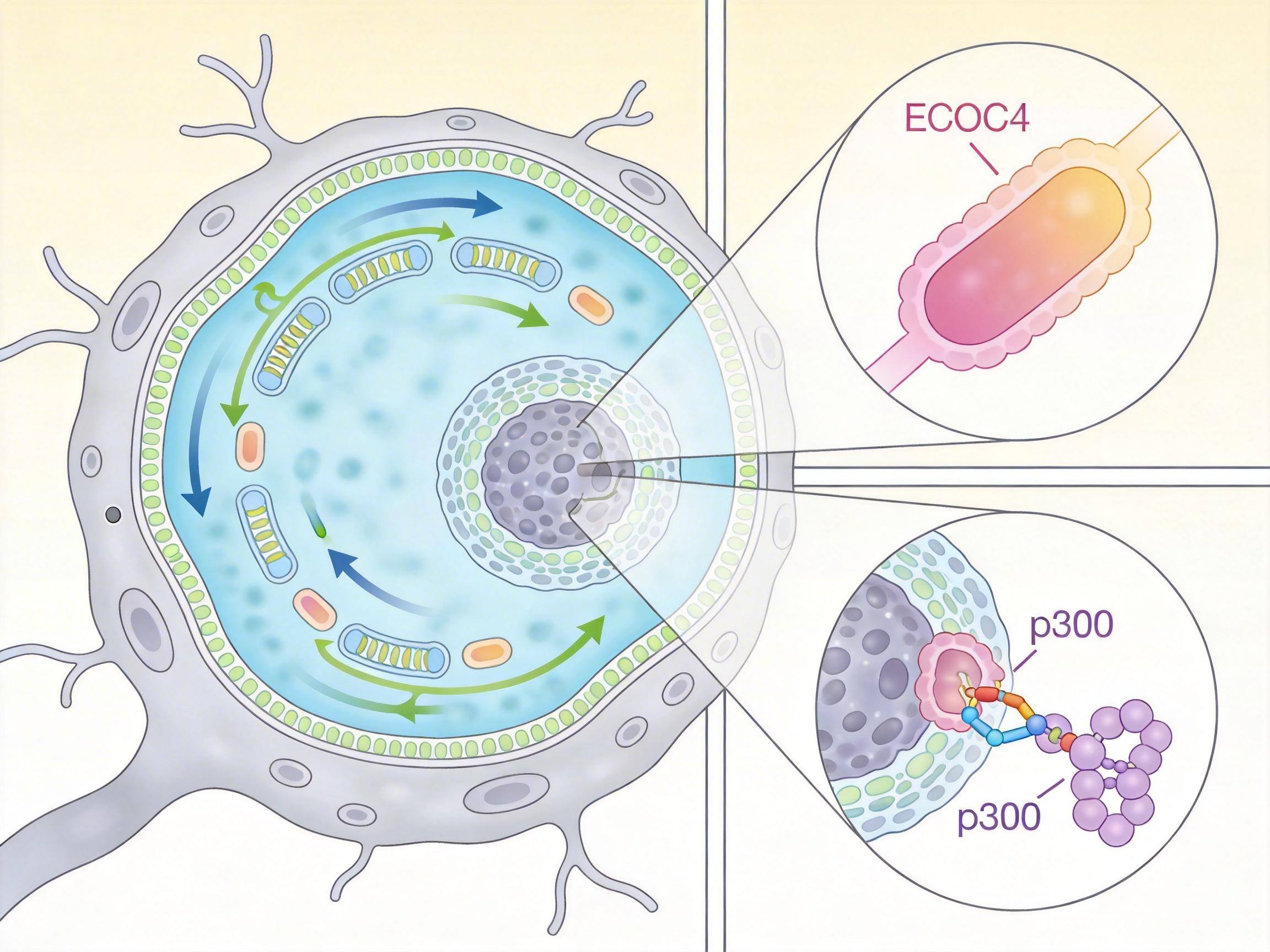
有了这张通行证,EXOC4就能穿过核孔,从细胞质的“快递站”直接跳进细胞核。这是个颠覆性的发现——过去没人想到,一个管运输的蛋白,会在细胞核里扮演完全不同的角色。
直给机制链: p300催化EXOC4 K433乙酰化 → EXOC4获得核定位能力 → 进入细胞核调控DNA修复
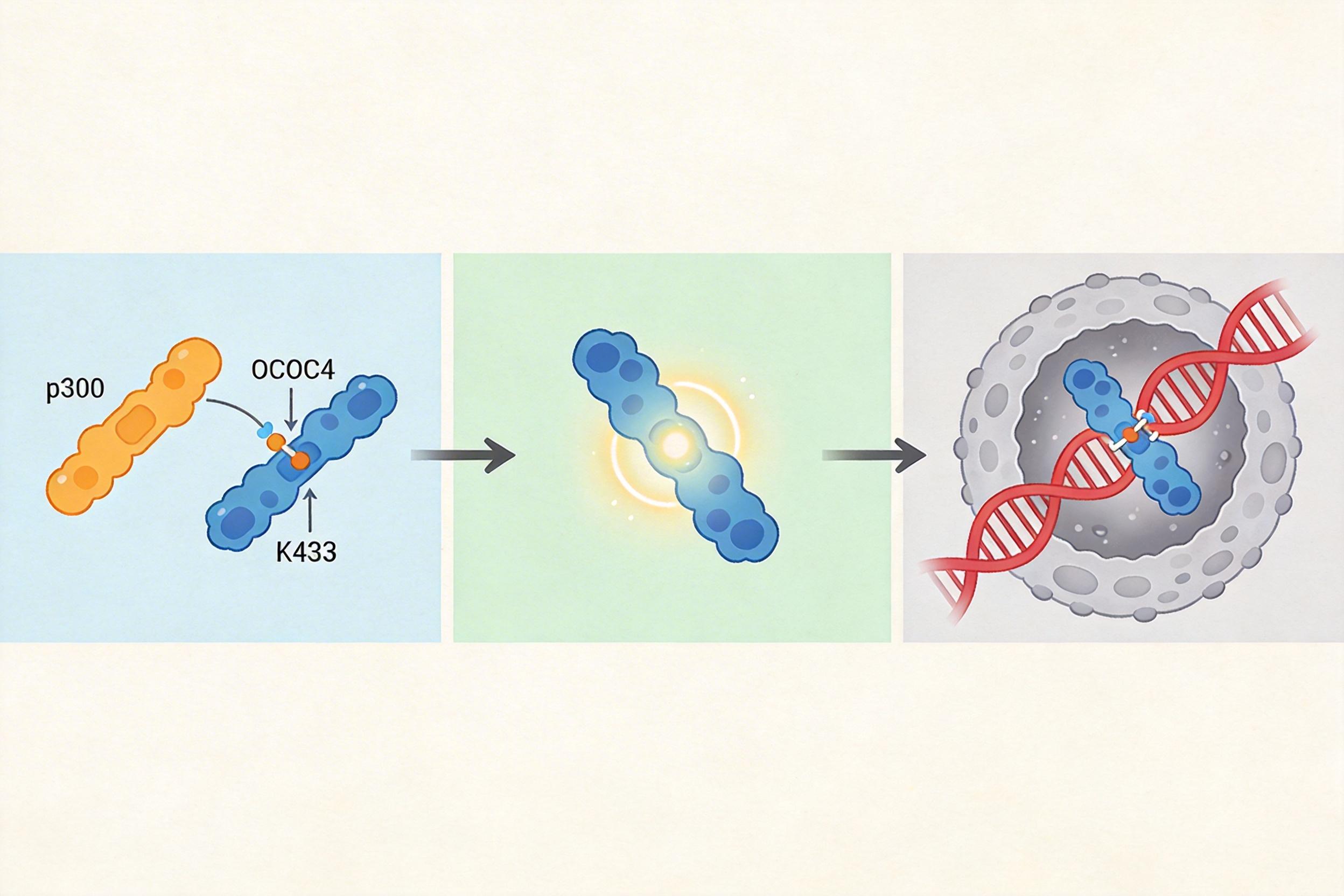
进入细胞核的EXOC4,立刻变成了DNA修复系统的“调度员”。它会主动牵线,让蛋白精氨酸甲基转移酶PRMT5和DNA修复核心蛋白KU70凑到一起。PRMT5就像个“刻章师傅”,会在KU70的第318位精氨酸上刻一个甲基化标记。
你可以把KU70想象成DNA断裂处的“抓钩”——原本它抓DNA的力气有限,但被PRMT5刻上标记后,抓力瞬间变强,能更快找到DNA双链断裂的缺口,拉起KU80、DNA-PKcs等“工友”一起修补。这个过程叫非同源末端连接(NHEJ),是癌细胞修复放化疗损伤的最快路径。
但真实的机制比这更精确:KU70的R318甲基化,直接增强了KU复合物与DNA断裂末端的结合亲和力,让修复速度提升了30%以上——这就是癌细胞能扛住放化疗的核心原因。
既然找到了耐药的关键通路,研究团队设计了一款精准“锁扣”:一段靶向EXOC4 K433位点的多肽。它能精准堵住p300给EXOC4贴“通行证”的位置,让EXOC4老老实实在细胞质里当快递员,没法再溜进细胞核搞破坏。
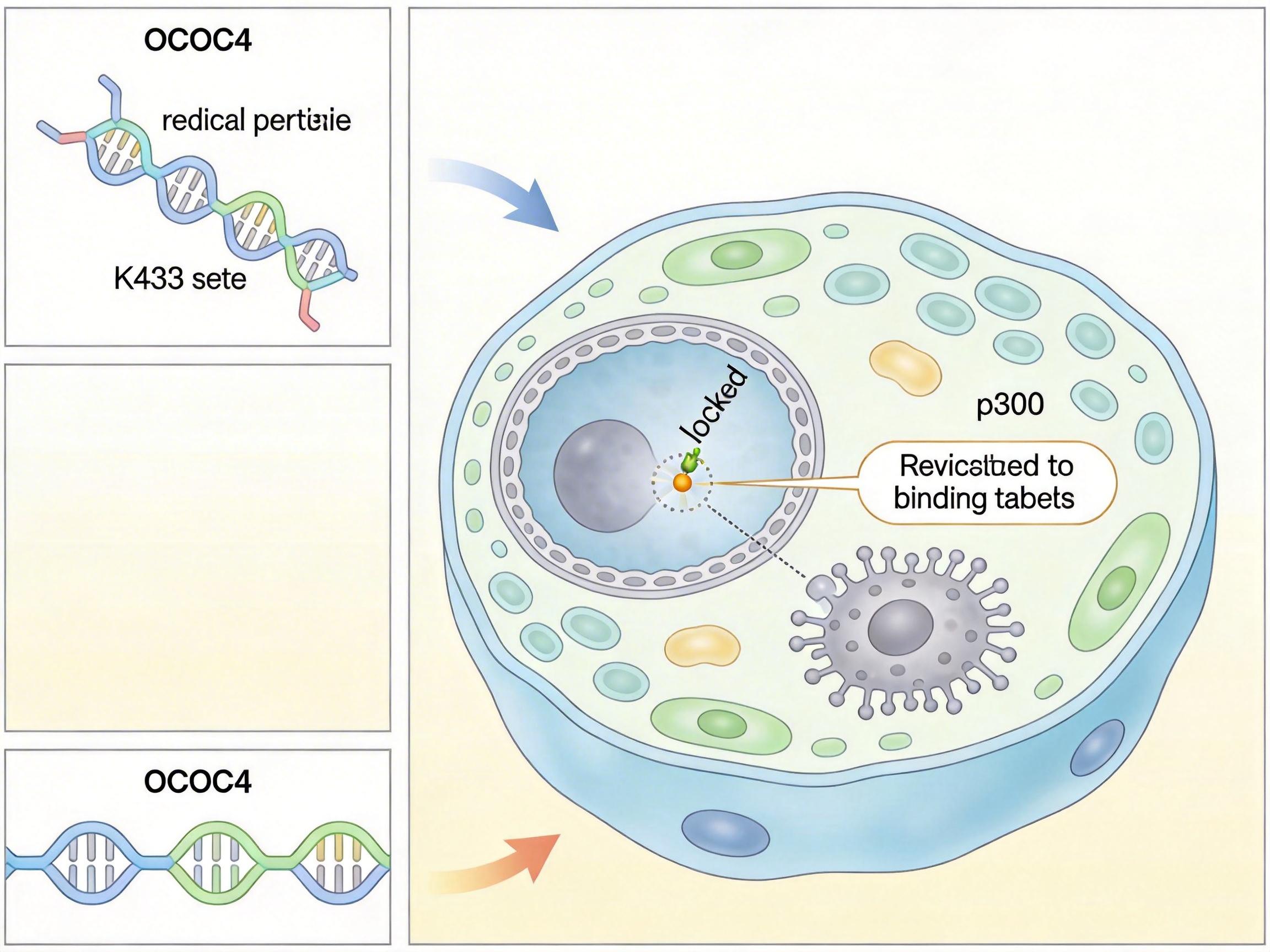
在临床前模型里,这款多肽展现出了强大的效果:它能让KU70的甲基化水平下降40%,癌细胞的DNA修复速度直接减半,原本对放化疗耐药的肿瘤,重新变得敏感——单独化疗只能让肿瘤缩小20%,加上多肽后,肿瘤缩小了70%还多。
当然,这一策略也有局限:多肽的稳定性和体内递送效率还需要优化,而且它只针对EXOC4介导的耐药通路,对其他机制导致的耐药可能无效。但它给胃癌治疗提供了一个全新的靶点,也让我们看到了“精准阻断蛋白修饰”这种治疗思路的潜力。
过去我们总把癌细胞的耐药归咎于“基因突变”,但这次的研究让我们看到,蛋白的“后天修饰”可能才是更隐蔽的帮凶——一个小小的乙酰化标记,就能让一个蛋白彻底改变定位和功能,给癌细胞装上“修复外挂”。
“蛋白修饰,是癌细胞的隐形武器。”这句话或许能概括这个发现的核心意义:未来的癌症治疗,或许不止要盯着基因突变,还要盯着这些蛋白身上的“小标记”——它们可能是打开耐药大门的新钥匙。而这款能锁住EXOC4的多肽,就是第一把试对了齿的钥匙。
点击充电,成为大圆镜下一个视频选题!