对抗知识焦虑,从看懂这条开始
App 下载
三种凶险儿童脑肿瘤,共享同一致命软肋
细胞发育地图|感光机制|Group 3型髓母细胞瘤|视网膜母细胞瘤|松果体母细胞瘤|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
细胞发育地图|感光机制|Group 3型髓母细胞瘤|视网膜母细胞瘤|松果体母细胞瘤|肿瘤学|医学健康
美国每年仅20例的松果体母细胞瘤,全球年发8000例的视网膜母细胞瘤,还有儿童最常见恶性脑肿瘤里预后最差的Group 3型髓母细胞瘤——这三种长在大脑不同角落、被医学界当成独立疾病治了几十年的肿瘤,最近被揪出了共通的命门。它们像三台装了同款核心系统的机器,一旦系统崩溃,所有机器都会停摆。更关键的是,这套让它们疯狂生长的系统,居然和我们眼睛里的感光机制一模一样。为什么偏偏是这些部位的肿瘤如此凶险?它们隐秘的联系到底藏着什么治疗转机?
要搞懂肿瘤的命门,得先知道它从哪来。研究人员先画了张正常松果体发育的「细胞地图」——这是全球首张完整记录松果体从胚胎到成熟所有细胞变化的单细胞图谱。拿着这张地图,他们比对了38例松果体母细胞瘤样本的基因表达,发现这些肿瘤细胞最像一种叫「松果体细胞前体细胞」的早期细胞:本该继续分化成熟的它们,卡在了发育的半路上,还把一套感光基因程序拉满了马力。
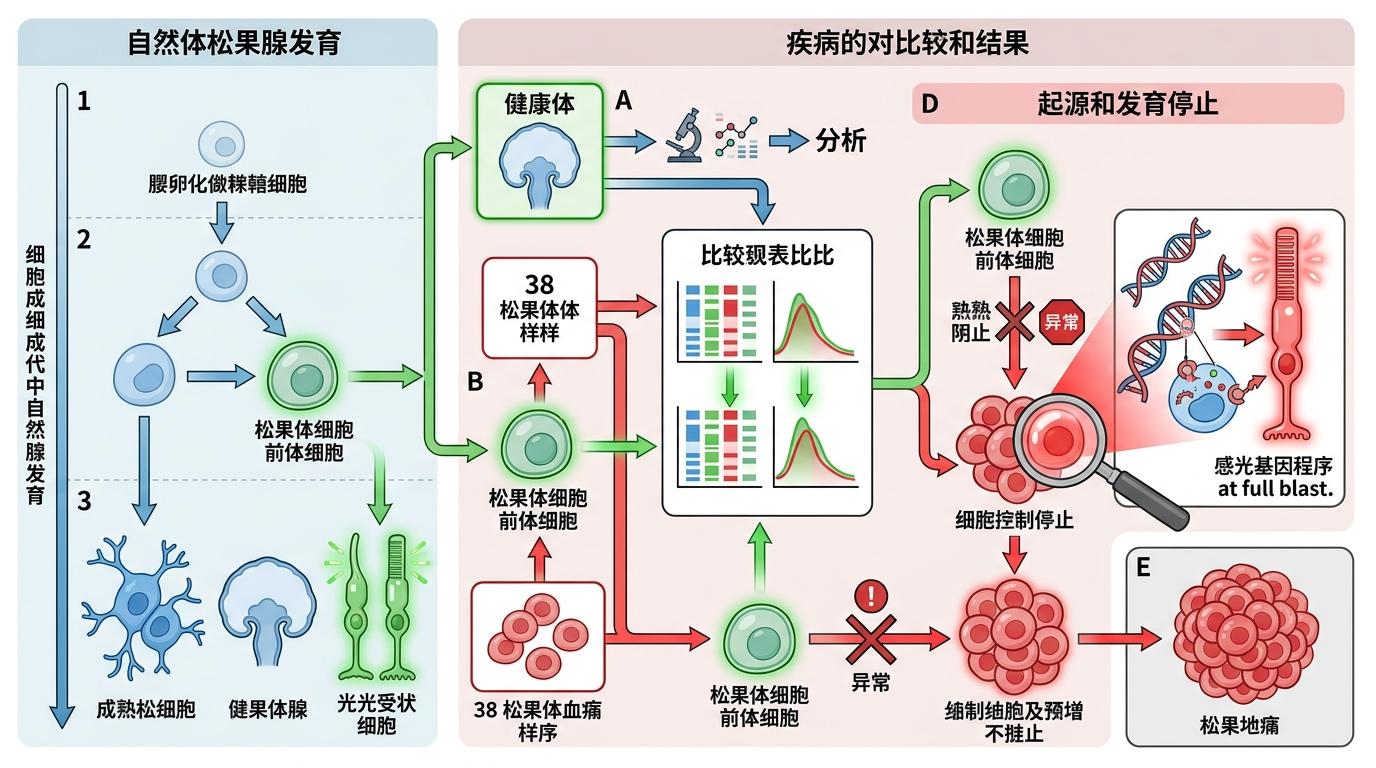
你可以把这套程序想象成肿瘤的「能量开关」——正常的松果体细胞只会用它来接收光信号、调节昼夜节律,但肿瘤细胞把它当成了生存的核心动力。更意外的是,当研究人员把目光投向另外两种肿瘤时,发现视网膜母细胞瘤和Group 3型髓母细胞瘤的细胞里,也亮着同样的「开关」。
这不是巧合。松果体在进化上是人类的「第三只眼」,天生带感光潜能;视网膜本身就是感光器官;就连小脑的部分区域,在胚胎发育时也和感光信号有过交集。这些肿瘤,其实都是胚胎时期带感光记忆的细胞,在癌变后把这份记忆异常激活了。
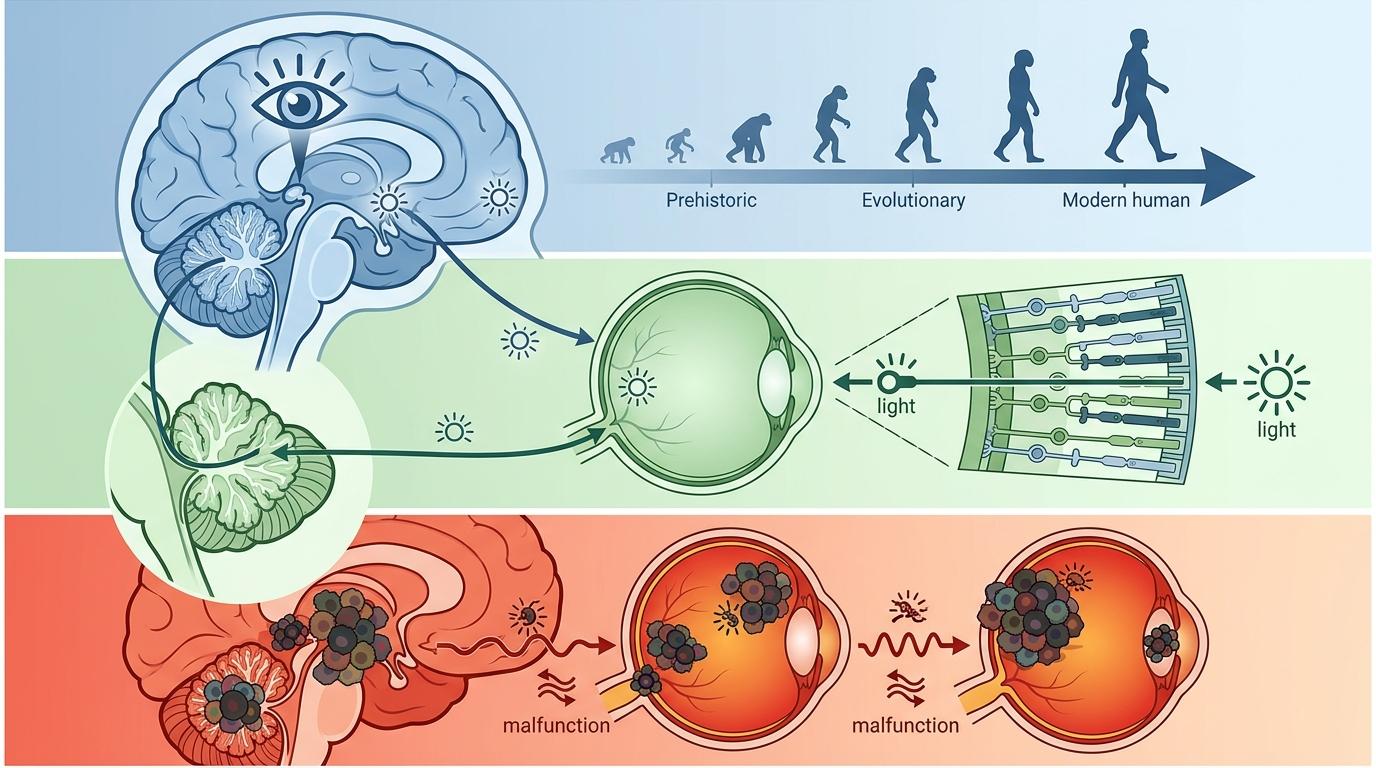
为了验证这套感光程序是不是真的命门,研究人员用了CRISPR基因编辑技术——你可以把它当成一把精准的分子剪刀,专门剪断目标基因的表达。
他们分别在三种肿瘤的细胞样本里,剪掉了感光程序里的关键基因。结果完全一致:
肿瘤细胞开始大量死亡。
而正常的脑细胞,却几乎没受影响。
这意味着这套程序是肿瘤的「专属软肋」——只有依赖它生存的癌细胞会因为失去它而死亡,正常细胞根本不需要这套程序来维持运转。更重要的是,这三种肿瘤不管起源于哪个部位、有什么驱动基因突变,只要剪断这根共同的「电线」,就都会断电。
之前的治疗思路,是给不同部位的肿瘤开不同的药方:松果体母细胞瘤要做颅脑放疗,视网膜母细胞瘤可能要摘除眼球,Group 3型髓母细胞瘤得靠大剂量化疗。但这些治疗不仅对孩子的发育伤害极大,五年生存率最高的也不到60%。现在,终于有了一个可能同时瞄准三种肿瘤的靶点。
当然,现在就说能治愈还太早。从这个发现到真正的药物,至少要闯过三道关:
第一关是找对最关键的靶点。这套感光程序里有上百个基因,到底哪个是最核心的「开关」?研究人员已经锁定了几个关键的转录因子,但还需要更精准的筛选。
第二关是让药物穿过血脑屏障。大脑就像一个被严密防守的堡垒,98%的药物都进不去。要让靶向感光程序的药物到达肿瘤部位,得给它装个「通行证」——比如修饰成能被脑内特定受体识别的分子,或者用纳米载体打包递送。
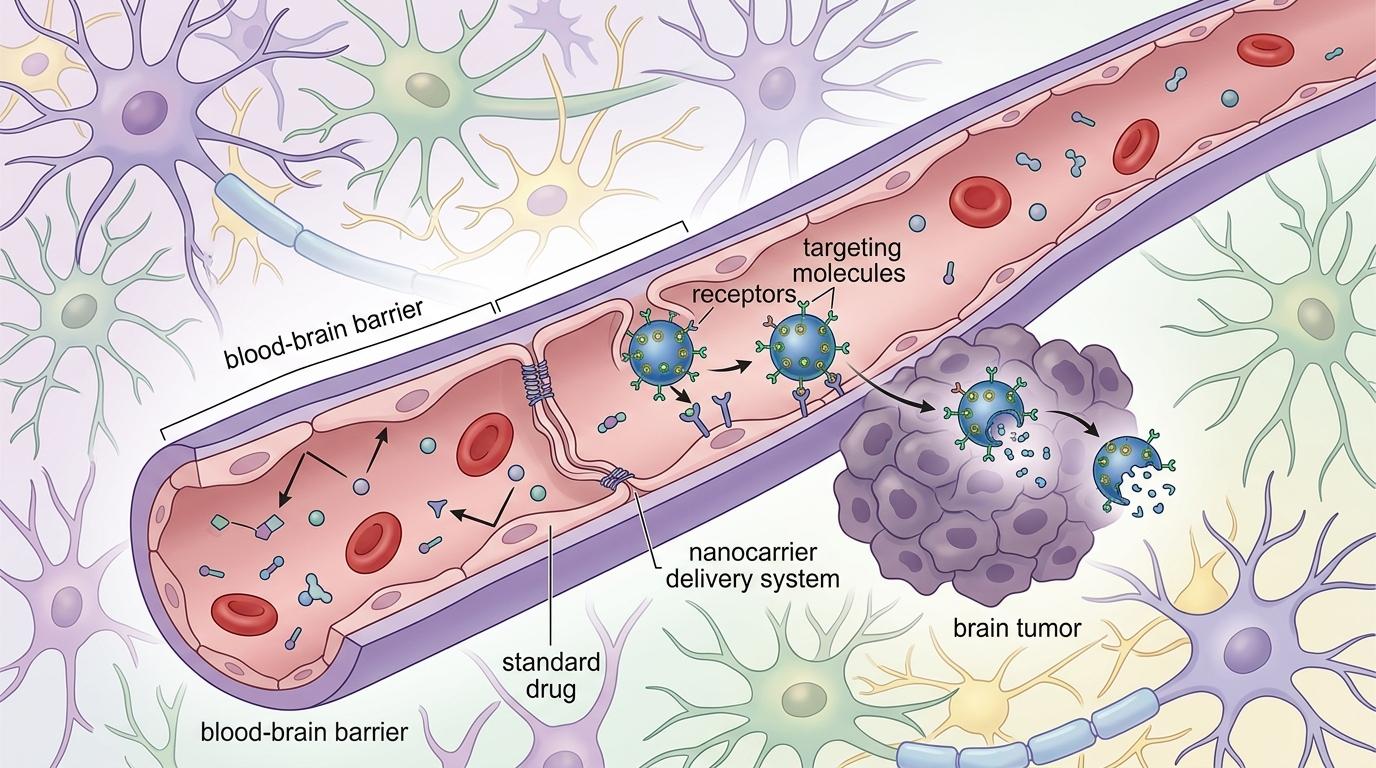
第三关是验证安全性。儿童的大脑还在发育,任何治疗都不能留下长期损伤。之前的化疗和放疗会导致认知障碍、听力损失,新的靶向药物必须能精准区分肿瘤细胞和正常细胞,把副作用降到最低。
更值得关注的是,这个发现打破了「肿瘤按部位治疗」的惯性思维。未来我们或许会发现更多跨部位的肿瘤共享机制,把那些被当成「罕见病」的零散研究,聚成能互相支撑的力量——毕竟对孩子来说,每一种罕见病,都是一个家庭的全部。
现在,研究人员已经在黑暗里摸到了那束光——那束原本该用来感受昼夜、看见世界的光,被肿瘤偷去当成了生长的燃料,如今又成了照亮治疗方向的火把。
「同病异治」的时代或许正在过去,「异病同治」的大门正在打开。对那些被罕见脑肿瘤困住的孩子和家庭来说,这不仅是一个科学发现,更是一份实实在在的希望:原来那些看似孤立的绝境,底下藏着同一条通往生机的路。
金句:共享的软肋,是跨越绝境的共同出口