3 个月前

3 个月前
同样的饭局,一桌咸香四溢的菜肴过后,为何有人安然无恙,有人却感到血压计上的数字悄然攀升?长期以来,我们将这种差异归咎于遗传或生活习惯。然而,一个更深层的秘密,隐藏在人体最喧闹繁华的“内部都市”——肠道之中。这个由数万亿微生物构成的生态系统,正像一位隐形的审判官,悄然决定着盐分进入我们身体后的命运。
高盐饮食,这个被公认为全球疾病负担首要诱因的“餐桌杀手”,它与高血压的关联早已是医学界的共识。但“为何盐对不同人影响迥异”的谜题,始终缺乏一块关键的拼图。直到2025年底,一扇通往答案的大门被中国科学家猛然推开。
2025年12月26日,顶级期刊《自然·通讯》(Nature Communications)上发表的一项研究,为这个古老的问题带来了突破性解答。由中国医学科学院/北京协和医科大学的顾东风院士与鲁向锋教授团队主导的研究,精准地描绘出了一条全新的调控通路:高盐膳食—肠道微生物—酰基肉碱代谢—高血压。
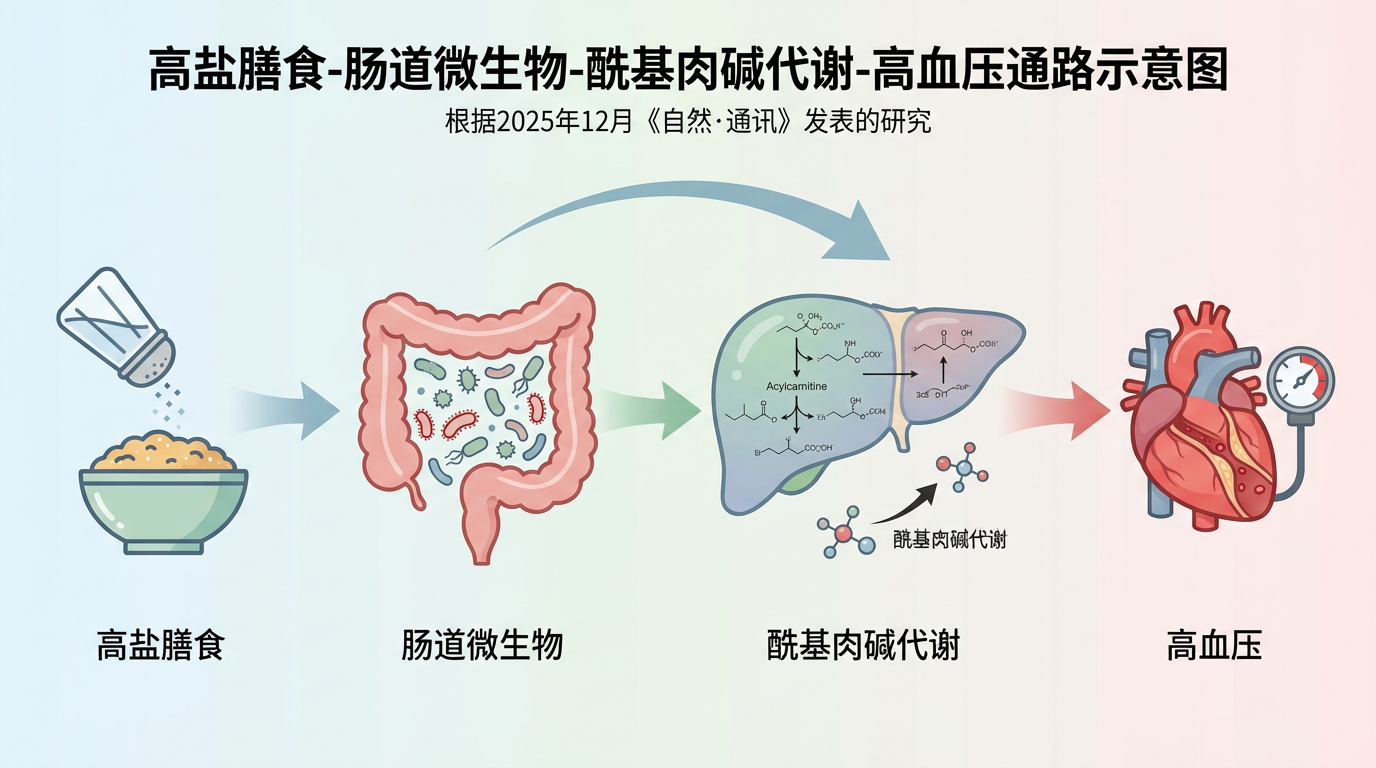
这项名为MetaSalt的多中心膳食盐干预试验,设计精妙而严谨。研究团队招募了528名受试者,让他们在23天内经历了一场从低盐(每日3克)到高盐(每日18克)的“盐分过山车”。通过对受试者粪便和血液样本的深度分析,科学家们捕捉到了惊人的变化:
在这场由盐导演的微观生态风暴中,一个名为**异戊酰肉碱(isovalerylcarnitine)**的分子脱颖而出,成为了故事的主角。研究人员发现,它是一个关键的“血压守护者”。
异戊酰肉碱,这种由特定肠道菌群产生的代谢物,在高盐饮食的冲击下水平显著下降。更关键的是,在那些血压对盐分反应剧烈的“盐敏感”个体中,这种下降尤为惨烈。这仿佛一艘守护血管健康的护卫舰,在高盐的“惊涛骇浪”中失去了动力。
为了验证这一发现,研究团队构建了“人群干预试验+动物实验+队列随访”的多层级证据链:
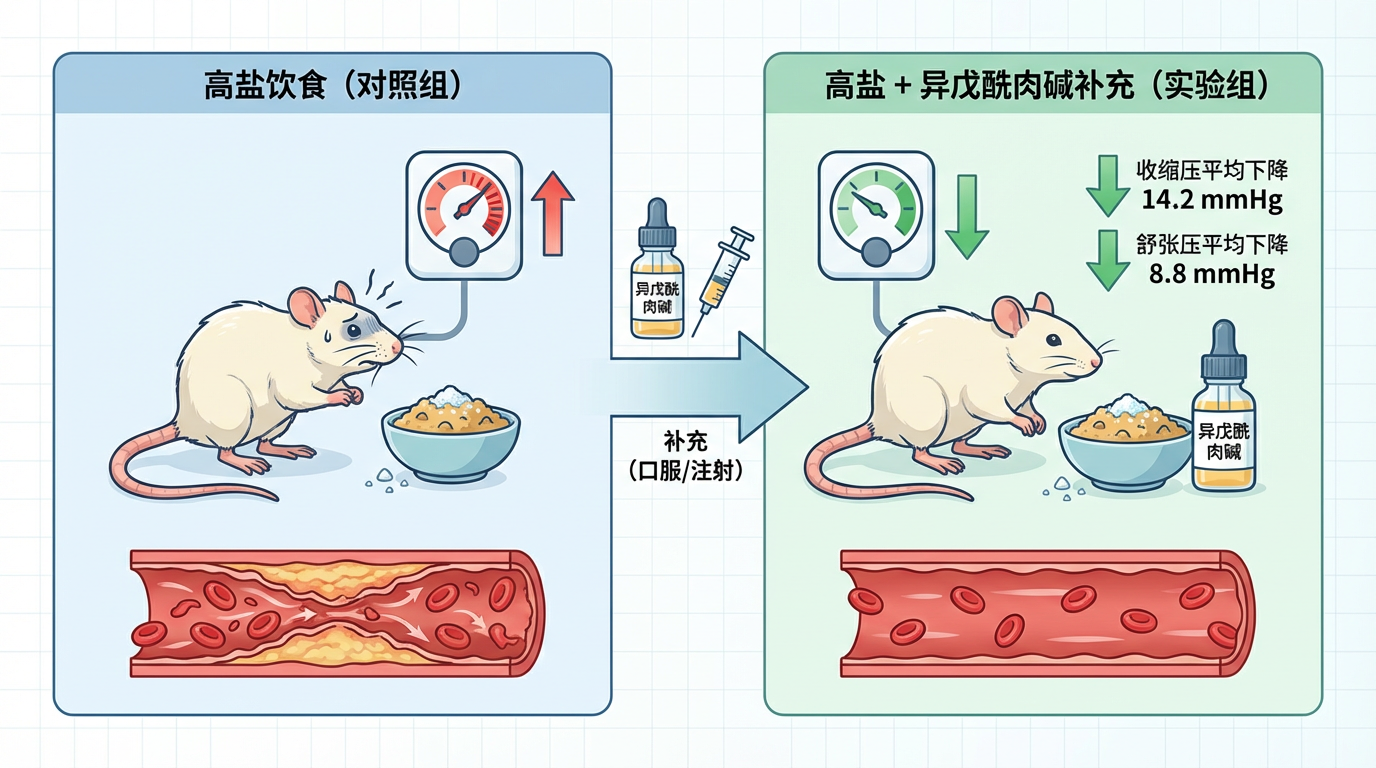
至此,拼图终于完整。高盐饮食通过扰乱肠道菌群,导致了关键保护性代谢物——异戊酰肉碱的减少,从而打开了盐敏感性高血压的闸门。我们每个人对盐的不同反应,很大程度上取决于我们肠道内的微观生态能否抵御这场“盐分风暴”。
这项研究的意义远不止于揭示了一个复杂的生物学机制。它为全球数亿高血压患者,尤其是那些深受盐敏感性困扰的人群,带来了全新的希望。传统的“一刀切”式低盐饮食建议,虽然有效,但并未触及问题的核心——个体差异。
现在,我们有了新的武器库:
这标志着高血压防控策略可能从宏观的饮食限制,迈向微观的、基于肠道生态的精准营养干预时代。
当然,任何一项突破性研究都只是打开了一扇门,门后的世界仍有广阔的未知等待探索。哪些特定的菌群是生产异戊酰肉碱的主力军?补充异戊酰肉碱的长期安全性与有效剂量如何确定?这些问题将是未来研究的重点。
但无论如何,这项源自中国的研究已经深刻地改变了我们对盐、肠道与血压之间关系的认知。它告诉我们,健康并非孤立的器官功能总和,而是一个由我们自身与体内亿万共生伙伴共同维系的动态平衡。我们与肠道菌群的关系,不再是简单的房东与房客,而是休戚与共的命运共同体。
下一次,当你面对一盘美食犹豫是否盐分超标时,或许可以换一个角度思考:我体内的微生物伙伴们,准备好迎接这场挑战了吗?而这,正是精准健康管理的未来所在——一场向内探索,与我们体内微观世界和谐共生的旅程。
点击催更,成为大圆镜下一个视频选题!