对抗知识焦虑,从看懂这条开始
App 下载
靶向双靶点ADC,为晚期前列腺癌患者续上生命
中位生存期|复旦大学|双靶点ADC|转移性去势抵抗性前列腺癌|前列腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
中位生存期|复旦大学|双靶点ADC|转移性去势抵抗性前列腺癌|前列腺癌|肿瘤学|医学健康
72岁的老陈在确诊前列腺癌第三年,还是走到了最凶险的那一步——转移性去势抵抗性前列腺癌(mCRPC)。他试过了新一代雄激素抑制剂,也做了化疗,但肿瘤还是在骨头里疯长,医生说他的中位生存期只剩14个月。这是全球每一位晚期前列腺癌患者最终都可能面对的绝境:所有标准疗法失效,剩下的只有等待。直到复旦大学的研究团队,给这个绝境砸开了一道缝——他们用一款同时瞄准两个靶点的新型抗癌药,让像老陈这样的患者中位生存期翻了近一倍。这不是科幻,是刚刚发表在《Journal of Clinical Investigation》上的真实临床数据。为什么这款药能打破之前的治疗僵局?
你可以把这款名为Iza-bren的双特异性抗体-药物偶联物(ADC),想象成一枚精准制导的“双头导弹”——它的前端是两个能精准识别癌细胞的“导航头”,分别瞄准癌细胞表面的EGFR和HER3蛋白;尾部则绑着一枚拓扑异构酶I抑制剂“弹头”,能直接炸碎癌细胞的DNA。
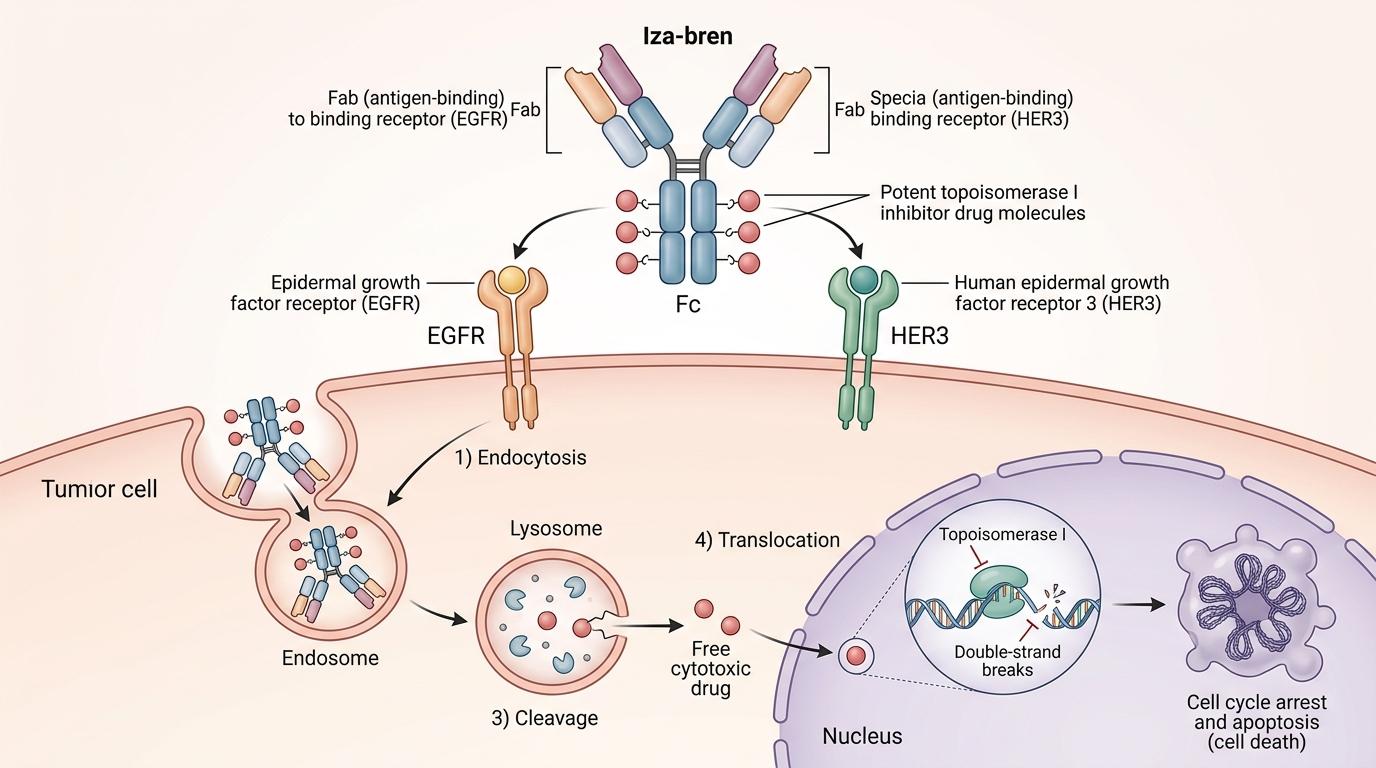
不同于传统单靶点ADC只能盯着一个标记物,这款双靶点设计刚好踩中了mCRPC的命门:EGFR会推着癌细胞到处转移,HER3则会帮癌细胞稳住雄激素受体,让它们对雄激素抑制剂产生耐药性。当两个靶点同时被锁定,不管癌细胞靠哪条路子存活,都逃不掉被“导弹”精准命中的结局。
实验室里的验证结果直接且残酷:在前列腺癌细胞系、小鼠异种移植物和患者来源的类器官中,这款ADC都展现出了极强的靶向杀伤力。更关键的临床数据是,在EGFR和HER3高表达的mCRPC患者中,客观缓解率达到了近50%,中位总生存期从原来的14-15个月,拉长到了24.8个月。
但癌细胞从来不会坐以待毙。研究团队很快发现,一部分患者在接受治疗一段时间后,肿瘤又开始卷土重来。通过分析耐药肿瘤的基因,他们找到了罪魁祸首——ABCG2蛋白。
你可以把ABCG2当成癌细胞细胞膜上的“排风扇”,它能把进入细胞内的化疗药、靶向药甚至ADC的“弹头”,一股脑地排到细胞外,让药物还没发挥作用就被赶了出去。研究人员在耐药患者的肿瘤组织里,清晰地看到了ABCG2的表达量大幅上升,就像癌细胞为了活命,紧急启动了这条“逃兵通道”。
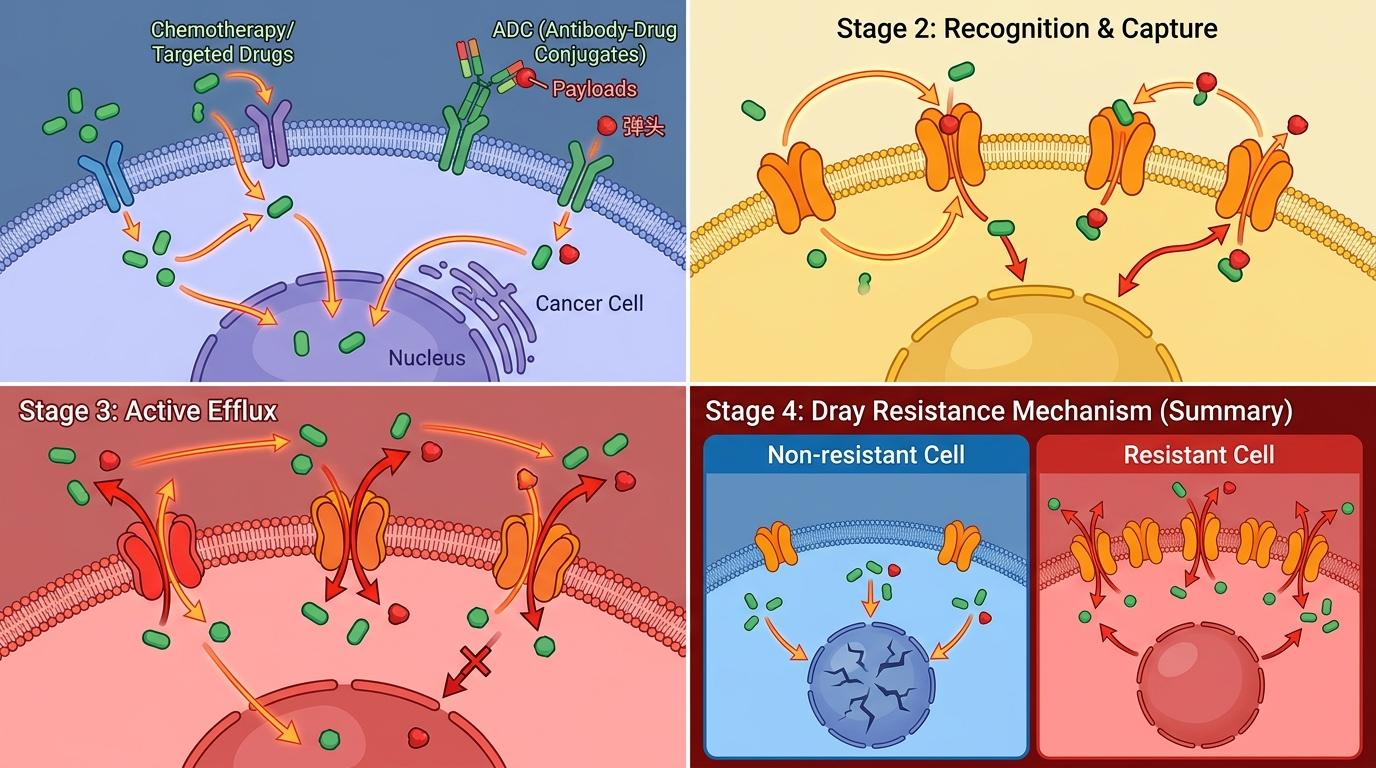
更重要的是,他们找到了关上这条通道的钥匙:不管是通过基因敲除让ABCG2失去活性,还是用名为Ko143的抑制剂堵住它,都能让耐药癌细胞重新对ADC敏感。甚至还有一款正在临床试验的MNK1/2抑制剂Tinodasertib,也能通过抑制ABCG2的ATP酶活性,让它转不动“排风扇”。这意味着,未来只要把ADC和ABCG2抑制剂联用,就能把癌细胞的这条后路彻底堵死。
这款双靶点ADC的潜力,远不止于mCRPC。在之前的非小细胞肺癌临床试验中,它针对EGFR exon20插入突变患者的客观缓解率达到了69.2%,而这类患者原本几乎没有有效的靶向药可用;在三阴性乳腺癌的三期试验中,它也显著延长了患者的无进展生存期和总生存期,是首个在这个适应症中取得阳性生存数据的双特异性ADC。
不过,它也并非完美。临床数据显示,约70%的患者会出现3级及以上的血液学毒性,比如贫血、中性粒细胞减少,虽然大多能通过支持治疗和剂量调整控制,但这依然是未来需要优化的方向。而且,目前它只对EGFR和HER3高表达的患者效果最好,如何通过生物标志物精准筛选适合的患者,也是接下来临床应用的关键。
更值得注意的是,这款药的成功,给整个ADC领域指明了一个新方向:双靶点甚至多靶点的设计,不仅能覆盖更多的肿瘤细胞,还能从根源上减少单一靶点带来的耐药风险。
当我们把目光从实验室的数据拉回到病房里的老陈,这款药的意义就变得格外具体——它不是一个冰冷的科研成果,而是能让老陈多陪家人吃几顿年夜饭的希望。
从单靶点到双靶点,从被动应对耐药到主动预判堵截,人类对抗癌症的每一步,都是在和癌细胞的“狡猾”斗智斗勇。精准瞄准,才能让希望落地。未来,随着更多双靶点ADC的研发和耐药机制的破解,我们或许能给更多像老陈这样的晚期癌症患者,续上更长、更有质量的生命。