对抗知识焦虑,从看懂这条开始
App 下载
帕金森更凶亚型的元凶,藏在肠道里
睡眠障碍|Signal Transduction and Targeted Therapy|肠道菌群|快速眼动睡眠行为障碍|帕金森亚型|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
睡眠障碍|Signal Transduction and Targeted Therapy|肠道菌群|快速眼动睡眠行为障碍|帕金森亚型|神经退行性疾病|医学健康
深夜的卧室里,张阿姨被身边的动静惊醒——老伴正挥着拳头喊“别过来”,胳膊重重砸在她肩上。这不是普通的做噩梦,而是快速眼动睡眠行为障碍(RBD),每两个帕金森患者里就有一个会出现这种情况。更可怕的是,有这种睡眠问题的帕金森患者,手抖得更厉害,忘事更快,连血压心跳的调节都出问题,是医生眼里“更凶”的亚型。一直以来,没人说得清为什么这类患者的病情会急转直下,直到2026年初发表在《Signal Transduction and Targeted Therapy》上的一项研究,把线索指向了我们肚子里的肠道菌群。
健康人的肠道菌群像个勤恳的加工厂,靠分解膳食纤维产生短链脂肪酸——这种物质是肠道屏障的“粘合剂”,能牢牢守住肠壁,不让坏东西跑进血液,还能抑制炎症。但在伴有RBD的帕金森患者体内,这套系统彻底乱了。
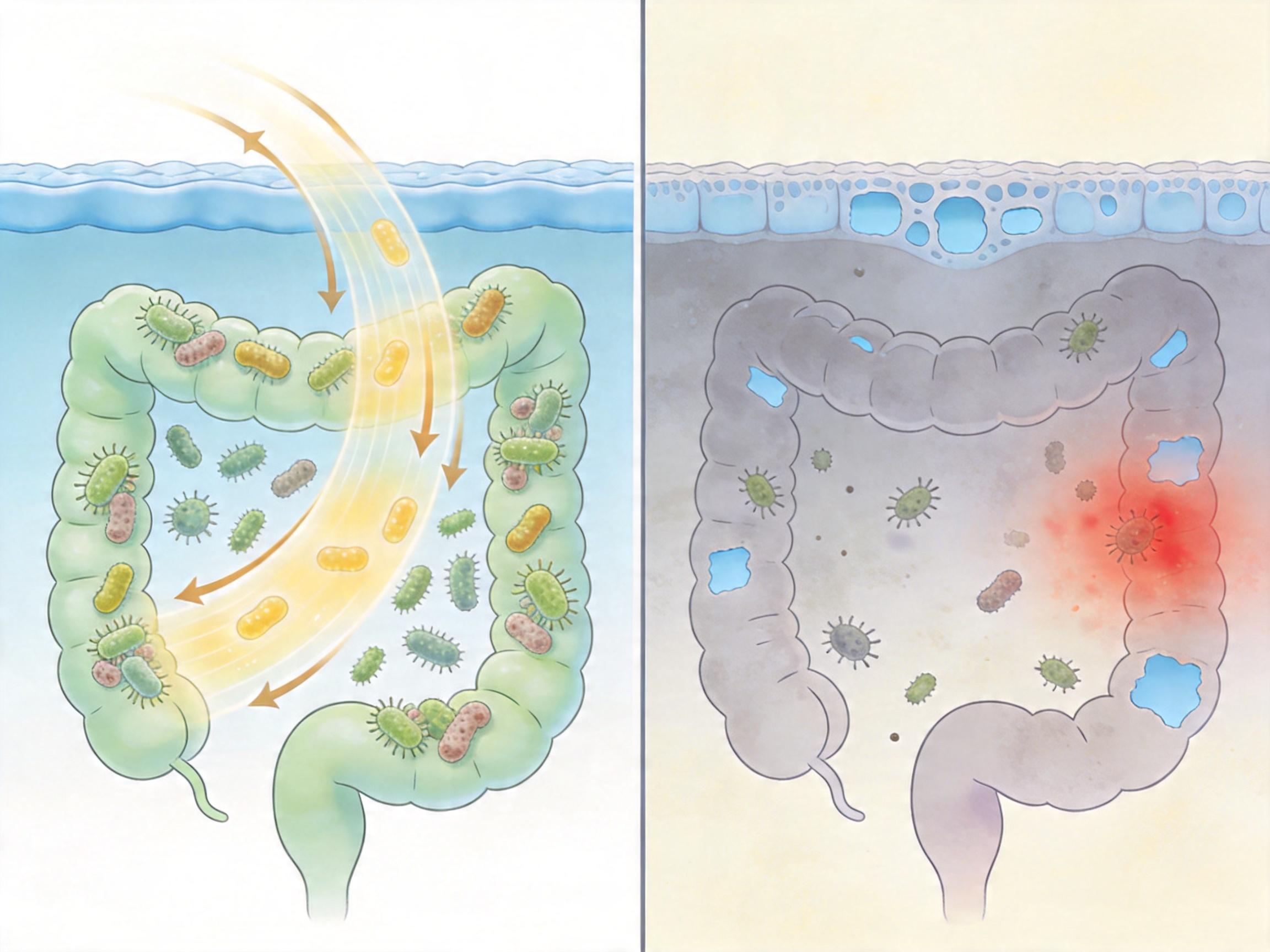
研究团队对比了135名伴RBD帕金森患者、113名不伴RBD患者和102名健康人的血液与粪便样本,发现前者的肠道菌群完全换了“食谱”:原本爱吃膳食纤维的益生菌(比如Faecalibacterium、Roseburia这类产短链脂肪酸的菌群)数量骤减,而专门分解蛋白质和肠道黏液层的细菌变得异常活跃。 这些“叛变”的细菌分解食物里的酪氨酸和苯丙氨酸,会产生一种叫p-甲酚的有毒物质。它在体内转化为硫酸盐和葡萄糖苷酸盐后,能轻易穿透血脑屏障——就像撬开了大脑的防盗门,不仅会直接损伤神经元的线粒体,还会激活炎症反应,让大脑里的“清道夫”小胶质细胞失控攻击神经细胞。更关键的是,这种毒素在还没出现手抖等运动症状的前驱期患者体内就已经存在,说明它可能是触发疾病的“先遣队”。
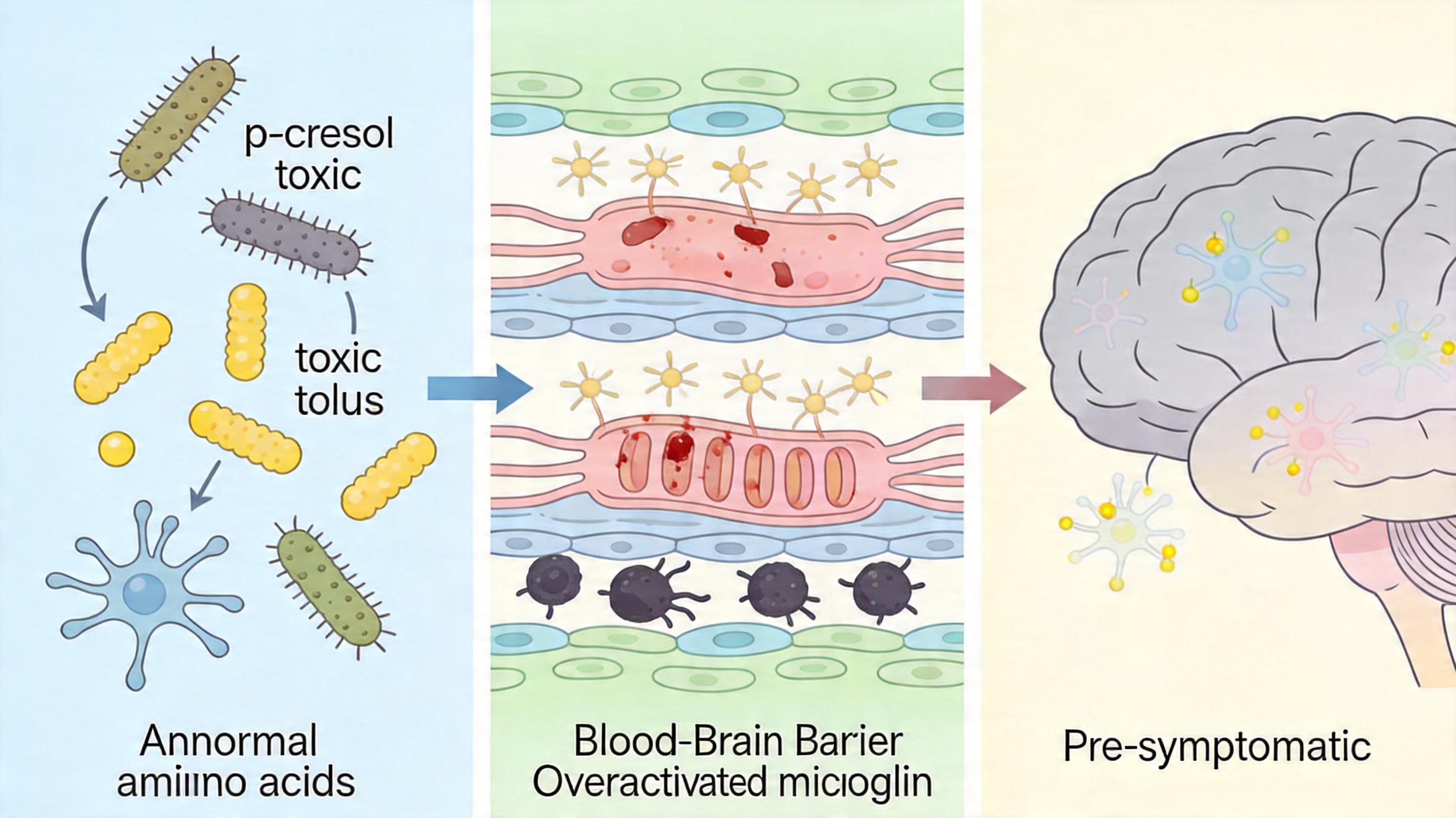
如果说肠道毒素是外来的敌人,那患者自身的抗氧化系统失灵,就是内部的“防线崩溃”。 研究发现,伴RBD的帕金森患者体内,甘氨酸水平明显降低,而5-氧代-L-脯氨酸水平升高——这是身体发出的红色警报:负责清除自由基的谷胱甘肽合成出了问题。谷胱甘肽就像细胞里的“消防员”,专门扑灭氧化应激产生的“火苗”,但甘氨酸是合成它的关键原料,原料不足,“消防员”的数量自然锐减。 与此同时,患者体内的NCF2蛋白水平大幅升高,这种蛋白会催生大量活性氧——相当于在已经着火的房间里又泼了汽油。一边是毒素源源不断涌入大脑,一边是自身的抗氧化能力节节败退,神经细胞在双重打击下加速死亡,这也解释了为什么这类患者的运动和认知衰退会更快。 更值得关注的是,所有帕金森患者都存在共性的代谢问题:三羧酸循环(细胞产能的核心流水线)下游堵塞,导致乳酸、丙酮酸等半成品堆积;脂质代谢紊乱,细胞膜的“建材”出现缺口;炎症因子IL-1β升高,神经保护蛋白MANF下降。而伴RBD患者的肠道毒素问题,是在这些共性问题上又加了致命的一层。
研究团队从海量代谢数据里,筛选出了9种能精准区分两类帕金森患者的代谢物——包括p-甲酚硫酸盐、甘氨酸、5-氨基戊酸等。用这9种代谢物构建的预测模型,在独立样本中的准确率超过90%,这意味着未来只要抽一管血,就能提前识别出那些病情会快速进展的高风险患者。 更重要的是,这些发现为治疗指明了新方向。既然肠道菌群是问题的源头,那么修复肠道微生态就成了关键:地中海饮食能增加产短链脂肪酸的益生菌,减少炎症;粪菌移植在动物模型中已经显示出能改善帕金森样症状的潜力;GLP-1受体激动剂(原本用于糖尿病的药物)也可能通过调节肠脑轴,间接保护神经细胞。 不过目前这些干预手段还处于早期阶段,比如粪菌移植的长期效果、个体化菌群调整的方案,都还需要大规模临床试验验证。但至少我们不再是在黑暗中摸索,终于抓住了那根连接肠道和大脑的关键线索。
过去我们总把帕金森当成一种“大脑病”,专注于黑质多巴胺神经元的死亡,却忽略了肠道这个“第二大脑”的信号。这项研究让我们意识到,神经退行性疾病的源头可能不在大脑,而在肚子里的菌群失衡。 “肠脑相连,菌动神经”,这不仅是对帕金森亚型机制的新认知,更可能是未来神经疾病治疗的突破口。或许再过十年,医生面对帕金森患者,除了开左旋多巴,还会开出一张调整肠道菌群的处方——毕竟,守护大脑的健康,可能要从守护肠道的菌群开始。