
12 天前

12 天前
当你连续三个月被KPI追着跑、深夜还在回工作消息时,你可能没意识到,这种每天都挥之不去的压力——也就是医学上的慢性应激——正在悄悄撬动你的身体平衡:情绪越来越容易崩溃,体检报告上的血糖指标也开始超标。35%的成年人每天都在经历这种无形的侵蚀,它一边催生焦虑,一边把人推向糖尿病的边缘。过去我们只知道压力会影响心情和血糖,却始终没搞懂,这两个看似不相关的问题,到底是被什么东西串在了一起。厦门大学的最新研究,终于找到了这个藏在大脑里的关键开关。
你可以把杏仁核想象成大脑里的「情绪调度中心」,它像个24小时不打烊的指挥室,专门处理恐惧、焦虑这类应激信号。而在这个指挥室里,星形胶质细胞是最勤恳的后勤团队——它们不仅给神经元提供能量补给,还负责合成一种叫L-丝氨酸的关键物质,再通过「丝氨酸穿梭」机制,把L-丝氨酸运给神经元,帮神经元合成D-丝氨酸,维持神经信号的正常传递。
但慢性应激会彻底打乱这个后勤系统。研究发现,持续的压力会激活一种叫PBX1的转录因子,它会精准地抑制星形胶质细胞里的HK2酶——这个酶是糖酵解的关键节点,就像后勤仓库的钥匙。钥匙没了,L-丝氨酸的合成直接陷入停滞,丝氨酸穿梭的传送带断了,神经元得不到足够的D-丝氨酸,就像士兵断了弹药,神经信号的平衡被彻底打破。
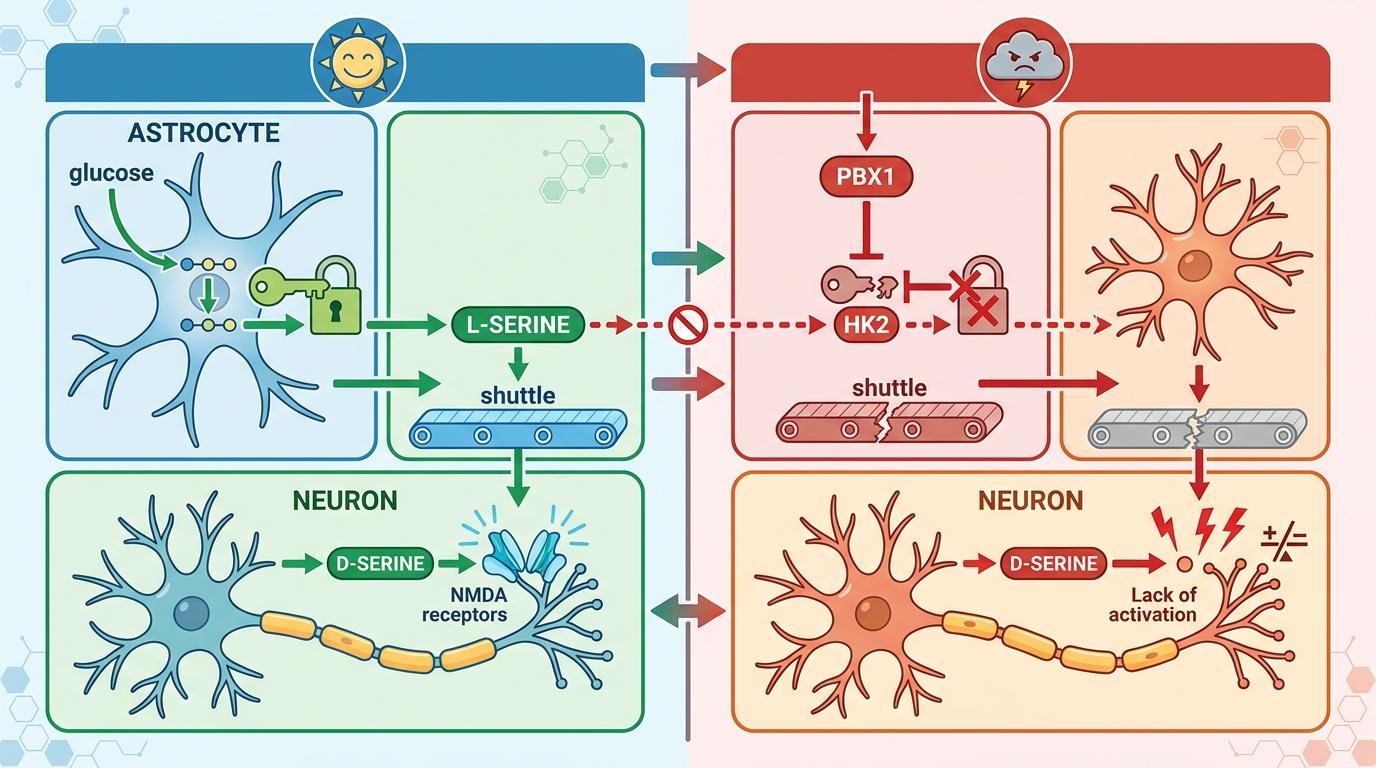
更糟的是,HK2的缺失会直接催星星形胶质细胞的衰老:细胞不再分裂,开始分泌大量炎症因子,整个杏仁核的环境从「后勤保障区」变成了「炎症灾区」。这就是压力引发的第一个多米诺骨牌——杏仁核的星形胶质细胞先垮了。
杏仁核的混乱不会只停留在大脑里。它还通过神经通路直接连接着胰腺——这个调节血糖的核心器官,而连接它们的是两套相互制衡的神经:交感神经像「油门」,会抑制胰岛素分泌、升高血糖;副交感神经像「刹车」,能促进胰岛素释放、降低血糖。正常情况下,这两套神经配合默契,把血糖稳稳地控制在安全区间。
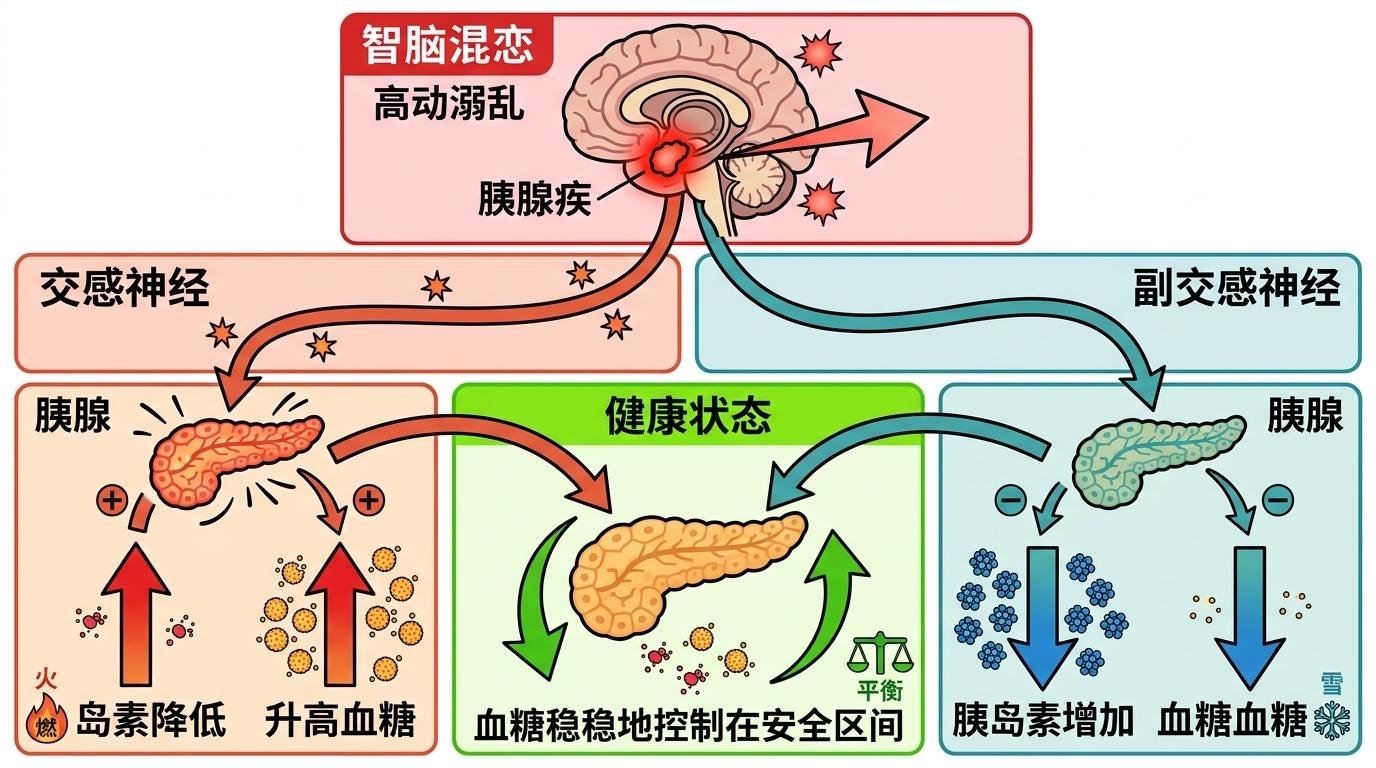
但当杏仁核的星形胶质细胞衰老,神经元的D-丝氨酸不足时,这套平衡就彻底被打破了。研究人员观察到,此时的神经信号会一边倒地偏向交感神经:油门被踩到底,刹车却失灵了。胰腺接收到的全是「升高血糖」的指令,胰岛素分泌被抑制,肝脏还在一个劲地释放葡萄糖,高血糖就这样找上门来。
更致命的是,这种神经失衡还会反向影响大脑:交感神经的过度兴奋会进一步刺激杏仁核,让焦虑情绪陷入恶性循环。就像一个人越焦虑越容易血糖升高,血糖越高又会加重焦虑——这就是压力把情绪和血糖绑在一起的完整链条。
有意思的是,当研究人员给小鼠补充L-丝氨酸,或者用达沙替尼和槲皮素清除掉衰老的星形胶质细胞时,小鼠的焦虑行为明显缓解,血糖也回到了正常水平。这相当于给断了的后勤传送带接上了电源,又把混乱的指挥室重新整理了一遍。
不过这个机制并不是对所有人都一模一样。研究发现,星形胶质细胞的衰老速度和应激反应存在明显的性别差异:雌性小鼠的星形胶质细胞对压力更敏感,衰老速度更快,也更容易出现焦虑和血糖问题;而雄性小鼠的星形胶质细胞则更依赖线粒体功能,对代谢压力的反应模式完全不同。这也解释了为什么女性在焦虑症和糖尿病的共病率上,要比男性高出不少。
当然,目前的研究还有不少未解之谜:比如PBX1到底是被压力的哪个信号激活的?不同脑区的星形胶质细胞衰老是否会有不同的影响?长期补充L-丝氨酸或者清除衰老细胞,会不会有潜在的副作用?这些问题都还需要更多的研究来回答。但至少现在,我们终于跳出了「压力影响心情、压力影响血糖」的表面认知,摸到了藏在大脑深处的那个关键枢纽。
当我们谈论压力对健康的影响时,总习惯把情绪和身体分开来看:焦虑去看心理科,血糖高去看内分泌科。但这项研究却告诉我们,从大脑里的一个胶质细胞,到胰腺的神经信号,再到我们每天的情绪和血糖,这是一个环环相扣的完整系统。
脑内胶质衰,身畔糖与哀。这句话精准地概括了慢性应激对身体的影响:大脑里的星形胶质细胞一衰老,焦虑和高血糖就会接踵而至。未来的治疗或许不再是头痛医头、脚痛医脚,而是从修复大脑里的这些「后勤细胞」开始,把被压力打乱的身体平衡,一点点地拉回正轨。毕竟,我们对抗的从来不是压力本身,而是压力在身体里埋下的那些看不见的隐患。
点击充电,成为大圆镜下一个视频选题!